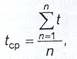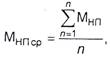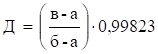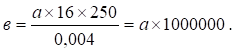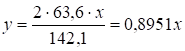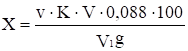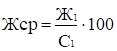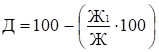|
|
ГІГІЄНА МОЛОКА І МОЛОЧНИХ ПРОДУКТІВ Електронний посібник |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
9. Лабораторні методи контролювання якості та безпечності молока |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
9.1. Відбір середніх проб молока для
досліджень 9.2. Методи консервування проб молока для
досліджень 9.3. Біосенсорне оцінювання молока. Дефекти органолептичних показників молока 9.4. Методики визначення температури та
маси нетто згідно з ДСТУ 6066 9.5. Визначення чистоти молока згідно з
ДСТУ 6083 9.6. Визначення густини молока згідно з
ДСТУ 6082 9.7. Визначення кислотності молока 9.8. Визначення термостійкості молока і
вершків за алкогольною пробою згідно з ДСТУ 5073 9.9. Визначення масової частки жиру в
молоці 9.10. Мікроскопія жирових кульок 9.11. Визначення масової частки білків у
молоці 9.12. Визначення масової частки молочного
цукру 9.13. Визначення масових часток сухої
речовини і води у молоці 9.14. Визначення показників якості молока
за допомогою аналізатора «Ekomilk» 9.15. Визначення вмісту вітамінів у
молоці 9.16. Методи визначення фальсифікації
молока 9.17. Визначення у молоці інгібувальних
речовин 9.18. Методи контролю температурної
обробки сирого молока 9.19. Визначення кетонових тіл у молоці 9.20. Методи визначення молока,
отриманого від корів, хворих на мастит 9.21. Визначення крові та гною у молоці 9.22. Кількісна реакція на бруцельоз 9.23. Мікробіологічні дослідження молока
і молокопродуктів 9.1. Відбір середніх проб молока для досліджень Відбір середньої проби
молока для досліджень. Склад молока змінюється в досить широких межах, тому
необхідно правильно відібрати і скласти середні проби. Правила відбору
середніх проб молока регламентують такі нормативні документи: 1) «Порядок
відбору зразків продукції тваринного, рослинного і біотехнологічного
походження для проведення досліджень (2002 p.)»; 2) «Правила
ветеринарно-санітарної експертизи молока і молочних продуктів та вимоги щодо
їх реалізації (2004 р.)»; 3) ДСТУ 3662:2015
«Молоко коров’яче − сировина. Технічні умови». Середня проба має
відображати склад молока певної партії. Залежно від
поставленої мети розрізняють середню пробу молока від окремих корів, групи
тварин, товарного молока. Згідно з «Порядком
відбору зразків продукції тваринного, рослинного і біотехнологічного
походження, для проведення досліджень», партією вважають призначену для контролю
сукупність одиниць продукції одного найменування в одній тарі з однаковими
фізико-хімічними і органолептичними показниками (одного ґатунку),
виготовлених на одному підприємстві, за однакового технологічного обладнання
впродовж одного технологічного циклу, за одним супровідним документом. Середня проба (об’єднана) – частина продукту, відібрана з усіх ємностей чи
одиниць упаковки, що представлені для експертизи. Під час хімічних та
бактеріологічних досліджень методика відбору середніх проб є різною (ДСТУ ІSО 5538:2004). Лабораторний зразок – установлена правилами певна частина середньої проби;
її виділяють тоді, коли середня проба занадто велика за масою чи об’ємом. У
разі експертизи молока і молочних продуктів, у лабораторіях
ветеринарно-санітарної експертизи середня проба є одночасно й лабораторним
зразком. Згідно з Правилами
ветеринарно-санітарної експертизи молока та молочних продуктів та вимог щодо
їх реалізації (2004 р., п. 6), огляду та аналізу підлягає усе молоко з кожної
доставленої тари. Проби беруть з різних шарів продукту в кількості: молоко –
не менше 250 см3 мірним черпачком (рис. 66, 67).
Відбір середніх
проб молока є дуже відповідальним етапом у комплексі лабораторних досліджень.
Правильно відібрані середні проби повністю характеризують склад
досліджуваного молока. Некваліфіковано відібрані середні зразки можуть бути
джерелом помилкових висновків. Під час дослідження
молока в умовах молокоприймальних та зливних пунктів, сепараторних відділень,
приймальних відділень молокопереробних підприємств, середні проби молока
відбирають до його обліку. У разі дослідження
складу молока окремих тварин, проби беруть безпосередньо у тваринницьких
приміщеннях або літньому таборі. Для якісного оцінювання молока загалом по стаду, відбір
проб проводять безпосередньо у приміщеннях або молочному відділенні. В умовах
лабораторії ветеринарно-санітарної експертизи на агропромислових ринках,
середню пробу відбирають з кожної ємності (тари, посуду) з молоком для
продажу. Стійлову пробу
відбирають у випадку різких відхилень хімічного складу молока (масова частка
жиру, густина) від нормативних показників та підозри на фальсифікацію. Проби відбирають
в умовах тваринницьких ферм після завершення доїння і не пізніше 2-ох діб після досліджень контрольних проб у присутності представника
господарства. Відбір проб проводять за однакових умов годівлі, в один час
доби, від тих же тварин, забезпечують повноту їх видоювання. Видоювання має
бути повним. Середню контрольну пробу беруть безпосередньо із доїльного
апарату не менш ніж 250 см3. Перед відбором
середніх проб для досліджень з ємностей молоко необхідно ретельно перемішати
для недопущення підняття молочного жиру на його поверхню. З цією метою молоко
в залізничних та автомобільних цистернах перемішують механічними колотівками
(від 15–20 с до 3–4 хв) та колотівками (8–10 разів). Молоко у флягах
перемішують колотівкою повільними круговими рухами та зануренням її зверху
вниз 8–10 разів.
Під час відбору
середніх проб від партії молока, що знаходиться в кількох ємностях (фляги, ванни,
цистерни), з кожної ємності відбирають пропорційну кількість молока. Під час відбору
проб молока від окремих корів, стада чи групи корів, середню пробу складають
з пропорційних порцій усіх добових надоїв (ранок, обід, вечір або ж ранок). Якщо є потреба
досліджувати молоко від значної кількості корів, складається графік відбору
середніх проб від тварин окремих груп. Проби молока
відбирають механічними або пластмасовими трубками діаметром не менше Металічні трубки,
черпаки, колотівки для відбору середніх проб повинні бути покриті
антикорозійними сплавами. Під час
дослідження густини, ступеня чистоти, масової частки білків, цукру, об’єм
проби має складати 250–300 см3, у разі визначення кислотності й
масової частки жиру – до 50 см3. Під час відбору
середніх проб молока трубку попередньо
споліскують молоком (опускають у молоко, не закриваючи отвір, і
виймають). Після перемішування трубку повільно занурюють до дна бідона так,
щоб рівень молока в ній і ємності був однаковим. Затиснувши верхній отвір
трубки великим пальцем, її строго вертикально переносять у чисту пляшечку з
притертим корком. Пляшечки із середніми пробами закривають гумовими корками.
На пляшечки наклеюють етикетки, де вписують назву господарства (ферму),
тварини, дату відбору зразка. У разі масових досліджень пляшки зберігають у
спеціальних переносних ящиках з гніздами. Пляшки (заповнені на ¾
об’єму) періодично струшують. Під час відбору стійлових проб пляшечки в
присутності представника господарства опечатують, охолоджують і направляють
на дослідження. Із партій питного
молока, розфасованого у пляшечки чи пакети (мішечки), проби відбирають з
кількості: 1) до 100 ящиків –
1–2 одиниці фасування; 2) від 100 до 200
ящиків – 2–3 одиниці фасування; 3) від 200 до 500
ящиків – 3–4 одиниці фасування; 4) від 500 до 1000
ящиків – 4–5 одиниць фасування. Із партій молока,
доставленого у флягах, середні проби відбирають у 5 % від загальної кількості фляг. Якщо відібрані проби не
піддають негайному дослідженню, їх консервують і зберігають у ємностях з льодяною
водою. Проби для мікробіологічних досліджень відбирають у стерильні пляшечки
чи колби, закриваючи їх ватними корками. Якщо неможливо дослідити їх відразу, проби зберігають за температури від 0 до 6° С до 4 год. Для контролю
молока і молочних продуктів у цистернах за фізико-хімічними і
мікробіологічними показниками відбирають об’єднану пробу від кожної партії
продукції. Об’єм об’єднаної проби – 1000 см3. Для контролю
якості молока і молочних продуктів у транспортній або споживчій тарі за
органолептичними та фізико-хімічними показниками від кожної партії продукції
відбирають вибірку. Об’єм вибірки партії молока в транспортній тарі становить
5 % одиниць транспортної тари з продукцією; за наявності в партії менше 20
одиниць – відбирають одну. Підморожене молоко
перед відбором проб підігрівають до температури 50 °С і перемішують. Після
перемішування молока пробник повільно занурюють до дна посуду і, закривши
верхній отвір трубки великим пальцем, переносять молоко в сухий чистий
скляний посуд з гумовими корками (рис. 67). У теплу пору року
молоко досліджують на кислотність через кожні 2 год у період реалізації або за проханням споживачів. Проби молока і молочних продуктів, що вимагають складних досліджень (на
токсичні елементи, мікотоксин, антибіотики, пестициди, гормональні препарати
тощо), – один раз у квартал мають досліджувати в
державних лабораторіях ветеринарної медицини згідно з Обов'язковим
мінімальним переліком досліджень сировини, комбікорму, вітамінних препаратів
та ін., які потрібно провести в державних лабораторіях ветеринарної медицини
і за результатами яких видають ветеринарне
свідоцтво (форма № 2). До отримання
результатів досліджень молоко і молочні продукти зберігають за температури не
вище 4°С (для бактеріологічних досліджень). Після відбору проб
молока складають акт відбору. АКТ відбору проб продукції для проведення ветеринарно-санітарної експертизи у державній лабораторії ветеринарної медицини “___”_____________20__р. _______________________ Комісія у складі _______________________________________________________________ (прізвище, ім’я, по-батькові) фахівця міської державної ЛВМ
__________________________________________________ (прізвище, ім’я, по-батькові) представника митної служби _____________________________________________________ (прізвище, ім’я, по-батькові) у присутності
__________________________________________________________________ (прізвище, ім’я, по-батькові)
Разом відібрано
проб ______________, загальною масою _____________________кг. Підприємство
____________________________________________________________ Вагон №
__________Автомобіль № ________Накладна № ______________________ Від “___”
___________20__р. Посвідчення про якість від “____” ____20__р. №_____ ________________________________________________________________________ (ким видано) Ветеринарне
свідоцтво (форма № 2) від “___” ___________________20__р. № Відбір середньої
проби проводять згідно з Порядком відбору зразків продукції
тваринного, рослинного і біотехнологічного походження, затвердженого
постановою Кабінету Міністрів України від 14 червня 2002
р. № 833. Примітка: проби відібрані для проведення ветеринарно-санітарної експертизи і опломбовані _______________________________________________________________________________________ (час) Фахівець
ветеринарної медицини
__________________________________________________________ (підпис) (ініціали та прізвище) Спеціаліст
державної лабораторії ветеринарної медицини
______________________________________________________________________ (підпис) (ініціали та прізвище) Представник митної
служби _________________________________________________________________ (підпис) (ініціали та прізвище) Власник продукції
(представник)_____________________________________________________________ (підпис) (ініціали та прізвище) Проби у кількості
____________штук, масою _____________ кг відправлено за адресою: М.П. Відбір середньої проби вершків для досліджень. Середню пробу вершків з однієї ємності (бідона,
цистерни) відбирають після ретельного перемішування колотівкою (10–15 рухів
уверх і вниз). Якщо на стінках
залишається щільніший шар вершків, його зчищають у загальну масу і знову
перемішують. Перед відбором
проби з ванни чи цистерни вершки перемішують упродовж 2–3 хв у кількох
місцях. Пробу вершків для досліджень відбирають аналогічно пробі молока.
Проби зберігають за температури до 8 °С, заморожування не допускається. Під час відбору
таких проб, трубку двічі споліскують тими вершками, пробу яких будуть
відбирати. Якщо відбирають проби густих вершків, трубку після цього
рекомендується промити теплою водою, а потім вершками, проби яких будуть
відбирати. З циліндричних ємностей одного діаметру пробу відбирають трубкою
один раз, дотримуючись наведених вище правил. Вершки відбирають у кількості Підготовка проб до аналізу. Проби молока і вершків, призначені для визначення
фізико-хімічних показників, перемішують, перевертаючи посуд не менше, ніж
тричі або переливанням в інший сухий посуд кілька разів. У разі визначення
фізико-хімічних показників проби молока і вершків доводять до температури
(20±2) °С. Перед дослідженням
консервовані проби і проби вершків з відстояним шаром за температури (35±5)
°С охолоджують до температури (20±2) °С. Маркування і зберігання проб. На посуд з пробами для аналізу молока і молочних
продуктів має бути наклеєна етикетка або бирка, яку зберігають до завершення аналізу. На ній вказують найменування
здавальника, дату і час забору проб молока та молочних продуктів. Проби
молока піддають аналізу відразу після відбору проб. 9.2. Методи консервування проб молока для досліджень Якщо досліджують
середню пробу молока за кілька діб, або молоко не відразу після взяття проби,
їх або охолоджують, або консервують. Зразки середніх проб молока зберігають охолодженими у посуді з водою і льодом не більше 2-х діб. Якщо більше 2-х діб, то їх консервують двохромовокислим калієм, формаліном або пероксидом водню. Консервовані проби
не можна піддавати органолептичній оцінці та досліджувати на кислотність,
проводити бактеріальне дослідження тощо. Консервувальні речовини вносять у
2–3 прийоми. Зазвичай, консервант додають за відбору проб у
першу добу, і наступні – у процесі зберігання проб упродовж 3–5-и діб. У разі
внесення кожної чергової порції консерванту, вміст пляшечки збовтують.
Законсервовані проби зберігають у темному місці за температури не вище 15 °С. Консервування
дворомовокислим калієм (хромпіком) базується на його окиснювальній дії та
руйнуванні ним протоплазми мікроорганізмів. У разі консервування щодекадних
проб молока, призначених для визначення масової частки жиру, застосовують
насичений розчин дворомовокислого калію (10–11 г дворомовокислого калію
розчиняють у 100 см3 свіжо-кип’яченої води). На кожні 100 см3
молока додають 1 см3 або 10–15 крапель консерванту. Проби молока,
законсервовані дворомовокислим калієм, можна зберігати до 10 діб. Необхідно
пам’ятати, що введений в молоко насичений розчин дворомовокислого калію
підвищує густину та титровану кислотність молока. Кращим для використання є
дворомовокислий калій у вигляді таблеток, у разі їх відсутності, можна
використовувати й інші форми цього консерванту. Консервування формаліном. Формалін (водний розчин
формальдегіду з масовою часткою 38–40%) має бактерицидну дію, що зводиться до
паралічу бактеріальних клітин унаслідок взаємодії з білками. Цей консервант
має різкий запах, безбарвний. Для консервування застосовують 1–2 краплі цієї
речовини на 100 см3 молока. Надлишкова кількість доданого
формаліну впливає на точність визначення жиру у молоці. Проби молока,
законсервовані формаліном, зберігають до 10 діб у темному місці за
температури не нижче 9 °С. У разі неправильного зберігання розчин мутніє з
утворенням осаду. На етикетках з середніми пробами молока з формаліном чи
калієм дворомовокислим пишуть розбірливо: «отрута». Ці проби не можна
використовувати для харчових цілей чи на корм тваринам. Консервування пероксидом водню. Для консервування середніх проб молока використовують
розчин пероксиду водню з масовою часткою 30–33% в кількості 2–3 краплі на 100
см3 молока. Законсервовані проби зберігають упродовж 6–10 діб. Під впливом ферментів молока (каталази та пероксидази)
консервант, який є нестійкою сполукою, розкладається з утворенням кисню, що
діє згубно на ріст і розвиток мікрофлори молока. Консервовані проби
не можна оцінювати органолептично на смак, запах, визначати їх кислотність,
ферменти, мікрофлору. Після аналізу їх також не можна використовувати на корм
тваринам. 9.3. Біосенсорне оцінювання молока. Дефекти
органолептичних показників молока Під час приймання
молоко обов’язково піддають біосенсорному (органолептичному) оцінюванню – визначають колір, запах, смак, консистенцію. На
підставі отриманих результатів установлюють наявність дефектів. Молоко від
здорових корів, за відповідних санітарно-гігієнічних умов – являє собою рідину білого чи жовтувато-білого кольору зі специфічним
запахом чи злегка солодкуватим смаком. Колір молока
визначають у скляному циліндрі з прозорого скла за відбитого денного світла.
Колір нормального молока корів – білий чи злегка жовтуватий. Запах молока.
Визначають його під час переливання з однієї посудини в іншу (з доїльного
відра у молокомір) або під час відкривання ємності, в якій його доставили.
Запах необхідно визначати за кімнатної температури чи після незначного
підігрівання молока в закритому посуді. більш правильним є дослідження запаху молока під час коротких
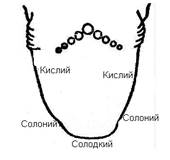
переривчастих вдихів через носову порожнину. Смак (присмак)
молока здорових корів злегка кислуватий. Визначення проводять таким чином: Беруть порцію молока, намагаючись змочити ним всю
порожнину рота до кореня язика. Обов’язково необхідно враховувати місця
фізіологічно найсильнішого відчуття різних смаків (рис. 68).
Необхідно вдихати повітря
і повільно видихати через ніс. Під час дослідження молоко має бути кімнатної
температури. Слабкі присмаки молока краще виявляють за підвищеної
температури. Проте, необхідно враховувати, що за температури вище 36°С
знижується відчуття кислого, гіркого, а нижче 15 °С – інтенсифікуються
відчуття запаху, солоності тощо. Дуже холодне
молоко необхідно підігріти до температури » 30 °С. Консистенція
нормального молока однорідна, без слизу, пластівців білку і не тягуча.
Визначають консистенцію під час повільного переливання молока з циліндра
(хімічної склянки) в інший посуд. Органолептичні
показники молока під впливом різних чинників кормового та бактеріального
походження, можуть набувати різних дефектів. Суттєвий вплив на органолептику
молока має клінічний стан лактуючої тварини та інші фактори. Відхилення
органолептичних показників молока від нормальних класифікуються як дефекти,
що можуть спричинятися різними факторами: захворювання тварин, неправильною
технікою одержання, обробки і зберігання молока, порушеннями годівлі тварин
тощо. Дефекти молока та причини, що їх спричиняють (табл. 61–64) Таблиця 61 Дефекти
кольору молока
Таблиця 62 Дефекти
консистенції молока
Таблиця 63 Дефекти запаху молока
Таблиця 64 Дефекти смаку молока
Оцінювання запаху і смаку здійснюють за п’ятибальною шкалою (табл. 65). Таблиця 65 П’ятибальна система оцінювання запаху і смаку молока
У спірних випадках
дефекти смаку і запаху молока порівнюють зі спеціально приготовленими
еталонами основних дефектів: а) кормовий запах і
смак – перемішують суміш рівних об’ємів підозрюваного корму і води,
фільтрують і до 50 см3 молока додають фільтрат до чіткого
відтворення дефекту; б) «ліполізний» –
до 100 см3 молока додають мікропіпеткою 0,02 см3
розчину масляної кислоти з масовою часткою 1 % і перемішують; в) окиснений – до
50 см3 молока додають, перемішуючи, 1 см3 розчину
сульфату (II) заліза з масовою
часткою 0,3 %. Інші еталони
описані в ГОСТ 28283–89. Відповідно до
бальної оцінки запаху і смаку молока оформлюють експертний лист. Зразок
оформлення експертного листа наведено в таблиці 66. Таблиця 66 Експертний лист Дата оцінки___________Прізвище експерта_____________________
Підпис: _______________ У разі виявлення в
молоці різкого кормового присмаку, гіркоти, невластивих запахів для
нормального молока, невластивого кольору та тягучої консистенції, таку сировину
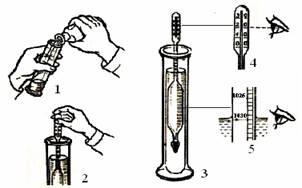
до використання на харчові цілі не допускають. 9.4. Методики визначення температури та маси нетто
згідно з ДСТУ 6066 Метод ґрунтується
на принципі об’ємного розширення термометричної рідини (висота стовпчика
рідини в скляному капілярі) або вимірювання сигналу іншої фізичної природи
(наприклад, електричного) залежно від температури продукту, за умови
теплового контакту між об’єктом вимірювання (продуктом) і чутливим елементом
засобу вимірювальної техніка (термометра). Техніка визначення. Скляні термометри повинні мати захисну оправу.
Температуру вагового продукту у транспортній тарі (цистерни або секції,
бочки, фляги, тощо), визначають одразу після перемішування у відібраних
точкових пробах, що включені у вибірку. Температуру рідких, напівгустих,
густих, в’язких та загущених продуктів у споживчому пакуванні, що включені у вибірку, визначають під час відбирання проб.
Температуру продукту (крім сиру) визначають під час відбирання проб у кожній
пакувальній одиниці, що включена у вибірку. Температуру молочних продуктів
рекомендовано визначати в центрі пакувальної одиниці. Температуру сирів
визначають у кожній одиниці, що включена у вибірку, помістивши термометр
безпосередньо у місце відбирання точкової проби. Температура буде більш
достовірною, якщо її визначати в місцях відбирання проб (цех, склад, камера
тощо). Розкривши пакування, термометр занурюють у продукт не вище нижньої цифрової відмітки
шкали та витримують у ньому від 1 до 2 хв. Відлік показників термометра
проводять, не виймаючи його з продукту, округлюючи значення температури до
найближчої поділки шкали термометра. За кінцевий
результат визначення температури продукту беруть середнє арифметичне значення
всіх температур пакувальних одиниць, що включені у вибірку, округлюючи його
до першого десяткового знака:
де tcp – середнє арифметичне значення температури продукту,
°С; t – значення температури продукту в окремій пакувальній одиниці, °С; n – кількість пакувальних одиниць, що включені у вибірку, шт. Межа допустимої похибки визначення температури продукту не має перевищувати ± 1°С. Визначення маси нетто. Метод ґрунтується на визначенні маси продукту
зважуванням за допомогою вагів та наступного знаходження маси нетто продукту
(без пакування) як різниці між масою брутто (разом із пакуванням) і масою
тари (пакування). Проведення дослідження. Зважування проводять на вагах відповідної
класифікації, класу точності та границь зважування залежно від вимог,
передбачених чинними нормативними документами на продукт. Масу нетто вагового
продукту у транспортній тарі (МНТ)
(цистерни або секції бочки, фляги тощо) визначають на вагах для статичного
зважування, як різницю мас заповненої (МБТ)
та порожньої транспортної тари (МТТ): МНТ = МБТ – МТТ порожньої транспортної тари, кг. де МНТ – маса нетто вагового продукту у
транспортній тарі, кг; МБТ – маса брутто вагового продукту у
транспортній тарі, кг; МТТ – маса Рекомендована
повірочна ціна поділки е (ціна
найменшої поділки шкали для вагів з аналоговим відліковим пристроєм та
дискретність відліку для вагів із цифровою індикацією) вагів, які
застосовують для визначення маси нетто продукту в пакувальній одиниці, має відповідати зазначеній у таблиці 67. Таблиця 67 Рекомендована повірочна ціна поділки вагів
Зважують кожну
пакувальну одиницю продукту з вибірки на вагах та фіксують значення її маси
брутто (МБП). Масу брутто одиниці
продукту у дрібному пакуванні визначають як середнє арифметичне
не менше п’яти пакувальних одиниць продукту. Одну із пакувальних одиниць продукту ретельно звільняють від умісту, упаковки,
промивають, витирають насухо та зважують, або визначають масу того ж
матеріалу і в тій же кількості, яку було використано для пакування одиниці
продукту. Значення його маси беруть за масу спожиткового паковання (МТП) одиниці продукту. Маса нетто
кожної паковальної одиниці (МНП)
визначають як різницю між МБП і МТП: МНП = МБП – МТП, МНП – маса нетто паковальної одиниці продукту, кг (г); МТП – маса спожиткового паковання одиниці продукту, кг (г); МБП – маса брутто паковальної одиниці продукту, кг (г). За кінцевий
результат визначення маси нетто продукту пакувальної одиниці беруть середнє арифметичне значень усієї маси нетто пакувальних одиниць, що включені у вибірку, округлюючи його до першого
десяткового знаку:
де МНП ср – середнє арифметичне значення маси нетто пакувальної одиниці продукту, кг (г); МНП – маса нетто окремої пакувальної одиниці продукту з вибірки, кг
(г); п – кількість пакувальних одиниць продукту, що включені у вибірку, кг (г). 9.5. Визначення чистоти молока згідно з ДСТУ 6083 Суть методу. Метод ґрунтується на відокремлюванні механічних домішок із дослідної
проби молока очищенням через фільтр і візуальним порівнянням механічних
домішок на фільтрі зі зразком порівнювання.
Дослідження
забруднення молока механічними домішками необхідне для виявлення джерел його
забруднення та дозволяє вжити заходів щодо їх усунення. Разом з механічними домішками у молоко потрапляють
мікроорганізми, бактерії, зокрема збудники хвороб.
За наявності великої кількості механічних домішок молоко є недоброякісним. Велика кількість
механічних домішок у молоці (шерстинки, частинки сіна, пісок, гній та ін.)
свідчить про антисанітарні умови його отримання чи транспортування і визначає
придатність молока для безпосереднього споживання чи переробки на молочні
продукти певних видів. Визначення чистоти
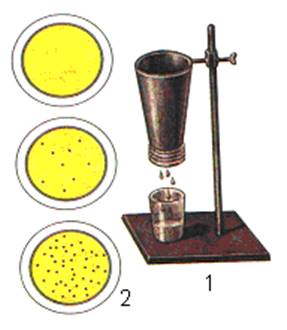
проводять за допомогою приладів системи «Рекорд» (рис. 69). Методика дослідження. 1. Досліджуване молоко попередньо нагрівають до
температури 35 °С для розчинення грудок вершків, що затримують на фільтрі,
«маскують» наявність механічних домішок. Оцінка результату. Ступінь чистоти (наявність механічних домішок)
визначають шляхом фільтрування 250 см3 молока за допомогою
приладів. Два фільтри візуально порівнюють між собою, рахуючи на кожному з
них кількість механічних домішок. За кінцевий результат беруть середнє
арифметичне значення двох показників. Залежно від кількості механічних домішок
на фільтрі молоко відносять до однієї з трьох груп чистоти порівнюванням
фільтра зі зразком порівняння (рис. 70).
Примітка. Колір фільтрату має відповідати кольору молока відповідно до вимог НТД. За
зміни кольору фільтрату молоко, незалежно від кількості механічних домішок на
фільтрі, відносять до третьої групи чистоти. Приклад. За порівняння даних, отриманих під час випробування двох фільтрів,
установлено, що на одному з них кількість механічних домішок – 12 одиниць, а на другому – 20. За кінцевий результат
беруть середнє арифметичне значення двох показників, тобто 16 одиниць
механічних домішок. Отже, посилаючись на зразок порівняння, молоко належить
до третьої групи чистоти.
9.6. Визначення густини молока згідно з ДСТУ 6082 Суть методу. Аерометричний метод полягає у вимірюванні густини молока занурюванням ареометра
в циліндр із дослідною пробою та візуальному відліку показників густини зі
шкали ареометра. Густина молока (молочних продуктів) – співвідношення маси молока
(молочних продуктів) за температури 20 °С до його об’єму. Визначення густини
молока за допомогою ареометра базується на законі Архімеда. В цьому випадку
ступінь занурення ареометра залежить від густини рідини: що вона нижча, то глибше в рідину занурюється ареометр (рис. 71).
Цей показник
широко використовують для перерахунку кількості молока, вираженого в
кілограмах, у літри, й навпаки; для встановлення і контролю натуральності
молока; розрахунків за формулами сухої речовини, сухого знежиреного молочного
залишку (СЗМЗ) та інших компонентів. Густина молока – це співвідношення маси молока за температури 20 °С
до маси рівного об’єму води (t = 4°С) та позначається Г = 20 °С 4 °С. Густина
незбираного коров’ячого молока коливається в межах 1,027–1,033 (в окремих
тварин від 1,026 до 1,031). Ці коливання суттєво залежать від породи, годівлі
та умов утримання тварин, а відповідно, від кількісних змін компонентів
молока, які й визначають його густину. Густина
знежиреного молока є дещо вищою за густину незбираного і становить
1,032–1,036. Вершки мають густину (залежно від жирності) від 1,005 до 1,025 г/см3. Значення густини збільшується у разі
зняття частини вершків чи додавання молочних відвійок до молока. У разі
розведення молока водою, його густина зменшується. У разі додавання
до молока води у кількості 10 %, його густина знижується на 3 °А. Високожирне молоко
може також мати знижену густину. Так, за
жирності молока 4 %, його густина становить 29 °А (1,029 г/см3);
6 %-ї жирності – 1,027 г/см3. Густина щойно
видоєного молока є вищою, ніж через кілька годин після доїння. За цей час
вивітрюється частина газів молока, а жир з рідкого стану переходить у
твердий. У зв’язку цим, густину молока визначають не раніше, ніж через 2 год
після доїння і за температури не нижче 10 °С та не вище 25 °С. Оптимальною
температурою для вимірювання густини молока є 20 ° С. Густину молока
визначають за допомогою спеціального приладу – ареометра (лактоденсиметра). Нижня частина
приладу є розширеною і містить дріб для надання певної ваги приладу та
стійкого вертикального положення під час занурення в молоко. Середня частина
приладу – це шкала з цифрами, яка вказує густину молока в: а) г/см3
(1,015; 1,020; 1,025; 1,030; 1,035 тощо); б) °А (градусах
ареометра: 15°; 20°; 25°; 30°; 35° тощо). Вираження густини
молока у градусах ареометра спрощує розрахунки поправок на температуру і
використовується в деяких розрахунках. Верхня частина
приладу містить шкалу термометра, за якою і визначають температуру
досліджуваного молока. Техніка визначення. Під час дослідження законсервовані проби молока та з відстояними вершками нагрівають до 30–40 °С, перемішують і охолоджують до (20±2) °С. У
арбітражних випадках під час визначення густини молоко необхідно нагріти до (40±2) °С, витримати за цієї температури до (5±1)
хв, після чого охолодити до 20 ± 2 °С. Не потрібно
проводити дослідження густини в молоці під час збивання жиру, його згортання
під дією консерванту – хромпіку.
Проведення дослідження. Циліндр із дослідною пробою встановлюють на рівну горизонтальну
поверхню та вимірюють температуру проби (t1). Відлік показників температури проводять не раніше, ніж через (3±1) хв після
занурення термометра в дослідну пробу (рис. 72). Сухий чистий
ареометр повільно опускають у дослідну пробу, занурюючи його доти, поки до
наміченої відмітки аерометричної шкали не залишиться від Перший відлік
показників густини (δ1) проводять візуально за шкалою ареометра через 3 хв після встановлення
його в нерухомому стані. Після цього ареометр обережно підносять на висоту до
рівня балансу в ньому та знову опускають, залишаючи його у вільно плавальному
стані. Після встановлення ареометра в нерухомому стані, знову проводять
відлік показників густини (δ2). Під час відліку
показів густини очі лаборанта мають знаходитися на
рівні меніска. Відлік показів проводять по верхньому краю меніска. Відлік
показників ареометрів типів АМ і АМТ проводять до половини ціни найменшої
поділки шкали. У ареометрах типів АОН-1 і АОН-2 відлік показників проводять
до ціни найменшої поділки, після чого вимірюють температуру (t2) дослідної проби. Вимірювання
температури проби під час використання ареометрів типів АМ, АМТ, АОН-1 і
АОН-2 проводять за допомогою ртутних і спиртових скляних термометрів. У разі
проведення масових вимірювань густини молока дозволено: під час вимірювання
густини чергової дослідної проби молока торкатися нижнім кінцем ареометра,
який витягують із молока, до внутрішньої поверхні циліндра негайно; після
стікання з ареометра основної частини молока, занурюють його в інший циліндр
із новою пробою молока, не допускаючи засихання молока на поверхні ареометра.
Потім повторюють вимірювання як вказано вище. Опрацювання результатів. За кінцевий результат (t) дослідної проби беруть середнє арифметичне
результатів двох показників (t1) і (t2). Приклад обрахування температури дослідної проби
молока подано нижче. За кінцевий результат показників ареометра за
температури (t (δср)) дослідної проби молока беруть середнє арифметичне
двох показників (δ1) і (δ2). Приклад обрахування густини проби молока подано
нижче. Якщо дослідна
проба під час визначення густини мала температуру, що відрізнялася від 20 °С,
результати визначення густини за температури (t) мають бути приведені до
20 °С, відповідно до вимог таблиць. За таблицями у лівій крайній графі знаходять
рядок із значеннями, а в наступних графах таблиць – температуру (t). На перетині відповідного рядка та графи знаходять
значення густини молока за температури 20 °С, яке беруть за кінцевий результат. Приклади
приведення густини молока до температури 20 °С за таблицями, поданими нижче.
Результат визначення густини молока δм з урахуванням
похибки методу повинен бути представлений у вигляді формули: δм = δт ± Δδа; Р = 0,99, де, δт – значення густини, приведене до температури 20 °С,
знайдене за таблицями, виражене в кг/м3; Δδа – похибка визначення густини молока
аереометричним методом, становить ± 0,5 кг/м3; Р – імовірність, з якою похибка вимірювань знаходиться в межах від мінус Δδа до Δδ. Таблиця 68 Приведення значення густини молока коров’ячого до
температури 20 °С
Таблиця 69 Приведення значення густини молока знежиреного до
температури 20 °С
Таблиця 70 Поправка для визначання фактичної густини молока
коров’ячого в діапазоні температур від 10 до 15 °С
Таблиця 71 Поправка для визначання фактичної густини молока
знежиреного в діапазоні температур від 10 до 15 °С
Приклад 1. Розглянемо можливі випадки під час вимірювання температури t проби молока. У першому: відлік
показів температури становив: t1= 16,0°С і t2= 16,5 °С. Середнє
арифметичне значення температури проби обчислюємо за формулою: t = (16,0+16,5) :2 =16,25 °С. У другому: відлік
показів температури становив: t1 = 15,5 °С і t2= 16,0 °С. Середнє
арифметичне значення температури проби обчислюємо за формулою: t = (15,5+16,0)
:2 =15,75 °С. За кінцевий
результат вимірювань у першому та в другому випадках беруть t = 16,0 °С. Керуються таким правилом: якщо дрібна
частина середнього арифметичного значення температури дорівнює або менша за
0,25 °С, – її не враховують; якщо більша, ніж 0,75 °С, – її зводять до
одиниці; якщо більша, ніж 0,25°С, але менша, ніж 0,75 °С – її зводять до 0,5
°С. Приклад 2. Розглянемо два можливих випадки під час вимірювання густини δср проби молока. У першому: відлік
показів густини склав: δ1 = 1028,5 кг/м3 та δ2 = 1028,0 кг/м3.. Середнє арифметичне
значення густини проби дорівнює: δср = (1028,5+1028,0)
: 2 = 1028,25 кг/м3 У другому: відлік
показів густини склав: δ1 = 1028,0 кг/м3
та δ2 = 1027,5 кг/м3.. Середнє арифметичне значення густини
проби дорівнює: δср = (1028,0+1027,5)
: 2 = 1027,75 кг/м3 За кінцевий
результат вимірювань у першому та в другому випадках беруть δср = 1028,0 °С. Керуються правилом
зведення числового значення δср, викладеного вище
(приклад 1). Фактори, що
впливають на точність досліджень: 1) наявність
механічних домішок і дослідження молока раніше, ніж через 2 год після доїння; 2) недостатнє
перемішування молока перед його дослідженням або надто сильне збовтування, що
приводить до утворення жирових грудочок і повітряних міхурців; 3) консервування
проб 10 % хромпіком. Оцінювання результату. Густина коров’ячого молока знаходиться у межах 1027,0–1032,0 кг/м3.
Середнє значення густини збірного коров’ячого молока дорівнює 1030,0 кг/м3.
Густина молозива у межах 1038,0–1040,0 кг/м3. Густина знежиреного
молока – 1033,0–1035,0 кг/м3, оскільки питома маса жиру менше
одиниці. Густина вершків – 1005,0–1020,0 кг/м3. Пастеризоване
впродовж 30 хв молоко за температури 85 °С або прокип’ячене впродовж 10 хв
має підвищену густину на 0,5–1,4 °А. Густину молока, яке заготовляють, необхідно визначити не раніше, ніж через 2 год після
доїння. Густину молока
можна також визначати ультразвуковим методом згідно з ДСТУ 7057:2009. 9.7. Визначення кислотності молока 1. Визначення
кислотності молока і молочних продуктів шляхом вимірювання величини рН Кислотність молока
визначається шляхом вимірювання рН, а також визначенням титрованої
кислотності. Для визначення рН молока і молочних продуктів застосовуються
рН-метри. Допускається
похибка приладів під час контролю рН молока і молочних продуктів в інтервалі
температури від 5 °С до 40 °С до ±0,05 рН. Співвідношення
титрованої кислотності молока і рН показано в таблиці 72. Таблиця 72 Середні значення співвідношення між величиною рН і титрованою кислотністю
молока коров’ячого незбираного заготовлюваного, пастеризованого,
топленого
2. Визначення кислотності молока і молочних продуктів з
використанням індикатора фенолфталеїну згідно з ГОСТ 3624 Необхідність
визначення кислотності молока зумовлена встановленням його ґатунку,
придатності до подальшої пастеризації та переробки на молочні продукти. Градус Тернера –
це кількість розчину NaOH або КОН (см3) з масовою концентрацією 0,1 моль/дм3
(0,1 н), необхідна для нейтралізації 100 см3 молока, розведеного вдвоє водою
за наявності індикатору фенолфталеїну. Титрована кислотність свіжовидоєного
молока складає 16...18 °Т. Нормативи
кислотності відповідно до ґатунків молока:
Приготування
розчинів: Приготування розчину NaOH з масовою концентрацією 0,1 моль/дм3 (з фіксаналу). Ампулу з
фіксаналом промивають ззовні, споліскують дистильованою водою. У отвір мірної
колби ємністю 1 дм3 поміщають лійку, в отвір якої вставляють пробивач гострим
кінцем догори. Ударяють одним з кінців ампули по пробивачу. Залишаючи ампулу
на місці, роблять отвір з другого боку ампули. Використовуючи промивач,
багаторазово промивають ампулу водою, що стікає в колбу. Вміст колби на 1 дм3
перемішують, доливають до мітки водою, після чого знову перемішують. Приготування
контрольного еталону. У колбу ємністю 150–200 см3 відміряють піпеткою 10 см3
молока, 20 см3 дистильованої води, 1
см3 розчину сірчанокислого кобальту з масовою часткою 2,5 %. Суміш
перемішують. Еталон є придатним упродовж 6–8 год. У разі більш тривалого
використання, до еталона додають 1–2 краплі формаліну. Приготування
розчину сірчанокислого кобальту. У мірну колбу ємністю 100 см3 уносять Техніка
визначення. 1. У конічну колбу ємністю 150–200 см3 наливають 10 см3
досліджуваного молока, 20 см3 дистильованої (питної свіжо-кип’яченої та
охолодженої до кімнатної температури) води. 2. До суміші
додають 3 краплі спиртового розчину фенолфталеїну з масовою часткою 1 % (рис.
73). 3. Уміст колби
титрують, за постійного перемішування розчином натрію гідроксиду, до появи
слабо-рожевого забарвлення, що не зникає впродовж 1 хв та відповідає кольору
еталону. 4. Відраховують
кількість лугу (см3), витраченого на титрування. Оцінка результату.
Кількість розчину натрію гідроксиду, витраченого на титрування, помножена на
10, показує градус кислотності молока (°Т). Розбіжність між двома
паралельними дослідженнями не повинна бути більше 1 °Т.
Фактори, що
впливають на точність визначення: 1) наявність
механічних домішок у молоці; 2) дослідження
проби раніше, ніж через 2 год після доїння; 3) низька (нижче
15°С), або висока (вище 25°С) температура молока; 4) погане
перемішування молока перед початком аналізу або значне його збовтування, що
призводить до утворення жирових коточків та повітряних пухирців; 5) недостатньо
чистий ареометр або циліндр; 6) ареометр
торкається стінок циліндра; 7) консервування
проб молока розчином хромпіку з масовою часткою 10 %. 3. Методи
визначення граничної кислотності молока Суть методу. Метод
використовується за проведення сортування молока і базується на нейтралізації
кислот, що містяться в молоці, надлишковою кількістю гідроксиду натрію за
наявності індикатора фенолфталеїну. Надлишок гідроксиду натрію та
інтенсивність забарвлення в отриманій суміші зворотно пропорційний
кислотності молока. Для визначення
граничної кислотності готують робочі розчини, що визначають відповідний
градус кислотності. Техніка
визначення. 1. У мірну колбу місткістю 1000 см3 відмірюють необхідний об’єм
розчину натрію (калію) гідроксиду з масовою концентрацією 0,1 моль/дм3
відповідно до вимог таблиці 73, додають 10 см3 спиртового розчину
фенолфталеїну з масовою часткою 1 % і доливають дистильовану воду – до мітки. Таблиця 73 Приготування робочих розчинів для визначення граничної
кислотності
2. У ряд пробірок
уносять по 10 см3 розчину гідроксиду натрію з масовою концентрацією 0,1
моль/дм3, приготовленого для визначення відповідного градуса кислотності. 3. У кожну
пробірку з розчином доливають по 5 см3 досліджуваного молока і вміст пробірки
перемішують шляхом її перевертання, попередньо закривши їх гумовою пробкою. Оцінка результату.
Якщо вміст пробірки знебарвлюється, кислотність даного зразка молока буде
вищою від відповідного даному розчину градуса. І, навпаки, якщо забарвлення
суміші в пробірці зберігається, кислотність молока нижча, ніж даний розчин.
Кислотність молока відповідає тій пробірці, де зберігається блідо-рожеве
забарвлення суміші. У лабораторіях
ветеринарно-санітарної експертизи агропромислових ринків звичайно готують
розчин для визначення граничної кислотності 20 °Т. 4. Експресний
метод визначення граничної кислотності молока Цей метод
використовується в державних лабораторіях ветеринарно-санітарної експертизи
агропромислових ринках. Техніка
визначення. 1. У пробірку вносять піпеткою 10 см3 дистильованої води, 1 см3
розчину натрію гідроксиду натрію з масовою часткою 0,1 моль/дм3, 3 краплі
спиртового розчину фенолфталеїну з масовою часткою 1 %. Уміст пробірки
забарвлюється в малиновий колір. 2. Потім у
пробірку приливають 5 см3 досліджуваного молока. Оцінка результату.
Якщо в пробірці зберігається малиновий колір різної інтенсивності, гранична
кислотність менше 20 °Т. Якщо вміст в
пробірці білого кольору, гранична кислотність більше 20 °Т. Молоко з
кислотністю понад 20 °Т визначається як некондиційне. За необхідності,
можна додатково проводити пробу кип’ятінням. Ця проба є особливо ефективною,
якщо змішується молоко з кислотністю 16–18 °Т і 27–28 °Т. Титрована кислотність такого молока не
буде перевищувати 20–22 °Т, але проба кип’ятінням буде позитивною (білки
молока коагулюють). Методика
дослідження. У пробірку наливають 5 см3 молока і кип’ятять упродовж 1 хв.
Якщо молоко під час кип’ятіння зсілося, його кислотність вища за норму. 5. Визначення
кислотності молока з наповнювачами (шоколадне, кавове), вершків, кислого
молока, кефіру, кумису та інших кисломолочних продуктів Техніка
визначення. 1. У колбу ємністю 100 або 250 см3 відмірюють дистильовану воду і
досліджуваний продукт в об’ємах, що вказані у таблиці 74, і 3 краплі
спиртового розчину фенолфталеїну з масовою концентрацією 1 %. 2. Під час
аналізування вершків і кисломолочних продуктів, залишки продукту переносять з
піпетки в колбу шляхом промивання піпетки отриманою сумішшю (3–4 рази). 3. Суміш ретельно
перемішують і титрують розчином гідроксиду натрію з масовою часткою 0,1
моль/дм3 до появи слабо-рожевого забарвлення, для молока і вершків, що
відповідають контрольному еталону забарвлення, що не зникає, – впродовж 1 хв. 4. Для молока з
наповнювачами, для більш точного визначення кінця титрування, разом з
титрованою пробою ставлять контрольну колбу з 10 см3 тієї ж проби молока і 40
см3 дистильованої води (табл. 74). Оцінка результату.
Кількість розчину гідроксиду натрію, витраченого на титрування, помножена на
10, показує градус кислотності молока (°Т). Таблиця 74 Об’єми досліджуваного продукту і дистильованої води
6. Визначення
кислотності плазми вершків Кислотність плазми
вершків у градусах Тернера визначають за формулою (°Т):
де: Х –
кислотність плазми вершків, °Т; а – кислотність
вершків, °Т; ж – масова частка
жиру у вершках, %. 7. Визначення
кислотності сметани, морозива Методика дослідження.
1. У не забарвленому морозиві та сметані кислотність визначають таким чином:
у колбу об’ємом 100 або 250 см3 відважують 2. Суміш ретельно
перемішують і титрують розчином гідроксиду натрію з масовою часткою 0,1
моль/дм3 до появи слабо-рожевого забарвлення, що не зникає впродовж 1 хв. Приготування
еталону: У колбу вносять 20 см3 дистильованої води, додають піпеткою 10 см3
вершків або Оцінка результату.
Кількість гідроксиду натрію (калію), витраченого на нейтралізацію 10 см3
вершків або Кислотність
забарвленого морозива визначають так: 1. У колбу об’ємом
250 см3 відважують 2. Суміш ретельно
перемішують і титрують розчином лугу з масовою часткою 0,1 моль/дм3 до появи
слабо-рожевого забарвлення, що не зникає впродовж 1 хв. 3. Для визначення
кінця титрування забарвленого морозива, колбу з титрованою сумішшю поміщають
на білий лист паперу і рядом ставлять колбу із сумішшю 8. Дослідження
сиру та сирних виробів Методика
дослідження. 1. У фарфорову ступку вносять 2. Потім
невеликими порціями додають 50 см3 води, нагрітої до температури 35...40 °С і
3 краплі спиртового розчину фенолфталеїну з масовою концентрацією 1 %. 3. Суміш ретельно перемішують
і титрують розчином гідроксиду натрію з масовою часткою 0,1 моль/дм3 до появи
слабо-рожевого забарвлення, що не зникає впродовж 1 хв. Приготування
еталону: попередньо розтирають у фарфоровій ступці Кислотність (у
градусах Тернера – °Т) знаходять шляхом множення об’єму (см3), розчину
гідроксиду натрію, витраченого на нейтралізацію кислот, що містяться в
певному об’ємі продукту, на коефіцієнт: 10 – для молока,
молока з наповнювачами, вершків, кислого молока, ацидофільного молока,
кефіру, кумису, і інших кисломолочних продуктів, а також плазми вершкового
масла; 20 – для морозива,
сметани, сиру і сирних виробів. Межа допустимої
похибки результату аналізу за прийнятої достовірної імовірності Р = 0,95,
становить: ±1,9 °Т – для
молока, молока з наповнювачами, вершків, кислого молока, ацидофільного
молока, кефіру, кумису, і інших кисломолочних продуктів, і морозива; ±2,3 °Т – для
сметани; ±3,6 °Т – для сиру
і сирних виробів; ±0,1 °Т – для
масла вершкового і його жирової фази; ±0,5 °Т – для
плазми вершкового масла. Розходження між
двома паралельними визначеннями не повинні перевищувати: 2,6 °Т – для молока,
молока з наповнювачами, вершків, кислого молока, ацидофільного молока,
кефіру, кумису та інших кисломолочних продуктів, і морозива; 3,2 °Т – для
сметани; 5,0 °Т – для сиру
і сирних виробів; 0,1 °Т – для масла
вершкового і його жирової фази; 0,6 °Т – для
плазми вершкового масла. За значного
розходження, готують заново всі реактиви, проводять державну повірку приладів
і повторюють дослід з чотирма паралельними визначеннями. У цьому випадку, за
наявності розходження більше, ніж вказаних вище значень, виконання такої
роботи доручають оператору більш високої кваліфікації. 9. Визначення
кислотності молока кип’ятильною пробою Суть методу.
Використовують для визначення свіжості молока для вирішення питання
можливості або неможливості його пастеризації. Методика
визначення. У склянці прокип’ятити 10−15 см3 молока. Оцінка результату.
Якщо молоко згорнулося, – воно має підвищену кислотність (більше 25°Т), або
до свіже-видоєного молока додане кисле, хоч показник кислотності такого
молока може бути в нормі. 9.8. Визначення термостійкості молока і вершків за
алкогольною пробою згідно з ДСТУ 5073 Суть методу. Метод
ґрунтується на здатності етилового спирту (визначення концентрації) повністю
чи частково денатурувати білки молока або вершків, порушуючи стійкість
колоїдної системи. Примітка. Цей
метод є опосередкованим, оскільки дія високої температури аналогічна дії
етилового спирту на стійкість колоїдної системи молока чи вершків. Готування до
випробування: відібрану пробу молока в кількості (5–6) см3 доводять до температури (20±2) °С підігріванням (за
потреби – охолодженням) на водяній бані. Пробу вершків підігрівають на водяні
бані до температури (43±2) °С перемішують, виймають із водяної бані й
охолоджують до температури (20±2) °С. Готування водного
розчину етилового спирту. Термостійкість молока та вершків визначають за
допомогою п’яти робочих розчинів етилового спирту з концентрацією (об’ємною
часткою) спирту – 68 %, 70, 72, 75 і 80 %. Температура розчину етилового
спирту та води під час готування робочих розчинів етилового спирту –
(20,0±0,1) °С. 1 дм3 робочого розчину готують у мірному циліндрі, де змішують
первинний розчин етилового спирту певної концентрації (об’ємної частки) з
водою. Потрібні для
змішування об’єми первинного розчину етилового спирту та води, залежно від
концентрації (об’ємної частки) первинного розчину етилового спирту та
потрібної об’ємної концентрації робочого розчину етилового спирту, наведено в
таблиці 75. Таблиця 75 Об’єми первинного розчину етилового спирту та води,
потрібні для приготування 1 дм3 робочого розчину певної концентрації (об’ємної частки)
Робочий розчин
етилового спирту витримують у водяній бані за температури (20,0±0,1) °С упродовж
30 хв. Ареометри загального призначення визначають густину приготовленого
робочого розчину етилового спирту або ареометром для спирту – об’ємну частину
спирту в цьому розчині. Залежність між густиною (кг/м3) та об’ємною частиною
етилового спирту (%) у робочих розчинах за температури (20,0±0,1) °С наведено
в таблиці 76. Таблиця 76 Залежність густини від об’ємної частки робочих розчинів
етилового спирту за температури (20,0±0,1) °С
Густина робочого
розчину етилового спирту не повинна відрізнятися від наведених величин
більше, ніж на половину ціни поділки шкали ареометра загального призначення. Об’ємна частка
спирту в робочому розчині, визначена ареометром для спирту, не повинна
відрізнятися від наведених величин більше, ніж 0,25 %. Методика
дослідження. У дві сухі чисті чашки Петрі піпеткою вносять по 2см3 проби
молока або вершків, підготовленої, як вказано вище. У кожну із цих чашок
Петрі додають спиртовий розчин, в якому об’ємна частка етилового спирту
становить 72 %, та ретельно перемішують суміш коловими рухами. Проби
відстоюють упродовж 2 хв, та спостерігають за змінами консистенції. Якщо під час
проведення випробування молока або вершків із робочим розчином спирту, у
якому об’ємна частка етилового спирту становить 72 %, на дні чашки Петрі не
з’являються пластівці (тобто стійкість колоїдної системи молока або вершків
не порушується), проводять випробовування з робочим розчином спирту з більш
високою концентрацією, відмічаючи наявність пластівців на дні чашки Петрі. Якщо під час
проведення випробування молока або вершків із робочим розчином спирту, в
якому об’ємна частка етилового спирту становить 72 %, на дні чашки Петрі
з’являються пластівці (тобто стійкість колоїдної системи молока або вершків
порушується), проводять випробовування з робочим розчином спирту з більш
низькою концентрацією, відмічаючи наявність пластівців на дні чашки Петрі. Приклад 1. Якщо у
разі взаємодії проби молока або вершків із робочим розчином етилового спирту
певної концентрації (об’ємної частки) спирту, на дні чашки Петрі не з’явилися
пластівці, вважають, що проба є термостійкою. Приклад 2. Якщо у
разі взаємодії проби молока або вершків із робочим розчином етилового спирту
певної концентрації (об’ємної частки) спирту, на дні чашки Петрі з’явилися
пластівці, вважають, що проба є нетермостійкою. Опрацювання
результатів. Групу термостійкості молока або вершків визначають за
результатами дослідження тієї проби молока або вершків, яка у разі взаємодії
з більш концентрованим розчином етилового спирту не змінила свою консистенцію
(пластівці на дні чашки Петрі не з’явилися), тобто стійкість колоїдної
системи молока або вершків не була порушена. Групу
термостійкості молока або вершків визначають відповідно до вимог таблиці 77. Таблиця 77 Визначення групи термостійкості молока або вершків залежно від
концентрації (об’ємної частки) робочого розчину етилового спирту
Якщо обидві
паралельно досліджувані проби витримали випробування певною концентрацією
робочого розчину етилового спирту, молоко або вершки відносять до відповідної
групи термостійкості. Приклад. Якщо у
разі взаємодії проби молока або вершків із робочим розчином етилового спирту
з концентрацією (об’ємною часткою) спирту, що становить 72 %, на дні чашки
Петрі не з’являються пластівці, а з робочим розчином етилового спирту з
концентрацією (об’ємною часткою) спирту, що становить 75 %, на дні чашки
Петрі вони є, – молоко або вершки належать до III групи термостійкості. Якщо лише одна з
паралельних досліджуваних проб витримала випробування з робочим розчином
етилового спирту певної концентрації, а інша – ні, – молоко або вершки
належать до нижчої групи термостійкості. Приклад. Якщо у
разі взаємодії проби молока або вершків із робочим розчином етилового спирту
з концентрацією (об’ємною часткою) спирту, що становить 72 %, на дні чашки
Петрі не з’являються пластівці, а другої – з’являються, – молоко або вершки
належать до IV групи
термостійкості. Визначення
термостійкості молока і вершків хлоркальцієвою пробою Техніка
визначення. У суху пробірку відміряють 10 см3 молока (вершків) та із бюретки
додають 0,5 см3 розчину хлористого кальцію (CaCl2) з масовою концентрацією 1 %.. Ретельно
перемішують уміст пробірки і занурюють у киплячу водяну баню на 4 хв. Потім
пробірку виймають, охолоджують і спостерігають за утворенням пластівців
білку. Оцінка результату.
Виявлені пластівці (коагуляція білка) свідчать про те, що молоко (вершки) не
є термостійкими. Визначення термостійкості молока і вершків
пробою кип’ятіння Суть методу. З
наростанням кислотності молока, його властивості також змінюються. Свіже
молоко не зсідається під час кип’ятіння; молоко з підвищеною кислотністю не
витримує кип’ятіння – зсідається. Часто свіжість молока визначають
кип’ятінням невеликої його порції в пробірці. Ця проба називається
кип’ятильною. Якщо молоко під час кип’ятіння зсілося – кислотність такого
молока вища 25 °Т. Проба кип’ятінням
необхідна для виявлення свіжості молока і показує можливість його подальшої
пастеризації. Недоліком проби кип’ятінням
є те, що вона вказує кислотність, за якої молоко є, безумовно, несвіже і не
придатне до споживання в такому вигляді та для переробки на молочні продукти. Проте, проба
кип’ятінням допомагає відрізняти дійсно свіже молоко від змішаного, в якому є
частина молока з підвищеною кислотністю. Наприклад, в суміші молока з
кислотністю 26 °Т і 17 °Т кип’ятильна проба позитивна (таке молоко
зсідається), в той час як його титрована кислотність є не вищою, ніж 22 °Т. 9.9. Визначення масової частки жиру у молоці 1. Кислотний метод
визначення масової частки жиру у молоці Для визначення
жиру у молоці необхідно виділити його у чистому вигляді, тобто вивільнити від
білкових оболонок. Як розчинники білків, застосовують спільні розчини кислот
чи лугів. Стандартним методом визначення вмісту жиру в молоці є кислотний
згідно з ГОСТ 5867. Суть методу. Цей
метод ґрунтується на вивільненні та виділенні жиру із жирових кульок
досліджуваної проби молока під дією концентрованої сірчаної кислоти та
ізоамілового спирту з наступним центрифугуванням і визначенням його кількості
в градуйованій частині бутирометру. Сірчана кислота,
внесена в бутирометр, не лише руйнує білкові оболонки жирових кульок, але й
діє на основний білок молока – казеїнат кальцію, від якого спочатку виділяється
кальцій з утворенням нерозчинного казеїну і сульфату кальцію, пізніше –
пластівці казеїну розчиняються в надлишку кислоти. Ізоаміловий спирт,
а також утворений за наявності кислоти його сірчаний ефір, знижують
поверхневий натяг на межі поділу жиру та плазми молока і сприяють виділенню
жиру. Підігрівання і
наступне центрифугування вмісту бутирометру призводить до повного виділення
жиру, кількість якого визначають за шкалою бутирометру. Прилади і
реактиви: жироміри для молока з гумовими корками, штатив для жиромірів,
центрифуга лабораторна, піпетки на 10,77 см3, автоматичні піпетки на 10 і 1
см3, водяна баня, термометр на 100 °С, рушники, ганчірки, якісна сірчана
кислота (густиною 1,81–1,82). Визначення якості
і густини сірчаної кислоти. Сірчана кислота,
що застосовується для визначення жиру в молоці, повинна бути прозорою і не
мати домішок. Допускається слабке забарвлення її в буруватий колір. Для
перевірки її якості в жиромір налити 11 см3 досліджуваної кислоти і 11 см3
води. Жиромір закрити корком,
струсити вміст і центрифугувати 5 хв за 1000 об/хв. Потім витримати жиромір 5 хв у воді за (65±2) °С
і після цього повторити центрифугування. Якщо на поверхні суміші у вузькій
частині жироміра не виділиться жироподібний шар, кислота придатна для роботи. Густина сірчаної
кислоти визначається ареометром, що має шкалу з поділками 1,40–1,85. У разі
відсутності ареометра, густину кислоти можна визначити ваговим способом – на
технічній вазі відважують з точністю до
де а – маса чистої сухої колби; б – маса колби з водою; в – маса колби з сірчаною кислотою; Д – густина кислоти за 20 о С; 0,99823 – постійний коефіцієнт. Сірчану кислоту, що надходить в лабораторії
молокопереробних пунктів та молокоприймальних пунктів, розводять за формулою:
де В – кількість води (л); К – кількість кислоти, яку розбавляють (л); Д1 – густина наявної кислоти (визначають ареометром); Д2 – потрібна густина кислоти. Визначення якості
і густини ізоамілового спирту У ізоаміловому
спирті не повинно бути сторонніх домішок. Для перевірки його якості, в
жиромір наливають 10 см3 сірчаної кислоти густиною 1,81–1,82; 10,77 см3 води
і 1 см3 ізоамілового спирту, який перевіряють. Жиромір закривають гумовим
корком, добре струшують і залишають у штативі на 24 год для відстоювання. Якщо
на поверхні рідини в жиромірі не виділиться масляний шар, спирт придатний для
аналізу. Можна
використовувати й інший спосіб. У двох жиромірах визначають уміст жиру в
молоці з явно придатним спиртом, а у двох інших жиромірах – з застосуванням
перевіреного спирту. Якщо одержані результати у всіх жиромірах будуть
збігатися, спирт придатний для аналізу. Різниця допускається в межах ±0,05
поділки шкали. Техніка визначення
масової частки жиру в молоці (рис. 74, 75). 1. Нумерують жироміри.
Для цього простим олівцем наносять номер на зашліфований кружечок, розміщений
у верхній частині жироміра. 2. У штатив
установлюють необхідну кількість пронумерованих жиромірів. У кожний жиромір
відмірюють піпеткою-автоматом 1° см3 сірчаної кислоти, стараючись не змочити
шийки жироміра. 3. Відмірюють
піпеткою 10,77 см3 добре розмішаного молока. Обережно, по стінці, вливають
молоко у жиромір. Шар молока повинен розміститися над шаром кислоти, щоб не
сталося передчасного розігрівання. Кінець піпетки не повинен торкатися
сірчаної кислоти. Видувати молоко з піпетки не потрібно. 4. Відмірюють
піпеткою-автоматом 1 см3 ізоамілового спирту, намагаючись не змочити шийку
жироміра; змочування призводить згодом до вискакування корка. 5. Заповнені
жироміри закривають гумовими корками. Жиромір необхідно тримати в кулаку за
розширену частину (не за шкалу), загорнувши його в рушник або помістивши в
патрон центрифуги. Корок уводять гвинтоподібним рухом правої руки доти, поки
його кінець не торкнеться поверхні спирту. 6. Старанно
перемішують уміст жироміра до повного розчинення білків.
Послідовність унесення інгредієнтів у жиромір для визначення
масової частки жиру в молоці та молочних продуктах подана в таблиці 78. Таблиця 78 Послідовність внесення інгредієнтів у жиромір для
визначення масової частки жиру в молоці та молочних продуктах
Жир у вершковому
маслі визначають згідно з ГОСТ 5867 у вагових % за формулами: Х1(несолоне) =
100–(В+С); Х2(солоне) =
(В+С+С1), де В – масова частка
води, яка визначається згідно з ГОСТ 3636; С – уміст
знежирених речовин, %, визначається згідно з ГОСТ 3626, С1 – масова частка
кухонної солі у соленому маслі, визначається згідно з ГОСТ 3627. Для правильного
визначення об’єму виділеного жиру, закриті жироміри необхідно перевернути
корком вниз. Верхній рівень рідини повинен бути в межах 4–5 великих поділок
шкали жироміра. Якщо рівень рідини виявиться в нижній частині шкали, – в
жиромір необхідно додавати 1–2 см3 сірчаної кислоти. Якщо ж рідина заповнить
весь об’єм жироміра, в тому числі й горловину, виділений після
центрифугування жир розміститься вище градуйованої частини жироміра, тому
аналіз потрібно повторити. 7. Ставлять
жироміри у водяну баню (за температури 65...70°С) на 5 хв. 8. Жироміри
встановлюють симетрично у центрифугу і центрифугують упродовж 5 хв з
швидкістю 1000 об/хв. Якщо жиромірів непарна кількість, для рівноваги
встановлюють жиромір з водою. 9. Після
закінчення центрифугування ставлять жироміри на 5 хв у водяну баню за
температури 65...70 °С корками донизу. Оцінка результату.
Виймають жироміри з бані, витирають їх і відраховують показники жиру. Для
цього спочатку встановлюють нижню межу стовпчика жиру за найближчою цілою
поділкою шкали, що досягається легким закрученням або викручуванням корка.
Утримуючи стовпчик жиру корком, роблять відлік. За верхню межу стовпчика
беруть нижній край меніска. Великі поділки шкали з цифрою відповідають цілим,
малі – десятим часткам відсотків жиру.
Фактори, що
впливають на точність досліджень: 1. Недостатньо
перемішане молоко перед аналізом або під час взяття середньої проби. 2. Похибки в градуюванні
жироміра. 3. Наявність у
сірчаній кислоті жиророзчинних домішок, що переходять у жир. 4. Занадто слабка
або міцна сірчана кислота. 5. Неточно
виміряна кількість молока, кислоти або ізоамілового спирту. 6. Низька якість
ізоамілового спирту. 7. Погано
перемішаний уміст жироміра. 8. Низька
температура або недостатнє витримування жироміра у водяній бані до
центрифугування і після нього. Масову частку жиру
у молоці коров’ячому сирому можна визначати також ультразвуковим методом
згідно з ДСТУ 7057:2009. 9.10. Мікроскопія жирових кульок молока Суть методу. Сила
поверхневого натягу надають частинкам молочного жиру у молоці форми кульок. У
1 см3 цільного коров’ячого молока кількість кульок коливається від 2 до 6
млн. Діаметр жирових кульок становить в середньому 3–4 μ, коливаючись від 0,1 до 20 μ. Визначення
чинників, що впливають на величину жирових кульок, має практичне і теоретичне
значення. Під час сепарування молока, виготовлення масла і сиру, найбільші
втрати жиру спостерігаються у тих випадках, коли у вихідній сировині – молоці
переважають дрібні жирові кульки. На величину жирових кульок впливають:
порода тварин, період лактації, умови утримання, годівлі, індивідуальні
особливості та ін. Кількість, діаметр
та об’єм жирових кульок широко використовуються як показники, що
характеризують молоко, його технологічні особливості. У склянці змішати
5 см3 молока з 25 см3 води. Скляною паличкою перенести краплю розведеного
молока на предметне скло і покрити його покривним. Препарат поміщають на
столик мікроскопа і розглядають за збільшення у 300−500 разів.
Порівнюють величину жирових кульок у полі зору мікроскопа. З цією метою,
обертаючи окуляр, поміщають на мікрометричну лінійку ті кульки, величина яких
становить найбільший інтерес. Кількість жирових
кульок визначають у камері Горяєва. Площа камери складає 1,25 мм2. Сітка
камери розділена на 16 квадратиків. Підрахунок проводять за збільшення в 120
разів з об’єктивом 8 і окуляром 15. Препарат
розміщують під мікроскопом і підраховують кількість жирових кульок, що
знаходяться в 5-и квадратиках, розміщених за діагоналлю (у чотирьох кутах і в
центрі сітки). Площа кожного
квадратика становить 400 мм2, глибина камери –
Оскільки
підрахунок проводиться не в 16, а в п’яти квадратиках, – з п’яти отриманих
підрахунків виводять середню величину кількості кульок, що знаходяться в
одному квадраті (а), та перемножують цю величину на кількість усіх
квадратиків. Коли в об’ємі 16 квадратиків кількість кульок буде 16 × а,
а об’єм становитиме 0,004 мм3, – у 1 мм3 розведеного молока уміст жирових
кульок складатиме:
У разі розведення в 250 разів підсумкова формула для
розрахунку кількості жирових кульок (в) в 1 мм3 досліджуваного молока буде
становити:
Приклад: середня
кількість жирових кульок у 1 маленькому квадратику – 2,6. Кількість жирових
кульок у 1 мм3 молока: в = 2,6 ×
1000000 = 2600000. 9.11. Визначення масової частки білка у молоці Харчова цінність
молока і вихід таких молочних продуктів, як кисломолочний сир, сири сичужні,
залежить від умісту білка. Білки молока є найціннішими в харчовому
відношенні, їх кількість коливається в межах 2,8–4,0 %. Білки молока часто
поділяють на дві основні групи – казеїн і білки сироватки молока. Основна частина
білків молока представлена казеїном (75–85%). У молоці казеїн представлений у
вигляді казеїнату кальцію. Здатність казеїну легко коагулювати під дією
кислоти, сичужного ферменту (пепсину) та наростання іонів кальцію широко
використовується у виробництві кисломолочних продуктів, сичужних сирів та
бринзи. Іншу значну
частину білків складають сироваткові білки (15–20% усіх білків). Відділяють
сироваткові білки внаслідок кип’ятіння прозорих фільтратів, отриманих після
осадження казеїну. Для контролювання
масової частки білків у молоці існує кілька методів. Арбітражним є достатньо
трудомісткий хімічний метод К’єльдаля. На молокопереробних підприємствах, в
державних лабораторіях ветсанекспертизи, як правило, використовують методи
формольного титрування і рефрактометричний, у наукових дослідженнях –
колориметричний та ультразвуковий методи згідно з ДСТУ 7057:2009.
Використовують й інструментальні фізичні методи контролю масової частки
білків у молоці. 1. Визначення
вмісту загального білка методом формольного титрування згідно з ТУ 491212 Метод можна
використовувати для контролю масової частки білка в не консервованому молоці
кислотністю не більше 22 °Т. Суть методу. Метод
формольного титрування базується на реакції лужних аміногруп білка з
формаліном, унаслідок якої вивільняються карбоксильні кислі групи білка,
підвищується титрована кислотність молока, за збільшенням якої й визначають
масову частку білка. Для визначення
вмісту формальдегіду, в технічному формаліні готують розчин натрію сульфіту: Розчин натрію
сульфіту в кількості 50 см3 нейтралізують розчином сірчаної кислоти з масовою
концентрацією 1 моль/дм3 до світло-рожевого забарвлення (за наявності
фенолфталеїну) і додають 3 см3 досліджуваного формаліну. Гідроксид натрію, що
утворився в результаті реакції, титрують розчином сірчаної кислоти з масовою
концентрацією 1 моль/дм3 до світло-рожевого забарвлення. Кількість розчину
сірчаної кислоти (см3), витраченої на титрування, вказує на кількість
формальдегіду, що міститься в 100 см3 формаліну (г/100см3). Для визначення
кількості білка в молоці, використовують формалін з умістом формальдегіду не
менше Нейтралізацію
формаліну, в якому утворився осад, приводять після фільтрування. Для приготування
еталону забарвлення, в хімічну склянку місткістю 150–200 см3 піпеткою
відмірюють 20 см3 молока і додають 0,5 см3 розчину сульфату кобальту з
масовою часткою 2,5 %. Еталон використовують впродовж робочої зміни. Техніка
визначення. 1. У хімічну склянку місткістю 150–200 см3 піпеткою відмірюють 20
см3 молока і додають 0,25 см3 розчину фенолфталеїну з масовою часткою 2 %. 2. Суміш
перемішують і титрують розчином гідроксиду натрію до появи світло-рожевого
забарвлення відповідно до забарвлення еталону. 3. У склянку
вносять 4 см3 нейтралізованого розчину формаліну з масовою часткою 40 %,
перемішують суміш, і через 1 хв удруге титрують до появи світло-рожевого
забарвлення, що відповідає забарвленню еталону (визначають на білому фоні). Оцінка результату.
Масова частка (%) загальної кількості білка в молоці дорівнює кількості
розчину гідроксиду натрію з масовою часткою 0,1 моль/дм3., витраченого на нейтралізацію за наявності
формаліну, помноженому на коефіцієнт 0,959. Уміст загальної
кількості білка в молоці можна визначити за показниками таблиці 79. Таблиця 79 Визначення вмісту білка в молоці за титрування проб із
формаліном
Фактори, що
впливають на точність аналізу: 1) неоднакова
інтенсивність забарвлення під час титрування; 2) якість і
точність внесеного формаліну. Використовують лише свіжо-приготований
формалін; 3) молоко з підвищеною
кислотністю дає завищені результати. 2. Виділення
казеїну кислотою, альбуміну і глобуліну – нагріванням Методика
дослідження. У колбу відміряють 100 см3 молока і 50 см3 дистильованої води. В
одержану суміш із бюретки краплями додають розчин оцтової кислоти з масовою
концентрацією 5 % до появи згустків казеїну. У подальшому осад
казеїну відфільтровують. У прозорому фільтрі залишаються розчинні азотисті
сполуки, в тому числі альбуміни і глобуліни. Відмірюють 5 см3
прозорого фільтрату, кількісно переносять у пробірку і кип’ятять.
Спостерігають появу каламуті, а далі – коагуляцію альбуміну і глобуліну.
Наявність цих білків свідчить про відсутність пастеризації молока. У бюретці
відмічають рівень гідроксиду натрію і вміст колби знову титрують до світло-рожевого
забарвлення. Оцінка результату.
Для встановлення масової частки загального білка, кількість розчину
гідроксиду натрію з масовою концентрацією 0,1 моль/дм3, витраченого на
титрування після додавання формаліну, помножити на коефіцієнт 1,94, а для
визначення масової частки казеїну – на коефіцієнт 1,51. 3. Визначення
вмісту казеїну в молоці (за методом Маттіопуло) Суть методу
ґрунтується на встановленні кількості децинормального розчину лугу, витраченого
на титрування казеїну. Знаючи, що 1 см3 децинормального лугу еквівалентний Техніка
визначення. У дві колби ємністю 200–250 см3 відміряють по 20 см3 з однієї досліджуваної проби молока і додають по 80
см3 дистильованої води. У одну з колб з
бюретки краплями, за постійного помішування, доливають 0,04 н розчин H2SO4 з масовою концентрацією 0,04 моль/дм3 (0,04 н) (приблизно 23–28 см3) до появи добре помітних
пластівців казеїну. У другу колбу з
бюретки доливають таку ж кількість сірчаної кислоти, що й у першу. Уміст першої колби
відфільтровують у мірну колбу ємністю 100 см3. У фільтрат перейдуть усі
складники молока, крім казеїну. Суміш з казеїном у
другій колбі титрують розчином NаОН з масовою концентрацією 0,1 моль/дм3 за наявності
індикатору – спиртового розчину фенолфталеїну (2−3 краплі), до
світло-рожевого забарвлення. 100 см3 прозорого
фільтрату переливають у конічну колбу ємністю 200−250 см3 і титрують
розчином NаОН масовою
концентрацією 0,1 моль/дм3 з індикатором фенолфталеїном до
світло-рожевого забарвлення. Вираховують уміст
казеїну в молоці. Приклад: у першій
колбі міститься 20 см3 молока + 80 см3 води + 24 см3 розчину H2SO4 (0,04 н), разом – 124 см3 суміші; у другій колбі –
теж 124 см3 суміші. На нейтралізацію суміші у другій колбі (з казеїном)
витрачено 15 см3 розчину NаОН (0,1 н). На нейтралізацію 100 см3 фільтрату з
першої колби (без казеїну) витрачено 8,3 см3 розчину NаОН (0,1 н). На 124 см3 фільтрату без казеїну
використається: 100 – 8,3 124 – х
Таким чином, на
нейтралізацію казеїну, що міститься у 20 см3 молока, витрачено 15 – 10,29 =
4,71 см3 розчину NаОН (0,1 н). Оскільки 1 см3
розчину NаОН (0,1 н)
еквівалентний Оцінка результату.
Для розрахунку відсотків казеїну у молоці необхідно кількість казеїну в
грамах розділити на показник густини досліджуваного молока (чи на середню
густину – 1,030). У даному випадку масова частка казеїну складатиме 2,65:
1,030 = 2,57 %. 4. Визначення
масової частки білка в молоці за допомогою рефрактометра ІРФ–464 Цей прилад є
візуальним і призначеним для вимірювання показників заломлення розсіювальних
рідких середовищ. Метод ґрунтується
на виявленні різниці в показниках заломлення променя світла, що проходить через
молоко і безбілкову сироватку за однакових умов вимірювання. На аналізаторі
можна досліджувати молоко коров’яче (сире, збірне або від окремих тварин,
пастеризоване, збірне) з кислотністю не вище 28 °Т за температури від 10 до
35 °С і вологості 80 %. Підготовка приладу
до роботи. Перед початком роботи необхідно перевірити початок підрахунку за
допомогою прикладеної контрольної призми або дистильованої води. Для
перевірки за контрольною призмою необхідно відокремити освітлювальну призму й
старанно протерти поверхні вимірювальної та контрольної призм, накласти і
притерти контрольну призму на вимірювальну, на поверхню контрольної призми
нанести краплю імерсійної рідини, яка повинна рівномірно розподілятися на
поверхні, але не виступати за її межі. Спостерігаючи в
окуляр, необхідно встановити різке зображення межі світлотіні, а поворотом
кільця ліквідувати його забарвлення. Зафіксувати показання приладу за шкалою
показників заломлення nD. вимірювання потрібно проводити 5 разів, потім
провести повторне накладання і притирання контрольної призми і зняти
показники nD три рази. Якщо
показник виявиться в межах перших п’яти, – притирання вважають правильним. Для перевірки
початку підрахунку за дистильованою водою, необхідно 1–2 краплі нанести на
чисту поверхню вимірювальної призми, опустити освітлювальну призму,
п’ятикратно зняти відлік nD та визначити середнє арифметичне. Якщо середнє
арифметичне відрізняється більше, ніж на 1,5±10-4 від значення nD, нанесеному на контрольній призмі, а для дистильованої
води – значення nD, наведеного в таблиці, – рефрактометр необхідно
відрегулювати. Для цього, повертаючи викруткою гвинт, необхідно встановити за
шкалою nD відповідно nDеф, нанесеному на контрольній призмі для дистильованої
води відповідно nD, наведеному в таблиці 80. Спочатку
визначають показник променя світла, що проходить через безбілкову сироватку.
Для отримання безбілкової сироватки, у флакон вливають 5 см3 молока і додають
5 крапель розчину хлористого кальцію з масовою часткою 4 %. Флакон закривають
корком, суміш ретельно перемішують і переносять у водяну баню, де рівень води
перевищує рівень молока у флаконах. Флакон кип’ятять 10 хв, потім
охолоджують, після чого струшують, щоб згусток зруйнувався і змішався з
конденсатом. Піпеткою з ватним
тампоном необхідно відсмоктати сироватку і, знявши тампон, нанести 1–2 краплі
на вимірювальну призму та плавно закрити її освітлювальною. Спостерігаючи в
окуляр, необхідно встановити різке зображення межі світлотіні і через 0,5–1
хв записати показники за шкалою «Білок». Вимірювання необхідно повторити 3–4
рази і визначити середнє значення Бс. Видаливши
сироватку з обох призм, їх старанно промивають водою і витирають насухо
ватою. Потім на вимірювальну призму наносять 1–2 краплі досліджуваного молока
і проводять вимірювання показника за шкалою «Білок» у такому ж порядку, як на
сироватці. Вимірювання повторюють 4–5 разів і визначають середнє арифметичне Бм. Уміст білків у
молоці визначають за формулою: Б мол% = Бм – Бс. Загальний білок
(білок + небілкові азотисті речовини) визначають за формулою: Бз% = (Бм – Бс)
× 1,0855. Уміст казеїну у
молоці визначають за формулою: К% = (Бм – Бкс)
× 1,1012, де Бкс – показник за
шкалою «Білок» для сироватки без казеїну, для одержання якої до 5 см3 молока
у флакон додають 10 крапель розчину оцтової кислоти з масовою часткою 10 %. Уміст сироваткових
білків визначають за формулою: СБ% = Бм – К Таблиця 80 Показники заломлення променя, що проходить через
дистильовану воду за температури 15...35 °С
Фактори, що
впливають на точність аналізу: брудні призми, недостатнє освітлення приладу,
неповне осадження білків під час одержання сироватки, нечітке встановлення
межі на світлотіні. 5. Визначення масової
частки білка в молоці колориметричним методом згідно з ГОСТ 25179 Метод базується на
здатності білків молока за величини рН, нижче ізоелектричної точки,
зв’язувати кислі барвники, утворюючи з ними нерозчинний комплекс. У
результаті оптична густина розчину зменшується пропорційно кількості білка.
Після видалення нерозчинного комплексу, вимірюють оптичну густину розчину
залишкового барвника і за градуйованим графіком визначають масову частку
білка в молоці. Для приготування
буферного розчину зважують Водний розчин
барвника готують так: зважують Для приготування
робочого розчину кислотного синьо-чорного барвника, в мірну колбу на 2000 см3
за допомогою скляної лійки з паперовим фільтром, переносять водний розчин
барвника і буферний розчин. Паперовий фільтр промивають дистильованою водою
до повного видалення барвника. Додають до розчину 0,2 см3 допоміжної речовини
ОП-7. Доводять об’єм розчином дистильованою водою до мітки і старанно
перемішують. Перед використанням робочий розчин барвника витримують упродовж
12 год у холодильнику. Готуючи робочий
розчин барвника, необхідно перевіряти правильність його приготування. Для
цього визначають рН розчину, який повинен дорівнювати 2,4. Якщо рН не
відповідає цьому значенню, додають сірчану кислоту або гідроксид натрію. Визначають
концентрацію барвника в робочому розчині. Для цього відбирають піпеткою 2 см3
робочого розчину барвника і переносять у мірну колбу на 200 см3. Об’єм у
колбі доводять до мітки дистильованою водою і старанно перемішують. На фотоелектроколориметрі
або спектрофотометрі в кюветі з довжиною робочої грані V=V1 [( D1 / D2 )-1], де V – об’єм буферного розчину для розведення, см3 ; V1 – об’єм початкового робочого розчину барвника, см3 ; D1 – необхідна оптична густина розведеного робочого розчину барвника, що
дорівнює 0,82; D2 – визначена оптична густина розведеного робочого розчину барвника. Якщо оптична
густина розведеного розчину барвника менша 0,82, готують новий робочий
розчин, відповідно збільшивши наважку барвника кислотного синьо-чорного. Робочий розчин
барвника зберігають у холодильнику в банці з темного скла не більше 12 міс. Для побудови
градуйованого графіка в 10 пробах молока з умістом білка 2,5–4,5 %, за
методом К’єльдаля визначають масову частку білка. У цих же пробах, способом,
описаним нижче, визначають оптичну густину розчину. За методом
найменших квадратів обчислюють значення а і в для рівня регресії D = а – в, що виражає залежність оптичної густини D від масової частки білка в молоці. Градуйований
графік будують на підставі одержаного рівняння регресії за двома значеннями
масової частки білка – 2,5 і 4,5 %. Для цього, на осі абсцис відкладають
значення масової частки білка, осі ординат – відповідне їм значення оптичних
густин, обчислених за рівнянням регресії. Періодично
(використання нової партії барвника, зміна пори року та ін.) перевіряють
правильність побудови градуйованого графіка за 2–3 пробами молока з визначенням умісту білка. Якщо
показники масової частки білка, одержані за градуйованим графіком,
відрізняються від показників, одержаних методом К’єльдаля, більше, ніж на
0,05 %, будують новий градуйований графік. Для аналізу
використовують свіжовидоєне молоко або консервоване тетраборитом натрієм
10-водним – У скляну пробірку
відміряють 1 см3 молока, 20 см3 робочого розчину барвника і закривають
гумовою пробкою. Рідину перемішують перевертанням пробірки впродовж 0,5 хв,
не допускаючи струшування. Для визначення утвореного нерозчинного комплексу
білка з барвником, пробірку центрифугують упродовж 10 хв за 1500 об/хв або 20
хв за 100 об/хв. Піпеткою
відбирають 2 см3 рідини над осадом і переносять у мірну колбу об’ємом 200
см3. Об’єм до мітки доводять дистильованою водою і старанно перемішують. На
фотоелектроколориметрі або спектрофотометрі в кюветі з довжиною робочої грані
Масову частку
білка в молоці (%) визначають за градуйованим графіком за одержаною середньою
величиною оптичної густини. За кінцевий результат приймають середнє
арифметичне двох паралельних визначень, розходження між якими має бути не
більшим, ніж 0,05 % білка. 6. Визначення
масової частки білка в молоці розрахунковим методом Знаючи досить
стійкі співвідношення основних компонентів молока, можна вирахувати і масову
частку окремих складників сухої речовини (СР): Масова частка
білка (%): Б=1,0+(0,65×Ж),
де Б – масова частка
білка, %; Ж – масова частка
жиру в молоці; 1,0 і 0,65 –
константи. Приклад. Масова
частка жиру молока 3,8 %; густина – 1,027 г/см3. Розрахуємо масову частку
білка молока: Б=
1,0+(0,65+3,8)=3,47 %. 9.12. Визначення масової частки молочного цукру У сухій речовині
міститься значна кількість вуглеводів. Центральне місце серед вуглеводів
молока відводиться лактозі. Вона складає близько 40 % усіх вуглеводів молока і міститься у молоці всіх
ссавців. Уміст молочного
цукру у коров’ячому молоці складає 4,5−5,2 %. За харчовою
цінністю молочний цукор не відрізняється від бурякового і майже повністю
засвоюється організмом (близько 98%). Лактоза бере активну участь у
енергетичному забезпеченні організму, нормалізації мікрофлори кишечнику.
Останнє має важливе значення для молодняку тварин. Молочний цукор є
вихідним матеріалом для процесів бродіння, що є основою виробництва всіх
кисломолочних продуктів і сирів. Під дією мікроорганізмів і їх ферментів, що
вносяться в молоко як закваски, процес бродіння молочного цукру необхідно
спрямувати у напрямку: а) молочнокислого
бродіння – для виробництва кисломолочних продуктів, сирів і кисло-вершкового
масла; б)
пропіоновокислого бродіння – для дозрівання твердих сичужних сирів; в) спиртового
бродіння з молочнокислим – для виробництва кумису, кефіру, айрану. Лактоза
значно впливає на властивості молочних консервів у процесі їх зберігання,
зміну кольору і смаку молочних продуктів під час їх термообробки. Так,
короткотривала пастеризація молока навіть за температури 90...95 °С не
викликає зміни вмісту молочного цукру. Нагрівання молока до температури 100 °С
призводить до появи коричневого забарвлення внаслідок утворення меланоїдинів
(результат реакції між амінокислотами білків і карбонільною групою молочного
цукру). За нагрівання лактози до температури 110...130 °С, вона втрачає
кристалізаційну воду, а під час подальшого нагрівання до температури 185°С –
відбувається її карамелізація. Молочний цукор
відіграє важливу роль у технологічних властивостях молока та інших молочних
продуктів. Форма і величина кристалів визначає піщанисту консистенцію
згущеного та гігроскопічність сухого молока. У вигляді готового
продукту лактозу, отриману з сироватки, широко використовують у
фармакологічній промисловості та харчовій галузі. 1. Визначення
масової частки лактози в молоці Метод ґрунтується на
визначенні кількості осаду закису міді, що виділяється під час кип’ятіння
молочної сироватки з фелінговим розчином. Реактиви: розчин CuSO4 ( Техніка
визначення. Приготування молочної
сироватки. У мірну колбу на
500 см3 відміряють 20 см3 молока і 400 см3 дистильованої води. Для осадження
білків і солей послідовно доливають 10 см3 розчину CuSO4 і 6−7 см3 розчину NаОН. Колбу щільно закривають, перемішують уміст і
залишають у спокої на 3 хв. Доливають до мітки
дистильованою водою, відфільтровують осад, що утворився, до отримання прозорого
фільтрату (блакитнуватого відтінку). Одержання осаду
закису міді. До 500 см3 фільтрату, перелитого у конічну колбу на 300 см3,
додають по 25 см3 фелінгових розчинів 1 і 2 та кип’ятять упродовж 6 хв. Дають осаду
осісти, рідину зливають на фільтр (бажано з азбесту) і відсмоктують
водоструменевим насосом. Зливають блакитний
розчин на фільтр, а осад (Cu2O) промивають гарячою водою 2−4 рази (40−50 см3). Зливають
промивну воду на фільтр. Промивши осад, лійку з фільтром уставляють у чисту
колбу. Розрахунок титру
розчину KMnO4 (за міддю). Титр
розчину розраховують за щавлевокислим амонієм унаслідок реакції окиснення
марганцевокислим калієм розчинів щавлевокислого амонію і сірчанокислого
закису заліза. Молекулярна маса щавлевокислого амонію складає 142,1, а міді –
63,6. Кількісне
співвідношення розраховується за пропорцією: х г (NH4)2C2O4 – у г Cu
де х – наважка щавлевокислого амонію (в г),
взята для визначення титру KMnO4 ( Під час визначення
титру розчину: відважують у колбу Приклад: наважка (NH4)2C2O4 = 0,24, що відповідає 0,24 × 0,8951 = 0,21 г міді. На титрування витрачено 19 см3 розчину KMnO4 (0,5 н). Титр KMnO4 за міддю = 0,21/19 + 2.
Рефрактометричний метод визначення вмісту лактози в молоці Суть методу. Метод
базується на зміні показника заломлення променя, що проходить через розчин,
залежно від вмісту в розчині молочного цукру. Перед
дослідженням, з молока виділяють сироватку осадженням білків розчином
хлористого кальцію з масовою часткою 4 %. У сироватці визначають показник
заломлення. Визначення проводять за постійної температури. Техніка
визначення.
1. Перед початком
роботи встановлюють рефрактометр на стійкій підставці і з’єднують гумовою
трубкою з посудиною, наповненою водою. 2. Воду
пропускають через рефрактометр з метою підтримання постійної температури.
Визначення проводять за температури 20 °С (рис. 77). 3. Скляною
трубочкою, закритою в нижньому кінці ватним тампоном, відбирають невелику
кількість сироватки. 4. Краплю сироватки
наносять на нижню призму рефрактометра і закривають її верхньою призмою. 5. За допомогою
дзеркала направляють промінь світла на верхню призму. 6. Спостереження
проводять через окуляр. Обертанням ручки встановлюють чіткість контурів. 7. Пересуванням окуляра
досягають збігу меж світла і тіні (з показником) у полі зору. Оцінка результату.
За лівою шкалою рефрактометра проводять відлік, що показує коефіцієнт
заломлення. За таблицею 81
знаходять процентний уміст лактози. Таблиця 81 Уміст молочного цукру (в %), що відповідає коефіцієнту
заломлення
3. Розрахунковий метод визначення вмісту лактози в
молоці Масова частка лактози в молоці корови становить 4,5–5,2
%. Знаючи доволі стійкі співвідношення основних компонентів молока, можна
вирахувати і масову частку окремих складників сухої речовини – молочного
цукру (лактози): а)
Л = (Ж + А)×0,135, де
б)
де
Приклад. Масова частка жиру молока становить 3,8 %;
густина – 27 °А; СЗМЗ – 8,27 %. Розрахуємо масову частку лактози в молоці: Л = (3,8 % + 27 °А)×0,135 = 4,16 %,
Масову частку
лактози також можна визначати ультразвуковим методом згідно з ДСТУ 7057:2009. 9.13. Визначення масових часток сухої речовини і води у
молоці Молоко –
біологічна рідина складної хімічної будови. До складу молока входять вода та
сухі речовини. Сухі речовини (сухий залишок) являють собою загальну масу
речовин, отриманих після висушування наважки молока за температури 102...105
°С. У середньому, в коров’ячому молоці міститься 12,5 % сухої речовини.
Проте, її кількість може змінюватися залежно від лактації, віку тварини,
рівня годівлі та багатьох інших чинників. До сухих речовин молока відносять
жир, білок, молочний цукор, мінеральні речовини, вітаміни, ферменти. За
мінусом із загальної кількості сухої речовини жиру отримують сухий знежирений
молочний залишок (СЗМЗ), уміст якого коливається в межах від 6,6 до 10,3 % (у
середньому – 8,7%). Показники сухої
речовини та сухого знежиреного залишку зумовлюють харчову цінність молока,
тому їх завжди враховують під час виробництва таких молочних продуктів, як:
сир, масло, кисломолочний сир, молочні консерви та морозиво. Визначення вмісту
сухих речовин проводять розрахунковим методом та більш точним – шляхом
висушування. 1. Визначення
масових часток води і сухої речовини у молоці шляхом висушування Визначення масової
частки сухої речовини, води і сухого знежиреного молочного залишку (СЗМЗ) в
молоці проводять розрахунковим методом та більш точним – висушуванням
(аналітичний метод). Масову частку СЗМЗ додатково можна визначати
рефрактометричним методом – на рефрактометрах АМ-2 і ІРФ-464, а також за
допомогою приладів «Лактан 1-4», «Клевер-1М», «Екомілк» тощо. Масову частку
сухої речовини можна визначати ультразвуковим методом згідно з ДСТУ
7057:2009. У середньому
масова частка сухих речовин в коров’ячому молоці складає 11−12 %. А. Аналітичний
метод визначення масової частки води і сухої речовини молока (висушуванням)
Реактиви і
прилади: вага лабораторна, шафа сушильна електрична (рис. 78), ексикатор,
бюкса скляна, піпетки 10 см3, водяна баня. Техніка визначення (рис. 79): 1. Скляну бюксу з
20−40 г добре промитого, прожареного піску і скляну паличку поміщають у
сушильну шафу та витримують за температури (102±2) °С упродовж 30−40
хв. Потім бюксу виймають з сушильної шафи, закривають кришкою, охолоджують в
ексикаторі 40 хв і зважують з точністю до 2. Уміст добре
перемішують паличкою. Потім відкриту бюксу і кришку поміщають у сушильну шафу
з температурою (102±2) °С. Через 2 год бюксу виймають із сушильної шафи,
закривають кришкою, охолоджують в ексикаторі 40 хв і зважують.
Оцінка результату. Масову частку сухої речовини (СР)
визначають за формулою:
де m0 – маса бюкси з піском і скляною паличкою, г; m – маса бюкси з піском, скляною паличкою і молоком до
висушування, г; m1 – маса бюретки з піском, скляною паличкою і молоком
після висушування, г. Масову частку води в продуктах (В) у відсотках
вираховують за формулою: В = 100 – СР, де СР – масова частка сухої речовини, %. Приклад: m0 – маса бюкси з піском і скляною паличкою = m – маса бюкси з піском, скляною паличкою і молоком до
висушування = m1 – маса бюретки з піском, скляною паличкою і молоком
після висушування =
Масова частка води (В) становить: В = 100 – 12,04 =
87,96 %. Основний недолік
цього методу – тривалість проведення аналізу. Для більш швидкого визначення
можна зменшити об’єм проби молока до 3 см3, нанести її на марлеві кружки,
вкладені на дно бюкси і висушувати за більш високої температури – 105 °С.
Тоді перше висушування скорочується від 2 год до 60 хв, а друге – від 1 год до 20−30 хв.
Тривалість висушування молока і молочних продуктів зменшується до кількох
хвилин за використання інфрачервоного випромінювання, методу контактного
висушу-вання (вологомір ЕВЛАС-1, прилад Чижової, апарат сушильний АПС-1). Б. Розрахунковий
метод визначення сухої речовини (CP). Формули для розрахунків складені, залежно від
масової частки сухої речовини молока, густини і масової частки жиру. 1) Для визначення
масової частки сухої речовини молока використовують формулу:
Де
2) Масову частку СР у молоці корів можна розрахувати за
модифікованою формулою професора М.І. Книги:
Де
3)
СР = СЗМЗ +Ж, де
4) Золи: СЗМЗ – масова частка сухого знежиреного молочного
залишку,%; 8; 100 – константи.
Приклад: СЗМЗ –
масова частка сухого знежиреного молочного залишку = 8,46 %. Отже: 2. Визначення сухого знежиреного молочного залишку
(СЗМЗ) молока розрахунковим методом СЗМЗ коров’ячого молока – 6,6−10,3 % Масову частку сухого знежиреного молочного залишку
(СЗМЗ) у молочних продуктах визначають за наступними формулами: а)
СЗМЗ = CP−Ж, де
Приклад:
СЗМЗ
= 12,16−3,7=8,46 %. б)
Приклад:
У збірному молоці
середня величина сухої речовини (СР) становить 12,5 %, а СЗМЗ для збірного
молока – 8,5 %. в) визначення сухих
знежирених речовин молока (СЗРМ) у складі СЗМЗ:
Приклад:
9.14. Визначення показників якості молока за допомогою
аналізатора «Еkomilk»
1. Підготовка проб
молока до аналізу: – температура
молока – 10…30 ºС; – кислотність – не
більше 25 ºТ, для овечого молока – не більше 28 ºТ; – не можна використовувати
досліджену пробу повторно. 2. Підготовка
приладу (рис. 80) до роботи: – включити прилад,
прогріти його
впродовж 5 хв; на табло появиться
«WARM UP», а потім «EKOMILK». 3. Режим
дослідження: – натиснути один
раз на кнопку «MODE», на табло висвітиться «COWMILK»; – обрати режим
натискання кнопки. На табло появляється написи: «COWMILK» − дослідження молока корови; «CLEANING» − промивання в кінці робочого дня; «MOTOR CHOICE» − вибір основного режиму застосування; «CALIBRATION» − калібрування; «SYSTEM» − системний режим використовується лише
виробником; «SHEEP (BUFFALO, GOAT) MILK» − дослідження овечого (буйволячого, козинячого)
молока. – обрати «MOTOR CHOICE» кнопкою «ОК», підтвердити свій вибір за допомогою
значка «^», а потім натиснути «ON» (2 рази). На індикаторі з’являється «MOTOR TURNED». 4. Аналіз молока: Заповнити добре
вимитий стакан молока, поставити його на місце вимірювання. Натиснути кнопку «MODE» – на табло висвітлюється «COWMILK» (коров’яче молока), а потім «ОК» (підтвердити свій вибір).
Доки триває процес визначення, на екрані висвічується «WORKING» і вертикальні прямокутники (показують розвиток
процесу вимірювання). Посуд з молоком не
можна видаляти до кінця вимірювання. На табло
висвічується надпис: уміст жиру, СЗМЗ, густина, % фальсифікації водою,
коефіцієнт замерзання, білок. Промивання між
дослідженнями: – лише
дистильованою водою за температури 40…60 ºС; – натиснути кнопку
«MODE», за допомогою значків «^» обрати «CLEANING» (промивати), потім 2 рази натиснути «ОК» ; – після закінчення
промивання (на дисплеї з’являється повідомлення «CLEANING END») забруднена вода видаляється. всю процедуру
повторяють, доки вода не очиститься. Промивання в кінці
робочого дня: – здійснюють
відразу після промивання водою; – стакан
заповнюють розчином лужного мийного препарату «EkoDay» з масовою часткою 2 % за температури 25…40 ºС і
становлять на пластмасову стійку аналізатора; – натискають
кнопку «MODE» за допомогою
значка «^» чи «^» обрати «CLEANING» (промивання), потім натиснути «ОК» ; – за допомогою «^»
встановити 20 циклів промивання, після чого натиснути «ОК» ; – після закінчення
промивання (на дисплеї з’являється повідомлення «CLEANING END») забруднений миючий розчин виливають в раковину. Щоб видалити залишки
мийного розчину, необхідно повторити промивання з водою, доки вона не буде
абсолютно чистою. 9.15. Визначення вмісту вітамінів у молоці У молоці містяться
майже всі життєво необхідні вітаміни. Деякі з них містяться в молоці в
недостатніх кількостях. Для оцінювання якості молока важливе значення мають
каротин та вітамін С. Уміст інших вітамінів у молоці є також цікавим і
пізнавальним, особливо з огляду на його подальшу високотемпературну обробку,
що впливає, переважно, на їх збереженість. Каротин,
паралельно з вітаміном А, надає молоку та маслу жовтуватого забарвлення.
Вітамін А руйнується під час нагрівання вище 100 °С, тоді як уміст каротину
знижується вже під час пастеризації. У таких продуктах, як масло, сметана та
сири – вітамін А знаходиться у жировій фазі, як і вітамін D. Вітамін D належить до термостійких. Вітаміни групи В є стійкими
до обробки та переробки молока і містяться у молочних продуктах. Їх багато у
кисломолочних продуктах. Уміст вітаміну С у
молоці суттєво залежить від його подальшої теплової обробки і тривалості
зберігання. 1. Визначення
вмісту в молоці каротину колориметричним методом Суть методу.
Виділення каротину в чистому вигляді і порівняння інтенсивності забарвлення його
розчину зі стандартним розчином каротину (чи азобензолу). Жири, ефіри і
супутні каротину пігменти молока омилюють лугом, а ті каротиноїди, що не
омилюються, виділяють з молока петролейним ефіром. Відділення каротиноїдів
від каротину базується на адсорбції їх MgO. Приготування
стандартного розчину азобензолу. Техніка
дослідження. 1. У конічну колбу відміряють 50 см3 молока, додають 30 см3
водного розчину КОН з масовою концентрацією 25 % і нагрівають на водяній бані
до повного розчинення білків. 2. Колбу з умістом
охолоджують до 20 °С, додають 10 см3 розчину етилового спирту з масовою
концентрацією 96 %; уміст перемішують і переносять у ділильну лійку. 3. Доливають у
лійку 3 см3 петролейного ефіру (температура кипіння не вище, ніж 60°С),
розмішують і дають відстоятися. 4. Нижній,
водно-лужний, шар зливають у іншу ділильну лійку і ще раз екстрагують ефіром.
5. Ефірні витяжки
зливають в одну ділильну лійку, промивають декілька разів дистильованою
водою, доки вода не стане прозорою, після чого витяжки переносять у колбу і
висушують, додають 7−8 г прожареного Na2SO4, одночасно колбу нагрівають у нахиленому положенні на
водяній бані. 6. Висушений
залишок розчиняють у 5−10 см3 ефіру, пропускають через адсорбційну
колонку з MgO; фільтрат з
каротином колориметрують. Як стандартний
розчин, використовують азобензол, 1 см3 якого за забарвленням відповідає
0,00235 мг каротину. Оцінка результату.
За формулою розраховують уміст каротину (мг на
де К – уміст каротину
(мг/кг); h – висота стовпчика стандартного розчину (см); V – кількість розчину (см3 ); m – маса молока (г); h1 – висота стовпчика досліджуваного розчину (см); 2,35 – постійний
коефіцієнт. Приклад. Висота
стовпчика стандартного розчину
Фактори, що
впливають на точність досліджень: 1) повнота
омилення і перенесення вмісту колби у ділильну лійку; 2) якість і
чистота ефіру; 3) ретельність
екстрагування і промивання не омиленого залишку; 4) швидкість
колориметрування підготованої суміші. 2. Визначення
вмісту в молоці вітаміну С Суть методу
полягає у титруванні спеціально підготованого екстракту індикатором розчину
2,6-дихлорфеноліндофенолу з масовою концентрацією 0,001 моль/дм3 (0,001 н), 1
см3 якого відповідає 0,088 мг аскорбінової кислоти. Приготування
розчину 2,6-дихлорфеноліндофенолу з масовою концентрацією 0,001 моль/дм3
(0,001 н): 1. 2. Розчин
фільтрують і доводять у мірній колбі до 0,5 дм3. У темній накритій склянці
розчин можна зберігати до 7 діб. Перед кожним дослідженням перевіряють титр. 3. Титр
установлюють за 0,01 н розчином солі Мора з масовою концентрацією 0,01
моль/дм3 (0,01 н) ( Титрування KMnO4. До 10 см3 розчину щавлевої кислоти з масовою
концентрацією 0,01 моль/дм3 (0,01 н), додають 1 см3 концентрованої сірчаної
кислоти. Суміш нагрівають до 80 °С і титрують розчином KMnO4 з масовою
концентрацією 0,01 моль/дм3 (0,01 н), до слабо-рожевого забарвлення. Титрування солі
Мора. До 10 см3 розчину солі Мора додають 3 краплі концентрованої кислоти і
титрують розчином KMnO4 до появи стійкого слабо-рожевого забарвлення. Під час
титрування розчину 2,6-дихлорфеноліндофенолу масовою концентрацією 0,001
моль/дм3 (0,001 н), до 10 см3 2,6-дихлорфеноліндофенолу додають 2 см3
насиченого розчину натрію і титрують розчином солі Мора (з мікропіпетки) до
переходу синього забарвлення у солом’яно-жовте. Поправку (К) до
титру 2,6-дихлорфеноліндофенолу вираховують за формулою:
а – кількість
(см3) KMnO4, витраченого на титрування 10 см3 солі Мора; с – кількість
(см3) солі Мора, витраченої на титрування 2,6-дихлорфеноліндофенолу; б – кількість
(см3) KMnO4, витраченого на титрування 10 см3 розчину щавлевої
кислоти масовою концентрацією 0,01 моль/дм3 (0,01 н). Приклад: а = 8,0 см3; б = 8,1 см3; с = 1,34 см3
Техніка
дослідження. У конічну колбу на 50 см3 відмірюють піпеткою 5 см3 молока і 10 см3 дистильованої води, суміш
розмішують. У колбу на 50 см3
відмірюють 5 см3 суміші, 9 см3 дистильованої води і 1 см3 розчину
хлористоводневої кислоти (HCl) з масовою концентрацією 2 %, ретельно перемішують і
титрують з мікропіпетки розчином 2,6-дихлрфеноліндофенолу з масовою
концентрацією 0,001 моль/дм3 (0,001 н), (додаючи його краплями) до
слабо-рожевого забарвлення, що не зникає впродовж 30−60 с. Розраховують уміст
вітаміну С у молоці за формулою: С = а · К · 52,8,
де С – уміст вітаміну
С (мг/дм3); а – кількість
розчину 2,6-дихлорфеноліндофенолу з масовою концентрацією 0,001 моль/дм3 (0,001 н), (см3), витраченого на титрування
молока; К – поправка до
титру індикатора; 52,8 – постійний
коефіцієнт. Приклад. На титрування
фільтрату витрачено 0,4 см3 розчину 2,6-дихлорфеноліндофенолу з масовою
концентрацією 0,001 моль/дм3 (0,001 н), поправка на титр – 1,320. С =
0,4×1,320×52,8 = 27,9 мг/дм3. Фактори, що
впливають на точність досліджень: точність установлення поправки до розчину
2,6-дихлорфеноліндофенолу з масовою концентрацією 0,001 моль/дм3 (0,001 н), 3. Стандартний
спрощений метод визначення вмісту аскорбінової кислоти Техніка
дослідження. Молоко, у кількості 5 см3, розводять у три рази дистильованою
водою. У разі розведення молока – відмірюють піпеткою, а дистильовану воду
наливають з бюретки. У конічну колбу
ємністю 25−50 см3 уносять 1 см3 хлористоводневої кислоти з масовою
часткою 2 % і 5 см3 розведеного молока та доводять водою до 15 см3. Уміст колби титрують
з мікробюретки розчином дихлорфеноліндофенолу з масовою концентрацією 0,001
моль/дм3 (0,001 н), доливаючи його краплями до появи світло-рожевого
забарвлення, що зберігається 0,5−1 хв. Проводять 2
паралельних визначення з однієї порції розведеного молока. Молозиво розводять
у 3−6 разів. Уміст аскорбінової
кислоти вираховують за формулою:
v – кількість робочого розчину 2,6-дихлорфеноліндофенолу, що пішла на
титрування, см3; К – поправка на
титр розчину 2,6-дихлорфеноліндофенолу для переведення на точно розчин з
масовою концентрацією 0,001 моль/дм3 (0,001н); V – об’єм, до якого доведена наважка молока у разі додавання до неї води і
хлористоводневої кислоти, см3; V1 – об’єм рідини, що аналізується взятою для титрування, см3; g – наважка молока, г; 0,088 – кількість
аскорбінової кислоти, що відповідає 1 см3 точно розчину
2,6-дихлорфеноліндофенолу з масовою концентрацією 0,001 моль/дм3 (0,001 н),
мг. 9.16. Методи визначення фальсифікації молока Молоко, в якому
виявлена стороння речовина, вважається денатурованим (фальсифікованим).
Розрізняють характер фальсифікації (що додано до молока) і ступінь
фальсифікації (яку кількість сторонніх речовин додано). Денатурованим
вважають і таке молоко, до якого додано знежирене молоко, маслянку та
сироватку. Для визначення
характеру і ступеня фальсифікації, необхідно у стійловій і досліджуваній
пробах молока визначити густину, вміст жиру, сухих речовин і СЗМЗ. Зміни в
молоці, що відбуваються за фальсифікації, залежать від її характеру. До найчастіших
випадків фальсифікації належать: а) розбавлення
водою; б) додавання
знежиреного молока (молочних відвійок) або зняття частини вершків; в) одночасне
розбавлення відвійками і водою (подвійна фальсифікація). З метою контролю
якості молока та недопущення його фальсифікації, у ньому визначають соду,
пероксид водню, формалін, аміак та антибіотики. 1. Визначення
вмісту домішки води в молоці А. Якісна проба
Йохельсона Техніка
визначення. У пробірку наливають 2 см3 досліджуваного молока, додають 2
краплі розчину хромовокислого калію з масовою часткою 10 % і 2 см3 розчину
азотнокислого срібла з масовою часткою 0,5 %. Оцінка результату.
Кондиційне молоко забарвлюється в лимонно-жовтий колір, а молоко, розбавлене
водою – в цеглисто-червоний різної інтенсивності. Проба Йохельсона є
ефективною для дослідження фальсифікованого молока з великою кількістю води
(20−25%), проте не є точною у разі доливання води меншої кількості. Б. Розрахунковий
метод У таблиці 82
подано зміну показників якості молока за його денатурації в разі додавання до
молока води, молочних відвійок, зняття вершків. Таблиця 82 Зміна показників молока за його денатурації (за А.А.
Розановим)
Ступінь
фальсифікації – кількість доданої води – розраховують за формулою:
В – кількість
доданої води, %; СЗМЗ – масова
частка сухого молочного залишку до розбавлення водою, %; СЗМЗ1 – масова
частка сухого молочного залишку після розбавлення водою, %; А – густина молока
до розбавлення (стійлова проба), °А; А1 – устина молока
після розбавлення, °А. Приклад. Під час
аналізу двох проб молока отримані такі результати:
У пробі, що
перевіряється, відносно стійлової, всі показники знижені, отже, характер
фальсифікації – додавання води. Ступінь
фальсифікації:
Оцінка результату.
Додавання до молока 10 % води знижує його густину приблизно на 3 °А. 2. Визначення
точки замерзання молока згідно з ДСТУ 30562 (ISO 5764) (термісторний кріоскопічний метод) Більш точним
методом виявлення у молоці води є визначення його точки замерзання
(кріоскопічне число). Температура
замерзання – одна з більш сталих властивостей молока (натуральність молока).
Точка замерзання свіжого молоко від здорових корів близька до –0,550 °С і
незначно коливається в межах від –0,510 до –0,590 °С. За розведення молока
водою температура замерзання підвищується (табл. 83). Таблиця 83 Відношення температури замерзання молока до кількості
додавання води
Суть термісторного
кріоскопічного методу. Пробу молока охолоджують до заданої температури
(залежно від приладу), викликають процес кристалізації шляхом механічної
вібрації, після чого температуру швидко підвищують до плато, що відповідає
точці замерзання проби. Прилад калібрують
двома стандартними розчинами за тією ж методикою, що й для проб молока. За
цих умов плато показує точку замерзання молока в градусах Цельсію (°С). Приготування
стандартного розчину. Зважують у бюксі відповідну кількість (табл. 84) сухого
хлористого натрію. Розчиняють у дистильованій воді, кількісно переносять у
мірну колбу місткістю 1000 см3 і розчиняють до мітки дистильованою водою
температурою 20 ± 2 °С. Зберігають розчин за температури 5 °С у добре
закупорених поліетиленових пляшках місткістю не більше 250 см3. Таблиця 84 Точка замерзання стандартних розчинів
Примітка.
Калібрування кріоскопу (за Хортветом) проводять з розчином сахарози. Якщо відомий метод
калібрування, можна результати, отримані за допомогою одного методу,
скоректувати з іншим, наступним чином: ТС=0,9656ТН і
ТН=1,0356 ТС, де ТС – точка
замерзання за Цельсієм, °С; ТН – точка
замерзання за Хортветом, °Н. Перед
використанням стандартного розчину, необхідно м’яко перевернути і обертати
пляшку декілька разів, ретельно перемішуючи її вміст. Стандартний розчин не
можна збовтувати, оскільки це може призвести до потрапляння повітря. Порцію
стандартного розчину виливають з пляшки без використання піпетки. Розчини не
можуть бути використані, якщо у пляшці залишається ¼ її вмісту, а
також під час зберігання більше 2 міс без консервації фунгіцидом (наприклад,
розчином тіомерсалу 10 г/дм3). Відбір та підготовка
проб для дослідження. Бажано проби аналізувати відразу після відбору. За
необхідності, їх можна зберігати за температури нижче 5 °С. Проби можна
зберігати до 12 тижнів за температури мінус 18 °С, або їх можна зберігати
більш короткий час, застосовуючи ізотонічний розчин бактеріостатичного
реагенту. Молоко для досліду може мати температуру зберігання або кімнатну.
Однак бажано, щоб стандартні розчини і проби молока під час виміру мали
однакову температуру. Титровану кислотність молока визначають, за можливості,
одночасно з вимірюванням точки замерзання. Проведення
досліду. Перед ввімкненням кріоскопу перевіряють, чи відповідає рівень
охолоджувальної рідини, а також положення термісторного зонду в пустій
пробірці для проби інструкції виробника. Включають кріоскоп і переконуються,
що охолоджувальна рідина добре перемішується або циркулює. Після 12-год
ввімкнення перевіряють температуру охолоджувальної рідини, положення та
амплітуду вібрації дроту для перемішування. Робоча
калібрувальна перевірка. Перед кожною серією дослідів визначають точку
замерзання стандартного розчину хлористого натрію (наприклад, розчин з точкою
замерзання мінус 0,512 °С), доки різниця в двох послідовних вимірах не буде
перевищувати 0,002 °С. Якщо середнє значення відрізняється від точки
замерзання стандартного розчину більше 0,002 °С, кріоскоп повторно
калібрують. Якщо кріоскоп працює безперервно, калібрування проводять не рідше
1 разу за годину. Вимірювання.
Контейнер з пробою обережно перевертають і обертають кілька разів, перемішуючи
вміст. Виливають або переносять піпеткою пробу молока в кількості (2,5±0,1)
см3 у чисту суху пробірку для проб. Переконуються, що зонд і дріт для
перемішування чисті й сухі (за необхідності, їх витирають м’якою чистою не
волокнистою тканиною). Вставляють пробірку у відкалібрований кріоскоп. Молоко
охолоджують і викликають кристалізацію за установленої температури з точністю
0,1 °С (у деяких автоматичних приладах температуру можна спостерігати на
цифровій шкалі; в інших пробах необхідна точність утворення кристалізації
забезпечується, коли стрілка гальванометру співпадає з відповідною поділкою). Якщо з будь-якої
причини кристалізація починається до встановленої температури, вимірювання
завершують і дослідження повторюють з іншою порцією молока. Якщо й інша проба
передчасно кристалізується – пробу підігрівають до 45 °С і витримують 5 хв
для розтоплення кристалів жиру. Потім знову охолоджують до (20±2) °С і зразу
повторюють вимірювання. Після початку кристалізації, температура молока
швидко підвищується і деякий час зберігається фактично постійною до її
зниження. Точкою замерзання є найвища на даний період температура і це
значення повинно бути зареєстрованим. Після завершення
вимірювань, пробірку виймають, термісторний зонд і дріт для перемішування
ополіскують водою, потім висушують м’якою, чистою не волокнистою тканиною, і
проводять паралельний дослід з другою пробою того ж молока. Якщо різниця в
паралельних вимірюваннях більше, ніж 0,004 °С, результати відкидають і
виконують ще два послідовні вимірювання. Обробка
результатів. Якщо робоче калібрування проведено вірно, за результат беруть
середнє арифметичне значення двох паралельних вимірювань, заокруглених до
третього десяткового знаку. Приклад обчислення
середнього арифметичного значення двох паралельних досліджень. Якщо сума двох
паралельних вимірювань є непарною, – середнє арифметичне значення
заокруглюють до найближчого парного. 3. Виявлення
додавання молочних відвійок або зняття частини вершків У даному випадку
густина підвищується, вміст жиру і сухих речовин знижується, а СЗМЗ не
змінюється або злегка підвищується. Ступінь фальсифікації молочними
відвійками розраховують за формулою:
ЗМ – масова частка
доданих молочних відвійок (знежирене молоко), %; Ж – масова частка
жиру до розбавлення, %; Ж1 – масова частка
жиру після розбавлення, %. Приклад. Під час
дослідження стійлових і контрольних проб (які перевіряють), отримані наступні
дані:
У пробі, що перевіряється
(контрольна проба), показники масової частки жиру і СР знижені порівняно зі
стійловою, а густина і масова частка СЗМЗ – дещо збільшені. Це свідчить про
те, що до молока додано знежирене молоко. Ступінь фальсифікації:
Для більшої
вірогідності під час встановлення характеру фальсифікації (додавання молочних
відвійок), проводять розрахунок за визначенням жиру в сухій речовині молока
за формулою:
Жср – масова
частка жиру у сухій речовині молока (%); Ж1 – масова частка
жиру у досліджуваному молоці (%); С1 – масова частка
сухої речовини у досліджуваному молоці (%). Приклад: У цьому випадку
фальсифікації вміст жиру у сухій речовині може зменшуватися. Якщо жиру у
сухій речовині менше 25 %, – це вказує на додавання до молока знежиреного
молока або зняття частини вершків. 4. Виявлення
подвійної фальсифікації молока У разі одночасного
додавання до молока води і знежиреного молока знижується вміст сухих речовин,
СЗМЗ, а густина не змінюється або значно не відхиляється від співвідношення
доданих продуктів. Для встановлення
ступеня цієї фальсифікації користуються формулами:
ЗМ = Д – В, де Д – загальна
кількість води і знежиреного молока (%); Ж1 – масова частка
жиру у контрольній пробі, що перевіряється (%); Ж – масова частка
жиру у натуральному молоці (стійлова проба) (%); В – масова частка
води, доданої до молока (%); СЗМЗ – масова
частка сухого знежиреного молочного залишку у досліджуваній (що
перевіряється, контрольній) пробі (%); СЗМЗ1 – масова
частка сухого знежиреного молочного залишку у стійловій пробі (%); ЗМ – масова частка
доданого знежиреного молока, %. Приклад: Під час
дослідження проб молока отримані наступні показники:
Характер
фальсифікації: у молоко додана вода і знежирене молоко, оскільки в пробі, що
перевіряється, порівняно зі стійловою, густина дещо змінилася, а решта
показників – зменшилися. Ступінь
фальсифікації:
Кількість доданого
знежиреного молока: ЗМ = 47,4– 8=39,4 %. 5. Визначення
вмісту домішки крохмалю або борошна у молоці Суть методу.
Крохмаль або борошно додають до молока для підвищення його в’язкості
(густини). Виявлення їх ґрунтується на реакції йоду з крохмалем, що
забарвлюється від наявності йоду, в синій колір. Техніка
визначення. 1. У пробірці змішати по 5 см3 молока і 2–3 краплі спиртового
розчину йоду з масовою концентрацією 0,5 %. Оцінка результату.
Встановити зміну забарвлення – за наявності крохмалю або борошна молоко
забарвлюється у синій колір, за відсутності крохмалю або борошна – в
блідо-жовтий. 9.17. Визначення у молоці інгібувальних речовин Чинний стандарт
ГОСТ 24065 передбачає дослідження молока на визначення інгібувальних речовин,
до яких належать антибіотики, формалін, пероксид водню та інші
мийно-дезінфікуючі та консервувальні речовини. 1. Визначення
вмісту домішки соди у молоці Визначення в
молоці соди проводять згідно з ГОСТ 24065 Суть методу. У
разі додавання до молока соди, реакція його стає лужною. Для визначення
конкретної інгібувальної речовини до молока додають індикатор (фенолрот,
розолову кислоту, бромтимоловий синій), який в кислому і лужному середовищі
має різне забарвлення. А. Проба з фенолротом Техніка
визначення. У пробірку наливають 3–5 см3 досліджуваного молока і додають 3–5
крапель розчину фенолроту (0,1 см3 фенолроту + 20 см3 розчину етилового
спирту з масовою часткою 96 % + 80 см3 дистильованої води). Вміст пробірки
струшують. Оцінка результату.
За наявності в молоці соди – вміст пробірки забарвлюється в яскраво-червоний
колір, за відсутності – помаранчевий або червоно-жовтий. Б. Проба з
розоловою кислотою Методика
дослідження. У пробірку наливають 3–5 см3 досліджуваного молока і додають 3–5
см3 спиртового розчину розолової кислоти з масовою часткою 0,2 %. Оцінка результату.
За наявності в молоці соди – вміст пробірки забарвлюється в малиново-червоний
колір, за відсутності – коричнево-жовтий (оранжевий). В. Проба з
бромтимоловим синім (метод Косолапова) Техніка визначення.
У пробірку наливають 5 см3 досліджуваного молока і обережно, по стінці,
додають 7–8 крапель індикатора – спиртового розчину бромтимолового синього з
масовою часткою 0,04 %. Оцінка результату.
Через 10 хв спостерігають за зміною кольору кільцевого шару, не допускаючи
струшування пробірки. Жовтий колір
вказує на відсутність домішки соди в молоці. Зелений колір та всі відтінки –
від світло- до темно-зеленого включно, вказує на наявність в молоці соди. Жовто-зелений
колір – наявність соди в кількості 0,03 %; світло-зелений – 0,05 %; зелений –
0,07–0,10 %; темно-зелений – 0,2 %; синьо-зелений – 0,3 %. 2. Визначення
вмісту домішки вапна (вапнованої води) у молоці Вапно або
вапновану воду, як і соду, додають до молока у літній період з метою попередження
його скисання, оскільки, в такому разі, молоко довше зберігається за високих
температур. Техніка
визначення. Частину молока профільтрувати через марлевий фільтр. До фільтрату
додати кілька крапель оцтової або лимонної кислоти. Оцінка результату.
На поверхні молока з домішками вапна будуть з’являтися добре помітні пухирці
вуглекислого газу, на відміну від кондиційного молока. 3. Виявлення
вмісту домішки пероксиду водню у молоці Молоко
фальсифікують пероксидом водню з метою зниження кислотності, недопущення його
скисання під час зберігання без охолодження. Техніка
визначення. У пробірку до 1 см3 молока додають краплю сірчаної кислоти
густиною 1,830–1,835 г/см3 і 0,2 см3 йодисто-калієвого крохмалю, перемішують. Оцінка результату.
Моментальне посиніння свідчить про вміст пероксиду водню більше 0,01 %. Поява
у пробірці окремих плям синього кольору свідчить про наявність пероксиду
водню у молоці. Якщо через 10 хв
немає синього забарвлення – пероксид водню відсутній. Приготування
йодисто-калієвого крохмалю. Наважку крохмалю масою Для визначення
придатності розчину йодисто-калієвого крохмалю проводять наступні
дослідження: у пробірку наливають 5 см3 прокип’яченого охолодженого молока,
додають 5 крапель розчину йодисто-калієвого крохмалю і 5 крапель розчину
пероксиду водню з масовою концентрацією 0,5 %, ретельно перемішують уміст
пробірки. Поява темно-синього або сірувато-синього забарвлення вказує на
непридатність розчину до використання для досліджень. 4. Визначення
вмісту домішки хлору в молоці Методика
дослідження. 1. У широку пробірку наливаємо досліджуване молоко у кількості
10 см3, додають 1 см3 розчину йодистого калію з масовою часткою 5 % та 1 см3
свіжоприготовленого розчину крохмалю з масовою часткою 2 %. 2. Перемішують
уміст пробірки, додають 10 см3 концентрованої хлористоводневої кислоти, знову
перемішують. Оцінка результату.
За наявності хлору молоко через 1–10 хв забарвлюється в синій колір. 5. Визначення
вмісту домішки формаліну в молоці (реакція з сірчаною та азотною кислотами) Для приготування
суміші кислот відмірюють 100 см3 концентрованої сірчаної кислоти (густина 1,80
г/см3) і додають краплю концентрованої азотної кислоти. Методика
дослідження. У пробірку наливають 5 см3 досліджуваного молока, потім обережно
приливають 5 см3 суміші концентрованих сірчаної та азотної кислот так, щоб
молоко з реактивом не змішувалося, а нашаровувалося. Оцінка результату.
Про наявність формаліну свідчить кільце фіолетового кольору, а про
відсутність – поява жовтувато-бурого кільця. Фіолетове кільце
з’являється відразу або через 1–2 хв, за незначної кількості (менше 0,00001
%) – через 30–50 хв. 6. Визначення
вмісту домішки двохромовокалієвої солі (хромпіку) в молоці Методика
дослідження. У пробірку наливають 2–3 см3 досліджуваного молока і приливають
2–3 см3 розчину азотнокислого срібла (АgNO3) з масовою часткою 2 %. Оцінка результату.
За наявності в молоці хромпіку (K2Cr6O7) – вміст пробірки забарвлюється в червоно-жовтий колір, за відсутності
– вміст пробірки без змін (білий колір). 7. Визначення
вмісту домішки мийних і дезінфікуючих речовин Методика
дослідження. У пробірку наливають 2–3 см3 досліджуваного молока і додають 1–2
краплі індикатора – спиртового розчину бромтимолового синього з масовою
часткою 1 %. Оцінка результату.
Інтенсивне посиніння в пробірці вказує на лужну реакцію молока – наявність у
досліджуваному молоці домішки мийних і дезінфікуючих речовин. 8. Визначення
вмісту домішки аміаку або солей амонію в молоці згідно з ГОСТ 24066 В основу методу
покладена специфічна реакція, що дає змогу визначити наявність аміаку або
його солей за зміною забарвлення молочної сироватки під час взаємодії з
реактивом Неслера. Методика
дослідження. 1. У стаканчик наливають близько 20 см3 молока і нагрівають на
водяній бані до 35...40 ºС. 2. У підігріте
молоко вносять 1,0–1,5 см3 розчину оцтової кислоти з масовою часткою 10 %. 3. Для осадження
казеїну, пробу залишають на 10 хв, потім піпеткою з ваткою на кінці
відбирають 2 см3 відстояної сироватки і переносять у пробірку. 4. Сюди ж додають
1 см3 реактиву Неслера. Уміст пробірки перемішують, спостерігаючи за зміною
кольору суміші. 5. Одночасно
ставлять контрольну пробу з натуральним сирим молоком. Оцінка результату.
Поява в пробірці лимонно-жовтого забарвлення свідчить про наявність аміаку в
кількості, характерній для натурального молока. Поява жовтого або жовто-оранжевого
забарвлення свідчить про підвищений уміст аміаку, що вказує на можливу
фальсифікацію або порушення санітарних умов одержання молока. Зміну забарвлення
суміші спостерігають упродовж перших 1–2 хв. Чутливість методу – 6–9 мг%
аміаку. Дослідження проводять не раніше, ніж через 2 год після доїння. 9. Виявлення в
молоці білого стрептоциду (за Н.М. Носковим) Білий стрептоцид,
доданий у щойно видоєне молоко у кількості 0,03–0,08 %, консервує його на 48−72
год. Таке молоко має нормативні органолептичні показники і кислотність. Методика
дослідження. 1. У дві аглютинуючі пробірки наливають по 1 см3 молока і 0,25 см3 діазореактиву. 2. Уміст
перемішують упродовж 3 хв. 3. Додають 0,25
см3 розчину бета-нафтолу з масовою часткою 2 %. Приготування
бета-нафтолу: 1 частина спиртового розчину нафтолу з масовою часткою 20 %, 5
частин розчину NaOH з масовою часткою 20 % і 4 частини Н2О. Реактив зберігають не більше 7 діб. Приготування
діазореактиву: 1 частину розчину натрію азотнокислого з масовою часткою 1 % змішують
з 1 частиною розчину хлористоводневої кислоти з масовою часткою 7 %. Реактив
готують за 5 хв до проведення дослідження. За наявності у молоці стрептоциду,
воно набуває кольору з різними відтінками:
10. Визначення
інгібувальних речовин у молоці Для проведення
аналізу відбирають 50 см3 молока середньої проби, яку можна зберігати в
холодильнику за температури 6–8 ºС не більше доби. Методи базуються
на відновленні резазурину і метиленового синього за розмноження у молоці
термофільних стрептококів, чутливих до інгібувальних речовин. 10.1. Визначення
інгібувальних речовин з індикатором резазурином згідно з ГОСТ 23454 Для приготування
розчину з масовою часткою 0,05 %, 100 мг резазурину розчиняють у 200 см3
прокип'яченої i охолодженої дистильованої води. Розчин зберiгають у склянках з темного скла не бiльше 20 дiб за температури 3...5 ºС. Колекцiйну тест-культуру готують так: у пробiрку з 10 см3 стерильного збираного молока вносять одну
бактеріологічну петлю колекцiйної тест-культури Streptocoссus thermophilus, або в пляшечку iз 100 см3 стерильного збираного молока вносять 1 см3 тієї ж
культури i витримують
у термостаті впродовж 16–18 год за температури 42...43 ºС. Для проведення
аналiзування використовують 1–2-добову культуру за умови
зберiгання її в холодильнику за температури 6...8 ºС.
Напередоднi використання,
робочу культуру перемішують інтенсивним струшуванням. Посуд, що
використовують для приготування i внесення тест-культури, стерилiзують. Новий посуд кип’ятять у пiдкисленiй водi впродовж 15 хв.
Гумові корки стерилiзуютъ в автоклавi за 0,1 Мпа впродовж 20 хв. Методика
дослідження. 1. У чистi пробiрки наливають по
10 см3 молока i закривають стерильними гумовими пробками. Решту проби зберiгають до кiнця аналiзування в холодильнику за температури 6...8 ºС. 2. Одночасно
проводять контрольне аналiзування. Для цього, у пробiрку наливають 10 см3 вiдновленого препарату (СКІР), одержаного розчиненням сухого препарату у
флаконi з 10 см3 дистильованої води за тeмпеpaтypи 50 ºС. 3. Пробiрки з дослiджуваним молоком i контрольною пробою нагрiвають на водянiй банi до 85...90 ºС, потiм охолоджують до 43...45 ºС i стерильною пiпеткою у пробірки вносять 0,3 см3 робочої
тест-культури. 4. Уміст пробiрки перемiшують триразовим перевертанням i витримують упродовж 2 год у редуктазнику або на водянiй банi за температури 42...43 ºС. 5. У пробiрки з молоком i контрольною пробою вносять по 1 см3 розчину резазурину
з масовою часткою 0,05 % за температури 18...20 °C. Уміст пробірок перемiшують дворазовим перевертанням. 6. Пробiрки витримують у редуктазнику або на водянiй банi впродовж 15 хв за темпеpaтypи 42...43 ºС. Оцінка результату.
У разі вiдсутності iнгiбувальних речовин, колір дослiджуваного молока буде рожевим або бiлим. За наявностi iнгiбувальних речовин молоко буде мати синьо-стальне,
синьо-фiолетове або фiолетове забарвлення. Метод дaє змогу виявити в молоцi вміст пенiцилiну білъше 0,01 МО/см3, формалiну – близько 0,005 %, пероксиду водню – бiльше 0,01 %. 10.2. Визначення
інгібувальних речовин із метиленовим синім згідно з ГОСТ 23454 Приготування
колекцiйної робочої тест-культури проводять аналогічно визначенню
iнгiбувальних речовин iз резазурином. Для приготування
водного розчину пептону з масовою часткою 3 %, беруть Для приготування
водного розчину метиленового синього з масовою часткою 0,5 % беруть 500 мг
фарби i вносять у колбу, доливають 100 см3 дистильованої
кип’яченої води i перемiшують до повного
розчинення. Розчин зберiгають у щiльно закритому
посудi не бiльше 30 дiб за температури
6...8 ºС. За приготування
сумiшi для аналiзу, до 20 см3 водного розчину пептону з масовою часткою
3 % додають 3,5 см3 однодобової культури термофiльного стрептококу (пiпетку заздалегідь потрiбно старанно прополоскати цiєю ж cумішшю) i 0,1 см3 водного
розчину метиленового синього з масовою часткою 0,5 %. Сумiш старанно перемішують (готують безпосередньо перед
аналізуванням). Методика
дослідження. 1. У чистi пробiрки наливають по
10 см3 дослiджуваного молока i закривають гумовими пробками. Решту проби зберігають у
холодильнику за температури 6...7 ºС упродовж доби. 2. Пробiрки з дослiджуваним молоком нагрiвають на водянiй банi до 85–90 ºС i, витримавши 10 хв, охолоджують до температури 42...45 ºС. 3. У пробiрки стерильною пiпеткою вносять по 2 см3 приготовленої сумiшi, перемiшують триразовим
перевертанням i витримують на водяній банi вiд 1 год 40 хв до 2 год 20 хв за температури 41...42 °C. Оцінка результату.
У разі вiдсутностi в молоцi iнгiбувальних речовин, уміст пробiрок буде мати синій колiр. Синє кiльце, що утворюється в пробiрцi на поверхнi молока висотою 11. Виявлення у
молоці антибіотиків Антибіотики
з’являються у молоці внаслідок: а) застосування
необґрунтованих доз під час лікування тварин; б) унесення в
молоко з метою недопущення його псування; в) інтенсивного
розмноження мікроорганізмів, здатних виробляти антибіотичні речовини. Антибіотики у
молоці негативно впливають на життєдіяльність мікрофлори заквасок (на
пеніцилін не діє навіть пастеризація), що різко сповільнює процеси
сквашування молока. Внаслідок цього порушуються процеси ферментації в
технології сирів. У багатьох молочних продуктах виявляють дефекти – гнильний
смак і запах, гіркий присмак, дефекти консистенції. Наявність
антибіотиків у молоці завдає значних економічних збитків молочній промисловості
та великої шкоди здоров’ю людей. Молочна промисловість не може виготовити з
такого молока молочні продукти. Вживання ж молока навіть з незначною
кількістю антибіотиків може спричинити у людей небезпечні захворювання
(алергію, токсичну дію, дисбактеріоз), а також звикання умовно патогенної
мікрофлори, що є в організмі, до антибіотиків. Наступне лікування
антибіотиками будь-якого захворювання є безрезультатним. Техніка
визначення. 1. У дві пробірки вносять по 10 см3 досліджуваних проб молока. 2. Закривають
ватними корками і прогрівають на водяній бані за температури 85...90 °С
упродовж 5 хв. 3. Охолоджують
проби до температури 45 °С і вносять у кожну пробірку по 0,5 см3
16–18-годинної культури термофільного стрептокока, приготованої попередньо на
знежиреному молоці звичайним способом. 4. Пробірки з
молоком і внесеною культурою струшують і поміщають в редуктазник за
температури 40...42 °С на 1,5 год. 5. У кожну
пробірку швидко додають по 1 см3 розчину резазурину з масовою концентрацією
0,05 %, струшують і знову поміщають у редуктазник за температури 40...42 °С
на 10 хв. Відмічають зміни
кольору. Оцінка результату.
Збереження початкового кольору або незначна його зміна (до бузкового)
свідчить про затримання розвитку у досліджуваному молоці культури термофільного
стрептокока і, отже, про наявність у зразку антибіотиків. У разі відсутності
антибіотиків у молоці, початковий колір змінюється до рожевого або
перетворюється на білий. Оцінку результатів досліджень проводять за таблицею
85. Цей метод дозволяє
визначати наявність у молоці пеніциліну в кількості від 0,001 до 0,02 Од/см3
і вище, стрептоміцину – від 0,005 до 2,0 Од/см3 і вище. Таблиця 85 Колір молока під час дослідження на наявність
антибіотиків
12. Визначення
антибіотиків за допомогою дельвотесту Зміст методу. Дельвотест
являє собою стандартний дифузний тест для визначення залишкової кількості
антибіотиків і сульфамідних препаратів. Основними
перевагами цього методу є: надійність і точність; надзвичайно висока
чутливість до антибіотиків групи пеніциліну; достатньо висока чутливість до
більшості інших антибактеріальних речовин; простота виконання та легкість
визначення результатів; тривалий термін зберігання й придатності. Агарове середовище
містить стандартизовану кількість спор мікроорганізмів Bacillus stearothermophilus. Цей вид бактерій взяли через високу чутливість до
більшості антибіотиків, особливо до групи пеніцилінів та інших беталактамних
речовин. У разі зберігання у холодних умовах, спори залишаються життєздатними
впродовж багатьох місяців. У разі додавання спеціальної таблеткової поживної
речовини і збільшенні температури до 64 °С спори швидко розмножуються і продукують кислоту.
Коли кислота накопичується, відбувається зміна кольору індикаторного середовища
з фіолетового на жовтий. Якщо проба молока містить інгібувальні речовини, а
саме, залишки антибіотиків, а їх концентрація буде досить високою, вони
затримують процес розмноження бактерій і, відповідно, утворення кислоти. В
цьому випадку колір тесту не зміниться на жовтий, а залишиться фіолетовим. Якщо концентрація
інгібітора близька до межі визначення, колір індикаторного середовища буде
знаходитися між жовтим і фіолетовим. Поведінка мікроорганізмів, а саме розмноження, розвиток і утворення кислоти,
залежить від температури витримування. Як висока, так і низька температура
спричиняють сповільнення цих процесів і призводить до більш тривалого
проведення аналізу. Відбір проб.
Дельвотест розроблений для об’єму проби 0,1 см3. Чутливість методу не дуже
залежить від точності цього об’єму, проте, бажано, щоб відхилення становило
не більше 10 %. Проба не повинна містити піни та пухирців повітря, а також у
жодному разі не можна однією й тією ж піпеткою відбирати більше, ніж одну
пробу. За такої малої кількості навіть одна крапля від попередньої проби, що
містила антибіотики, може вплинути на результати аналізу. Необхідно
маніпулювати поршнем шприца не надто швидко, що практично виключає його
забруднення, у зв’язку з цим його можна використовувати кілька разів. Контрольні проби.
Для забезпечення максимальних умов аналізу або для перевірки оптимального
часу витримування, можна, паралельно з пробами молока, проводити періодичні
дослідження контрольних проб. Як контрольну пробу, беруть молоко, яке точно
не містить будь-яких інгібувальних речовин. Контрольні (негативні) проби
можуть проводитися разом з дельвотестом. Як пробу, не можна використовувати
воду. Зберігання зразків
молока. Якщо немає можливості протестувати пробу молока в межах кількох годин
після відбору, її зберігають у холодному місці, а якщо тестування відкладається
на наступний день, проби необхідно зберігати глибоко замороженими. Підтвердження
результатів. Підтвердження наявності антибіотиків групи бета-лактамів у пробі
молока, яка визнана позитивною, здійснюється таким чином: змішують 1 см3
проби молока з 0,1 см3 розчину 10 МО penicillinase типу 1 (наприклад, Bacillus cereus) і 1 см3 води. Потім 0,1 см3 цієї суміші досліджують
за допомогою дельвотесту. Інтерпретація
результату. Якщо тест дає жовте забарвлення, це свідчить про відсутність
бета-лактамних антибіотиків (penicillin G, ampicillin, cloxacillin, cephapirin, cefuroxim тощо) у пробі молока. Можна підтвердити наявність
залишку сульфамідних та інших подібних інгібувальних речовин шляхом
тестування 1 см3 суміші, що складається з 1 см3 молока і 0,1 см3 натрієвої
солі амінобензойної кислоти. Жовте забарвлення повторного тесту підтверджує
наявність сульфамідів, сульфонів або антифолатів у відповідній пробі молока. Анормальне молоко.
Існує незначна достовірність того, що результат тесту виявиться неточним,
унаслідок наявності у молоці так званих природних інгібувальних речовин. Ці
речовини містяться у вимені корів у період їх отелення (в молозиві); у
випадку захворювання на мастит, вони мають антибактеріальну активність та
діють інгібувально в усіх системах бактеріальних аналізів. Чутливість до
мийних та дезінфікуючих речовин. Ймовірність одержання помилкової позитивної
реакції через забруднення проби мийними або дезінфікуючими речовинами можливе
у випадку високої концентрації цих речовин. Якщо їх застосовують для очищення
доїльного обладнання або обробки вим’я, їх залишкова концентрація у молоці
надзвичайно мала, щоб вплинути на процедуру тестування. Загалом, дельвотест
сприйнятливий до таких речовин лише за концентрації 0,1 % (100 частин на н.)
або вище (табл. 86). Консерванти, які використовують, щоб зберегти
молоко для наступних досліджень, роблять молоко непридатним для тестування. Таблиця 86 Концентрація окремих мийних і дезінфікуючих речовин, що дають позитивний
результат під час тестування
Контроль якості.
Кожна виготовлена партія дельвотесту підлягає спеціальному цифровому
кодуванню, контролю на час інкубації, необхідний для тестування негативної
контрольної проби молока і дослідження на чутливість до окремих
антибактеріальних речовин. Поживні таблетки мають своє індивідуальне
кодування. Впродовж терміну зберігання, час інкубаційного витримування
постійно збільшується, але незначно. Тести, термін придатності яких близький
до закінчення, можуть потребувати більшої тривалості інкубації, ніж свіжі. Ветеринарно-санітарне
оцінювання. Молоко, одержане від корів, які піддавалися лікуванню
антибіотиками, забороняється використовувати для харчових потреб (після
останнього введення препаратів) згідно з даними, наведеними у таблиці 87.
Молоко, що містить антибіотики, але має нормальний зовнішній вигляд, після
кип’ятіння або пастеризації використовують на корм тваринам. Таблиця 87 Термін бракування молока корів після введення
антибіотиків
9.18. Методи контролю температурної обробки сирого
молока Температурну
обробку (пастеризацію, стерилізацію) сирого молока проводять з метою знищення
мікроорганізмів й інактивації їх ферментів, які знижують стійкість молока і в
наступному спричиняють дефекти молочних продуктів. Пастеризація –
теплова обробка молока за температур, нижчих від температури його кипіння, що
спрямована на знищення вегетативних форм бактерій. Методи визначення
ефективності пастеризації молока і молочних продуктів подано у ГОСТ 3623. Залежно від
температурних режимів, на молокопереробних підприємствах України застосовують
такі режими пастеризації молока: висока (ГОСТ
3623–73): 85 °С – миттєво; 80 °С – упродовж 30 с; 75 °С – упродовж 10
хв. низька (ГОСТ 3623
– 73): 63 °С – упродовж 30 хв; 72 °С – упродовж 20 с. Ефективність
пастеризації залежить від ступеню бактеріального обсіменіння молока і,
особливо – наявності термофільних бактерій. Контроль
пастеризації молока базується на визначенні в молоці ферментів фосфатази та
пероксидази. Фосфатазною пробою
визначають ефективність низькотемпературної обробки молока (від 62 до 65 °С
упродовж 30 хв та 72 °С – 20 с). Пероксидазною
пробою користуються для перевірки ефективності високотемпературної
пастеризації, оскільки фермент пероксидаза руйнується під час нагрівання
молока не нижче ніж 75 °С упродовж 10 хв та більше. Ефективність
пастеризації залежить від температури, тривалості впливу, ступеня
бактеріальної забрудненості молока і якісного складу мікрофлори. Мікрофлору, що
залишається в молоці після пастеризації, називають залишковою мікрофлорою
пастеризованого молока. Характер залишкової мікрофлори залежить, у першу
чергу, від режиму пастеризації. Так, мікрофлора молока, пастеризованого за
температури 85 °С без витримки, складається з термостійких молочнокислих
паличок і бактеріальних спор. У разі короткочасної і тривалої пастеризації,
залишкову мікрофлору утворюють, переважно, термофільні молочнокислі
стрептококи і палички, ентерококи, мікрококи, бактеріальні спори,
бактеріофаги. Ефективність
пастеризації вважають задовільною, якщо кількість залишкової мікрофлори
становить не більше, ніж 0,1 % і за відсутності Е. сoli у 10 см3 пастеризованого молока. Під час
виробництва питного молока, найпоширенішим режимом є пастеризація за
температури 76 ºС з витримуванням упродовж 20 с. Пастеризоване молоко
фасують у скляні пляшки, паперові пакети з полімерним покриттям,
поліетиленові пакети місткістю 0,25; 0,5 і Молоко для
заквасок пастеризують за 92...95 °С з витримуванням 20–30 хв. За такого режиму знищуються усі вегетативні форми й
бактеріофаги, у молоці залишаються лише спори бактерій. У сироварінні
режими пастеризації обирають таким чином, щоб знищити патогенні й
газоутворювальні бактерії, бактерії групи кишкових паличок – температура
72...74 °С з витримуванням 15...20 с. У разі значного
мікробного обсіменіння сирого молока (>106 КУО в 1 см3) ефективність пастеризації знижується, тому
застосовують інший режим пастеризації: температура 75...77 °С і витримування
близько 35 с. 1. Пероксидазна
проба з йодисто-калієвим крохмалем Суть методу. Метод
ґрунтується на розкладанні пероксиду водню ферментом пероксидазою, що
міститься в молоці і молочних продуктах. Активний кисень, що звільнився під
час розкладання пероксиду водню, окиснює йодистий калій, звільняє йод, який з
крохмалем утворює сполуку синього кольору. Підготовка
йодисто-калієвого крохмалю: Техніка
визначення. 1. У пробірки налити по 5 см3 різних проб молока, 5 крапель розчину пероксиду водню з масовою концентрацією
0,5 % і 5 крапель розчину
йодисто-калієвого крохмалю. 2. Після додавання
кожного реактиву вміст пробірок перемішати. Оцінка результату.
Наявність пероксидази визначають за зміною забарвлення: 1. За відсутності
ферменту пероксидази колір молока не змінюється впродовж 1 хв. Це свідчить
про те, що молоко пастеризували з дотриманням температурного режиму, згідно з
інструкцією і пероксидазу зруйнували повністю нагріванням за температури 80
°С. За наявності
пероксидази в молоці, якщо уміст пробірок не довше, ніж через 2 хв набуває
блідо-блакитного забарвлення – це вказує на часткове руйнування пероксидази
дією на молоко температури 65...70 °С, тобто молоко не піддавалося
пастеризації або піддавалося пастеризації за температури нижче 80 °С, чи було
змішане з не пастеризованим. Поява забарвлення
в пробірках через 2 хв після внесення йодисто-калієвого крохмалю і пероксиду
водню не свідчить про відсутність пастеризації (може спричинялися непридатністю
реактивів). Чутливість методу
дає змогу виявити додавання до пастеризованого молока не менше 5 % не
пастеризованого. 2. Фосфатазна
проба з фенолфталеїнфосфатом натрію Суть метода.
Фермент фосфатаза більш чутливий до високих температур. Він руйнується
нагріванням за температури 63 °С упродовж 30 хв або за температури 72 °С – 20 с. Проба
рекомендується для контролю пастеризації молока за режимів температури 63…65
°С. Крім того, за допомогою цієї проби можна встановити додавання до
пастеризованого або кип’яченого молока сирого в кількості 2 % і більше. Методика
дослідження. У пробірку наливають 2 см3 досліджуваного молока, 1 см3 розчину
фенолфталеїнфосфату натрію з масовою концентрацією 0,1 % в аміачному
буферному середовищі, закривають пробірку корком і, після ретельного
перемішування вмісту, пробірку поміщають на водяну баню за температури
40...45 °С. Результати реакції перевіряють через 10 хв і 1 год. Аміачна буферна
ємність складається з 80 см3 1 н розчину аміаку і 20 см3 1 н розчину хлористого амонію (рН суміші = 9,8). Розчин
фенолфталеїнфосфату натрію з масовою концентрацією 0,1 % готують таким чином:
Розчин зберігають
у темній склянці з притертим корком у темному прохолодному місці. Не можна
використовувати реактив з рожевим забарвленням. Суть реакції:
фенолфталеїнфосфат натрію у лужному середовищі безбарвний. Фермент фосфатаза,
відщеплюючи від нього фосфат, вивільняє фенолфталеїн, що й надає вмісту
пробірки червоного забарвлення, а за незначної активності фосфатази –
рожевого. Результати
реакції. У пробірці з пастеризованим
молоком (фосфатаза інактивована) жодних змін у забарвленні не виявляють. У разі порушення
режиму пастеризації, коли фосфатаза залишається в активному стані, вміст
пробірки буде мати колір від світло- до яскраво-рожевого. Аналогічне
забарвлення виявляють і в тому випадку, коли молоко сире або пастеризоване,
проте розведене сирим молоком. Необхідно
врахувати й те, що внаслідок незначного чи часткового нагрівання, фосфатаза
може залишитися частково активною. Цей фактор може суттєво сповільнити
швидкість появи забарвлення, яке виявляють пізніше, ніж через 1 год. У такому
випадку додають 3 краплі хлороформу, закривають корком, перемішують і
залишають на 24 год за кімнатної температури. Якщо через 24 год рожеве
забарвлення не з’явиться, реакцію вважають «негативною». 3.
Лактоальбумінова проба Суть реакції: під
впливом нагрівання за температури вище 80 °С альбумінова фракція молока
зсідається. Методика
дослідження. І варіант. 1. У
колбочки чи склянки наливають 5 см3 досліджуваного молока і 20 см3
дистильованої води, додають 3 см3 розчину сірчаної кислоти з масовою
концентрацією 0,1 моль/дм3. 2. Казеїн, що
випадає в осад, відфільтровують. 3. Відмірюють у
пробірку 5 см3 прозорого фільтрату і кип’ятять. ІІ варіант. 1. У пробірку
відмірюють 5 см3 досліджуваного молока, 10 см3 дистильованої води, після чого
з бюретки краплями вносять у пробірку слабкий розчин оцтової кислоти до появи
дрібних пластівців казеїну. 2. Через 2−3
хв уміст пробірки профільтровують через паперовий фільтр, а фільтрат
кип’ятять. Оцінка результату.
1. У молоці, пастеризованому за температури вище 80 °С, не виявляють
пластівців альбуміну; у разі кип’ятіння досліджуваної проби – фільтрат
залишається прозорим. 2. У пробі молока,
сирого чи пастеризованого за температури нижче 80 °С, з’являються пластівці альбуміну у різній кількості
залежно від ступеня та тривалості нагрівання молока. Чинники, що
впливають на точність аналізу: 1. Порушення
техніки приготування реактивів. 2. Підвищена
кислотність молока. 3. Не витриманий
температурний режим. 9.19. Визначення кетонових тіл у молоці Молоко від корів,
хворих на кетоз, містить кетонові тіла, небезпечні для людей. У такому молоці
підвищується кислотність і хлор-цукрове число. У молоці, пастеризованому за
температури 72 °С упродовж 30 хв або 85 °С без витримування, якісна реакція
на кетони – негативна. Молоко корів,
хворих на кетоз, рекомендується пастеризувати. Унаслідок
порушення обміну речовин, у молоці можуть з’являтися кетонові тіла. Є
повідомлення про токсичність молока з кетоновими тілами для людей. У разі
позитивної реакції на кетонові тіла молоко вибраковують. У виробничих
умовах використовують реакції у модифікаціях (за К.В. Марковою та Россу). 1. Реакція за
Россу Техніка
визначення. 1. У пробірку насипають 2. Додають 5 см3
досліджуваного молока і ще кілька маленьких крупинок гідроксиду натрію.
Оцінка результатів представлена у таблиці 88. 3. Пробірку з
умістом струшують і залишають на 5 хв за кімнатної температури. 2. Реакція за К.В.
Марковою Техніка
визначення. До 10 см3 досліджуваного молока додають Пробірку з умістом
струшують; через 5 хв оцінюють результати згідно з таблицею 88. Таблиця 88 Оцінювання
реакції на наявність кетонових тіл у молоці
3. Експрес-реакція
для визначення кетонових тіл в молоці Техніка
визначення. До 1 краплі молока на фільтрувальному папері додають декілька
кришталиків нітропрусиду натрію і сульфіту амонію. Якщо з’являється
фіолетове забарвлення, реакція вважається позитивною. 9.20. Методи визначення молока, отриманого від корів
хворих на мастит Мастит –
захворювання молочної залози внаслідок механічної дії, застудного чи
інфекційного чинників. За маститу у
молоці підвищується: вміст сухих речовин жиру, білка, солей, альбумінів та
глобулінів, хлору і натрію, кількість лейкоцитів та соматичних клітин. За маститу у
молоці зменшуються: всі складові компоненти молока, у тому числі вміст
лактози, калію, кальцію, фосфору. Молоко за маститів
набуває лужної реакції, погано зсідається під дією сичужного ферменту. Розрізняють 2 види
дослідження молока: 1) виявлення
субклінічного маститу у кожної конкретної корови, яке проводиться лікарем
ветеринарної медицини на фермі: димастиновою
пробою; лейкоцитарною
пробою; бромтимоловою
пробою; визначенням
хлор-цукрового числа; пробою з
відстоюванням; визначенням
соматичних клітин; за допомогою
спеціальних приладів. 2) виявлення
домішок маститного молока в загальному збірному надої за кількістю соматичних
клітин (мастопримом тощо). Це дослідження молока-сировини є обов’язковим на
молокопереробних підприємствах. 1. Димастинова
проба Робочий розчин
димастину готують розчиненням
Техніка
визначення. У заглиблення молочно-контрольної пластинки (рис. 81) відміряють
1 см3 досліджуваного молока та 1 см3 водного розчину димастину з масовою
концентрацією 5 % і розмішують скляною паличкою. Визначають колір і
консистенцію вмісту заглиблення. Оцінка результату.
Утворення щільного згустку яскраво-червоного кольору свідчить про
захворювання тварини на мастит. Наявність маси гелеподібної консистенції
оранжево-червоного кольору вказує на підозру захворювання на мастит. У разі відсутності
маститу, маса має однорідну рідку консистенцію, частіше оранжевого кольору. 2. Бромтимолова
проба Техніка
визначення. У заглиблення пластинки відміряють 5 см3 досліджуваного молока і
1 см3 спиртового розчину бромтимолового блакитного з масовою концентрацією
0,2 %. Визначають колір
умісту заглиблення. Оцінка результату.
Якщо молоко, отримане від корів, хворих на мастит, колір його змінюється від
темно-зеленого до темно-синього. Молоко, отримане від корів здорових,
забарвлюється в темно-зелений колір. 3. Лейкоцитарна
проба Техніка
визначення. 1. Нагрівають профільтроване через вату молоко до температури
60…65 °С і витримують упродовж 5 хв. 2. Відміряють 1
см3 у суху градуйовану пробірку. 3. Розміщують
пробірки симетрично в центрифузі і центрифугують упродовж 5 хв за 1200 об/хв.
4. Виймають
пробірки із центрифуги, відраховують кількість поділок з осадом. Оцінка результату.
У молоці, отриманому від здорових корів, цей осад займає не більше 1−1,5
поділки шкали пробірки. У молоці корів, хворих на мастит, об’єм осаду
збільшується. Із осаду готують
препарат, зафарбовують його метиленовим синім і проглядають під мікроскопом з
метою виявлення стрептококів і лейкоцитів. Під впливом лугу, лейкоцити
розчиняються із вивільненням дезоксирибонуклеїнової кислоти (речовина ядра).
Це спричинює гелеутворення у досліджуваній пробі молока. 4. Визначення
хлор-цукрового числа (ХЦЧ) За захворювання
корів на мастит відбуваються зміни і в складі молока – знижується масова
частка СЗМЗ, жиру, цукру, підвищується кількість сироваткового білка і
хлоридів. Між кількістю
молочного цукру і хлору існує певне співвідношення, яке назване хлор-цукровим
числом (ХЦЧ). Для визначення хлор-цукрового числа необхідно визначити у
досліджуваному молоці масову частку молочного цукру і хлору:
Оцінка результату.
У молоці, отриманому від здорових корів, ХЦЧ не перевищує 4, а у молоці
корів, хворих на мастит, доходить до 10−15. Прискорене
визначення. Для прискореного визначення хлоридів до 5 см3 розчину азотнокислого срібла (арґентуму) з масовою
концентрацією 1,5 %, що містить 2 краплі 10 % водного розчину
двохромовокислого калію з масовою концентрацією 10 %, приливають 1 см3
молока. Оцінка результату.
Молоко, отримане із хворих чвертей вимені корів, забарвлюється в жовтий
колір, що свідчить про вміст у ньому понад 0,15 % хлоридів. 5. Візуальний
метод виявлення соматичних клітин у збірному молоці за допомогою препарату
«Мастоприм» згідно з ГОСТ 23455 Виявлення
соматичних клітин у збірному молоці корів здійснюють візуальним методом і за
допомогою віскозиметра. Приготування
водного розчину препарату «Мастоприм»: Розчин, перед
використанням збовтують до рівномірного розподілу. Термін придатності розчину
– 1 доба за температури зберігання 10...20 ° С. Техніка
візуального визначення соматичних клітин. 1. У заглиблення пластинки вносять
1 см3 добре перемішаного досліджуваного молока. 2. Додають 1 см3
водного розчину препарату «Мастоприм» з масовою концентрацією 2,5 %. 3. Молоко з
препаратом перемішують дерев’яною, пластмасовою або скляною паличкою впродовж
10 с. Оцінка результату.
Одержану суміш із заглиблення пластинки за безперервного перемішування
піднімають паличкою вверх на 50−70 мм, потім, упродовж не більше 60 с,
оцінюють результати аналізу відповідно до вимог таблиці 89. Таблиця 89 Кількість соматичних клітин у молоці
6. Дослідження
молока від корів, хворих на мастит, за допомогою мастидину Метод полягає в
руйнуванні ядер клітин лейкоцитів поверхнево активними речовинами, що входять
до складу діагностичних препаратів, унаслідок чого змінюється консистенція
молока. Розчин мастидину з
масовою часткою 2 %, одержують розведенням розчину мастидину з масовою
часткою 10 % у 5 разів (до 100 см3 розчину мастидину з масовою часткою 10 %
доливають 400 см3 дистильованої води). Техніка
визначення. 1. У кожне заглиблення молочно-контрольної пластинки з
відповідної чверті вим’я надоюють по 1см3 молока і додають 1 см3 розчину мастидину з масовою часткою 2 %. Примітка: Якщо
досліджують молоко, здоєне з усіх чвертей вимені (ранішнє або вечірнє),
використовують розчин мастидину з масовою часткою 10 %. 2. Суміш молока з
реактивом перемішують паличкою впродовж 30 с за реакції з димастином і 15–20
с за використання мастидину. Оцінка результату.
Реакцію враховують за ступенем утворення желеподібного згустку та кольором. На пластинці
МКП-1: негативна реакція
– однорідна рідина (–); сумнівна реакція –
сліди утворення желе (±); позитивна реакція
– добре виражений згусток, що частково або повністю вилучається з луночки
молочно-контрольної пластинки паличкою під час перемішування (+). На пластинці
МКП-2: негативна реакція
– утворюється однорідна суміш (–); сумнівна реакція –
під час обертання пластинки на дні луночки помітні тонкі пластівці без
тенденції утворення згустку (±); позитивна реакція
– поява слабкого або тугого згустку, що швидко утворюється і, під час
обертання, збирається у центрі луночки (+). За кольором
суміші: світло-фіолетовий,
сірий – рН молока у межах норми; майже білий –
підвищена кислотність; темно-фіолетовий –
підвищена лужність молока.
7. Дослідження молока
від корів, хворих на мастит, пробою відстоювання Для такої проби
використовують молоко, що дало позитивну реакцію з димастином або мастидином. Техніка
проведення. 1. У пробірку наливають по 10–15 см3 молока, одержаного з кожної
чверті молочної залози, і переносять його на 16–18 год у холодильник за
температури 4...10 °С. 2. Після
закінчення цього терміну враховують результати. Оцінка результату.
Молоко здорових корів має білий або злегка синюватий колір, без осаду. У
молоці корів, хворих на мастит, на дні пробірки утворюється осад. У деяких
випадках молоко стає водянистим, з невеликим шаром вершків, які можуть бути
тягучими. Якщо висота осаду у відстояному молоці 0,1 см3 і більше або наявні
пластівчасті тягучі вершки –результат проби позитивний. 9.21. Визначення крові та гною у молоці Поява у молоці
корів гною та крові є наслідком дії багатьох чинників: ударів, порізів, інших
пошкоджень вимені, а також перебігу захворювань –інфекційних (туберкульоз),
паразитарних (гемоспоридіоз), незаразних (мастити). Найпростішим способом
виявлення крові у молоці є метод центрифугування та постановка бензидинової
проби. Техніка визначення
(бензидинова проба). 1. У пробірці з 2 см3 розчину спирту-ректифікату з
масовою часткою 96 % і 2 см3 розчину пероксиду водню з масовою часткою 3 %
розчиняють невелику кількість бензидину. 2. Після
енергійного струшування додають 3−4 краплі льодової оцтової кислоти і
вносять 4−5 см3 досліджуваного молока. 3. Ретельно
перемішують уміст пробірки. Оцінка результату.
Поява через 20−30 хв у пробірці темно-синього забарвлення характеризує
позитивну реакцію. ІІ варіант
(центрифугування): 1. У пробірку
наливають досліджуване молоко з температурою 40...50 °С, щільно закривають корком і центрифугують упродовж
10 хв за 1000 об/хв. Оцінка результату.
Поява на дні пробірки осаду рожевого забарвлення або жовтого з рожевим
обрамленням навколо – показник позитивної реакції. 9.22. Кількісна реакція на бруцельоз Техніка
визначення. 1. У пробірку діаметром 5–8 мм градуйованою піпеткою відмірюють 1
см3 молока і 1 краплю кольорового бруцельозного антигену (змив культури
бруцел, забарвлених гематоксиліном). 2. Пробірку з
умістом поміщають у термостат за температури 37 °С на 40–45 хв. Оцінка реакції.
Позитивна – поява синього кільця в верхньому шарі рідини; Сумнівна – слабо
забарвлене синє кільце; Негативна –
рівномірне забарвлення вмісту пробірки. Реакцію ставлять
за підозри, що молоко отримане від корів, хворих на бруцельоз. 9.23. Мікробіологічні дослідження молока і
молокопродуктів Молоко містить
багато цінних поживних речовин, зокрема, казеїн, альбуміни, молочний цукор,
вітаміни тощо, що є сприятливим середовищем для розвитку мікроорганізмів.
Проте, молоко не є першоджерелом мікроорганізмів. Кров, із складників якої у
вимені синтезується молоко, не є джерелом контамінації його мікроорганізмами. Основна маса
мікроорганізмів потрапляє в молоко у процесі його отримання. Щоб зберегти
високий ґатунок молока і забезпечити його відповідність стандартам,
доводиться вирішувати низку проблем, які можна розділити на наступні
категорії: термостійкі бактерії (бактерії, що не гинуть після пастеризації),
бактерії групи кишкової палички, психрофільні бактерії, що розвиваються за
температури 15 °С, псування молока, розповсюдження через молоко збудників
інфекційних захворювань, визначення інгібіторів у молоці (антибіотиків і
залишків дезінфікуючих засобів). Пастеризацією
сирого молока на підприємстві знищується більшість мікроорганізмів. Мікрофлору молока
поділяють на ту, що утворюють кислоту; протеолітичні; а шляхи її потрапляння
мікроорганізмів в молоко – шкіряний покрив, ґрунт, молочний посуд, гній та
ін. Серед мікрофлори
молока важливе значення мають представники родин: Lactobacteriaceae, Pseudomonadaceae, Micrococcaceae, Bacilliaceae, Enterobacteriaceae, Corinebacteriaceae. Представниками
родини Pseudomonadaceae, роду Pseudomonas є Ps. fluorescens, Ps. fragi, Ps. viscosa та інші, які зумовлюють появу дефектів молока. До родини Micrococcaceae, роду Micrococcus належить, зокрема, Microc. pyogenes, який продукує токсин. Вони надзвичайно резистентні й
здатні розвиватися у вимені. Крім мікрококів, у вимені зустрічаються
стрептококи кишкового походження. Із представників
родини Bacilliaceae, роду Bacillus, зустрічаються такі види, як: Bac. cereus, Bac. coagulus, також Enterobacteriacea, роди Escherichia, Salmonella, Рroteus. Нормальна
мікрофлора молока 1. Молочнокислі
бактерії: а) стрептококи – Str. lactis, оптимальна температура – 30...37 °С. Викликає
максимальну кислотність – до 120 °Т (близько 0,9% молочної кислоти внаслідок
зброджування 1% лактози). Str. cremoris – розвивається за дещо нижчої кислотності порівняно
із Str. lactis. Str. mastitidis (agalactiae) – не згущає молоко, зброджує сахарозу і крохмаль. Str. citrovorum, Str. paracitrovorum – зброджують лимонну кислоту і молоко, утворюють леткі
кислоти з невеликою кількістю діацетилену, що надає продукту специфічного
запаху; б) лактобактерії –
паличкоподібні бактерії, довгі палички, порівняно зі Str. lactis у них більше виражені анаеробні властивості. Більш
типовою є Lactobact. casei, Lactobact. bulgarium, які належать до роду Thermobacterium, що свідчить про їхню здатність розвиватися за
підвищеної кислотності. Зниження
активності молочнокислих бактерій є досить поширеним явищем. Необхідно
розрізняти тимчасове зниження активності цих бактерій і повне, коли
активність відновити неможливо. Дуже часто втрата
активності молочнокислих бактерій пов’язана з дією бактеріофага, який
викликає лізис клітин. Для підтримання
активності молочнокислих бактерій, їх необхідно висівати у молоко з дріжджами
і залишати у такому стані на тривалий час. Слабка активність
розвитку молочнокислих бактерій, особливо стрептококів, часто зумовлюється
властивостями молока, в якому вони культивуються. 2. Бактерії групи кишкової
палички. Містяться в сирому молоці й гинуть у пастеризованому. Від
молочнокислих бактерій вони відрізняються тим, що: а) зброджують
молоко повільно (через 3–4 доби); б) разом з
молочною, оцтовою, пропіоновою, масляною кислотою утворюється незначна
кількість етилового спирту; в) на відміну від
молочнокислих бактерій, завжди утворюється велика кількість газу (СО2,
водню). Ця група мікроорганізмів надає молоку неприємного запаху. Наявність
бактерій цієї групи свідчить про фекальне його забруднення. Мікрококи часто
зустрічаються у вимені корови, тому їх виділяють із свіжовидоєного молока.
Вони утворюють таку кількість молочної кислоти, якої недостатньо для згущення
молока. Завдяки наявності
в мікрококах протеолітичних ферментів, вони викликають розпад білків
(пептонізацію молока). За суворого
дотримання санітарних правил, у молоці переважають мікрококи і невелика
кількість молочнокислих стрептококів (ентерококів). Психрофільні
бактерії. До них належать Bact. fluorescens ligbefaciens, Pseudomonas, які розвиваються за температури 0...30 °С. Під час
пастеризації вони повністю знищуються. Якщо Pseudomonas виявлено після пастеризації, це свідчить про
забруднення після пастеризації. Маслянокислі
бактерії: Bac. putrificum, Bac. botulinum amylibacter. На склад мікрофлори
молока впливають умови утримання корів. Під час стійлового утримання
переважають бактерії групи кишкової палички та маслянокислі бактерії, під час
утримання на пасовищі – мікрококи і молочнокислі бактерії. Дефекти молока Гіркий смак часто
з’являється під час тривалого зберігання молока за низьких температур. Він
викликається психрофілами, найчастіше – флуоресціюючими. Ці бактерії
викликають протеоліз казеїну, внаслідок чого накопичуються пептони. Подібні
речовини можуть накопичуватися за розвитку бактерій Coli aerogens і Torula amara. Гіркий смак молока може викликати Bruc .abortus, оскільки він виділяє фермент ліпазу, що розщеплює
жир. Запах хліву
свідчить про наявність у молоці Bac. coli. Мильний смак
молока зумовлюють Bac. lactis gaponacei. Слизисте або
тягуче молоко свідчить про наявність у ньому Bac. lactis viscosum, Str. cremoris, Str. thermophilus. Причиною цього є те, утворення муцинів у молоці. Розмноження
бактерій у видоєному молоці залежить від початкової кількості бактеріофага і
температури зберігання. За підвищення кислотності прискорюється розмноження
бактерій у молоці. За низької температури (0°), упродовж першої
доби спостерігається незначне зменшення кількості бактерій, після чого
починається їх розмноження. За 0° упродовж 3-х днів кількість бактерій підвищується дуже
повільно, а потім зростає. Послідовність фаз
мікрофлори молока під час його зберігання: Бактерицидна фаза. Фаза змішаної
мікрофлори (тривалість – до 12 год). Фаза молочнокислих
стрептококів. Фаза грибної
мікрофлори. Через молоко
можуть передаватися такі захворювання, як: мастит, бруцельоз, лістеріоз,
сальмонельоз, холера, туберкульоз, лептоспіроз та ін. Методи
мікробіологічного контролювання молока і молочних продуктів згідно з ДСТУ
7357:2013 Згідно з ДСТУ 7357 проводять контролювання
сторонньої мікрофлори у таких продуктах: ● молоко (вершки) – сировина,
продукти перероблення молока (знежирене молоко, маслянка, сироватка), молоко
(вершки) термічно оброблене (пастеризоване, стерилізоване, УВТ-оброблене
тощо), кисломолочні та молочні (десерти, пасти, напої, коктейлі, соуси тощо)
продукти; ● молоко сухе, незбиране та
знежирене, сухі вершки, сухі продукти перероблення молока (маслянка,
сироватка), молочні суміші, сухі кисломолочні продукти, сир; ● білкові концентрати (казеїни,
казеїнати, казецити тощо), таблеткові продукти та продукти в капсулах,
молочний цукор, молочно-овочеві, молочно-фруктові пюре, замінники незбираного
молока, молочні коктейлі тощо; ● молоко (вершки) згущене (-і) з
цукром і без нього та зі смаковими наповнювачами і без них, згущене (-і)
стерилізоване молоко (вершки), сироватка та маслянка, концентроване
стерилізоване молоко (вершки) та інші подібні до них продукти; ● сир (кисломолочний, твердий,
напівтвердий, м’який, розсільний, плавлений, пастоподібний, свіжий), сиркові
вироби та напівфабрикати, сир для плавлення тощо; ● масло вершкове та топлене, спреди,
суміші жирові тощо; ● продукти молочні заморожені,
зокрема морозиво, торти і рулети сиркові та з морозива; ● закваски сухі та рідкі,
бактеріальні концентрати, бактеріальні препарати прямого внесення тощо. 1. Методи
відбирання проб молока та молочних продуктів Проби для
мікробіологічного контролювання відбирають асептично, перед відбиранням проб
для фізико-хімічних та органолептичних досліджень. Порядок приймання та
відбирання проб продуктів повинен відповідати вимогам ДСТУ 4834, ДСТУ ІSО 707, ДСТУ ISО 2859-1 та ГОСТ 13928. Відібрана проба
продукту повинна бути достовірною, непошкодженою та незабрудненою під час
зберігання та (або) транспортування. Щоб контролювати якість продукту за
мікробіологічними показниками, незалежно від розміру партії, роблять з неї
вибірку обсягом: • 2 паковальні
одиниці транспортної тари з ваговим продуктом або продуктом у спожитковому
пакованні (за винятком продуктів, що зазначені нижче); • 3 одиниці
спожиткового паковання таблеткових продуктів та продуктів у капсулах; • 5 одиниць
спожиткового паковання стерилізованих продуктів; • 4 одиниці
спожиткового паковання бактеріальних препаратів прямого внесення; • 15 одиниць
спожиткового паковання бактеріальних концентратів; • 100 одиниць
спожиткового паковання сухих заквасок; • 15 одиниць
спожиткового паковання рідких заквасок; • 2 головки сиру
(твердого, напівтвердого, м’якого, розсільного, сиру для плавлення тощо); • з кожної
цистерни або секції – від 0,5 дм3 до 1,0 дм3. Якщо маса проби
продукту дорівнює масі продукту в спожитковому пакованні, що потрапила до
вибірки, – її вміст використовують повністю. Якщо маса продукту
в спожитковому пакованні менше маси проби, – її формують із кількох одиниць
продуктів спожиткового паковання з однієї партії або з однаковим кодом. Від продукту в
транспортному або спожитковому пакованні, вага якого більше маси проби,
відбирають точкові проби з різних місць, різної глибини й поверхневих шарів в
одну, або кожну пробу в окрему ємність. Потрібно відбирати
дві паралельні проби, а якщо того вимагає законодавство або угода між
зацікавленими сторонами, дозволено відбирати і більшу кількість проб. Проби для
мікробіологічного контролювання відбирають: 1. У стерильний
посуд, використовуючи стерильне устатковання, та накривають стерильними
накривками. 2. Посудина для
проб має бути така, щоб її можна було повністю заповнити пробою, щоб
запобігти сколочуванню під час транспортування, та давала змогу перемішати
пробу перед контролюванням. Стерилізувати приладдя та устатковання для
мікробіологічного контролювання необхідно витримуванням: 1. у сушильній
шафі – за температури від 170 ºС до 175 °С упродовж (2±0,5) год; 2. в автоклаві – за температури (121±1) °С
не менше, ніж 20 хв; 3. над полум’ям спиртівки або газового
пальника – упродовж від 1 до 2 с усіх робочих поверхонь устатковання; 4. занурюванням у розчин етанолу
концентрацією не менше, ніж 70 %; 5. занурюванням у етанол концентрацією 96
% та наступним фламбуванням; 6. пропарюванням,
кип'ятінням або хлоруванням з наступним ополіскуванням питною водою (металеві
трубки або пробник, у разі відбирання проб сирого молока для визначання
редуктази). Приладдя, що
використовують для відбирання проб, має бути виготовлене з нержавіючої сталі
або іншого матеріалу, інертного до проби. Матеріали мають бути дозволені до
застосування в харчовій промисловості центральним органом виконавчої влади у
сфері охорони здоров’я. Примітка. Не
дозволено застосовувати несправне або забруднене устатковання. Відбирання проб
для мікробіологічних досліджень повинна проводити особа, що має досвід з
проведення мікробіологічних досліджень. Відбирають проби
молока та молочних продуктів для мікробіологічного контролювання залежно від
виду продукту. Кількість проби
молока та молочних продуктів має бути не менша, ніж 200 см3 або У разі формування
об'єднаної проби продукту у спожитковому пакованні, його перемішують,
перевертаючи паковання не менше, ніж п'ять разів до отримання достатньої
однорідності, нагрівають до температури (32±2) ºС на водяній бані та
охолоджують до температури (20±2) ºС. Знежирені продукти не нагрівають.
Поверхню спожиткового пакування, перед відкриванням, необхідно обробити
спиртом (концентрація не менше, ніж 70%). Потім усі відібрані спожиткові
паковання відкривають і продукт зливають в одну ємність, отримавши об’єднану
пробу, яку необхідно перемішати. Посуд з об’єднаною пробою закривають. Від продуктів
різної консистенції пробу відбирають так, щоб до неї ввійшли всі компоненти у
співвідношенні, в якому вони перебувають у продукті. Для того, щоб
забезпечити однорідність проби та запобігти розшаруванню складників, її
необхідно відбирати відразу після перемішування, Якщо одержати
необхідну однорідність важко, проби потрібно відбирати з різних частин
ємності з продуктом у кількості, що забезпечить загальний обсяг маси проби не
менше, ніж Пробовідбірник
пропускають крізь продукт, занурюючи його до дна тари. У разі потреби, тару
нахиляють або кладуть на бік. Коли пробовідбірник досягне дна тари, його
обертають на 180º, витягають і переносять його вміст у посудину для
проби. Таку процедуру повторюють стільки разів, щоб одержати пробу масою не
менше, ніж 1.1. Відбирання проб
молока незбираного, знежиреного, маслянки, сироватки, замінників незбираного
молока та інших рідких продуктів, подібних до них Поверхню
спожиткового паковання з вибірки, перед відкриванням, необхідно обробити
спиртом (концентрація не менше, ніж 70%). Щоб отримати об'єднану пробу,
продукт у спожитковому пакованні перемішують, не порушуючи цілісності
паковання, перевертаючи його не менше, ніж п’ять разів. Нагрівають до
температури (32±2) ºС на водяній бані та охолоджують до температури
(20±2) ºС. Знежирені продукти не нагрівають. Посуд з об’єднаною пробою
закривають. 1.2. Відбирання
проб вершків сирих та пастеризованих, густих та напівгустих молочних
продуктів (сметани, десертів, паст та інших продуктів, подібних до них) Не розфасовані
вершки ретельно перемішують мішалкою або колотівкою, чергуючи вертикальні та
обертальні рухи з дна контейнера до верхніх шарів упродовж 1 хв, після чого
відбирають пробу. Щоб уникнути
утворення піни, збивання або утворення масла, диск колотівки між зануреннями
не піднімають над поверхнею вершків. Відбирання
точкових проб вершків для складання об’єднаної проби виконують відповідно до
чинного стандарту. Пробу сметани у
флягах відбирають трубкою, черпаком або щупом відповідно до чинного
стандарту. Об’єднану пробу
продуктів у спожитковому пакованні, з якого складається вибірка, готують
відповідно до чинного стандарту. 1.3. Відбирання
проб рідких кисломолочних продуктів (кефіру, ряжанки, йогуртів та інших
продуктів, подібних до них) Рідкі кисломолочні
продукти у спожитковому пакованні перемішують, не відкриваючи його та
перевертаючи паковання не менше п’яти разів. Густіші продукти перемішують у
відкритому пакованні впродовж 1 хв шпателем, ложкою тощо. Порядок відбирання
проб із гомогенного продукту викладено вище. 1.4. Відбирання
проб сиру кисломолочного, альбумінного, виробів сиркових, напівфабрикатів,
сирної маси для плавлення, білкових концентратів та інших продуктів, подібних
до них Перед відбиранням
проби не розфасованого продукту, з транспортного паковання відкидають верхній
шар продукту висотою від Переносять
стовпчик у ємність для проб і ретельно перемішують, готуючи об’єднану пробу. Для формування
об’єднаної проби продукту у спожитковому пакованні, зі сформованої вибірки
відібраний продукт звільняють від паковання. 1.5. Відбирання
проб сиру (твердого, напівтвердого, м’якого, розсільного, сиру для плавлення
тощо) Поверхню сиру,
навколо місця відбирання проби, дезінфікують спиртом (концентрація не менше,
ніж 70%). Перед взяттям стовпчика, відбирають його короткий стовпчик
діаметром від Точкові проби сиру
відбирають щупом із двох протилежних сторін кожної головки сиру, взятих для
вибірки. Від отриманих у
такий спосіб стовпчиків сиру відрізають (1,5±0,2) см його верхньої частини і
потім використовують для закривання отвору. Нижню частину стовпчиків довжиною
(4,5±0,5) см переносять у посуд для формування проби. У разі відбирання
точкових проб з дрібних сирів, щуп уводять, відступивши від однієї з основ
головки сиру на 1/3 найбільшого виміру головки. Від вийнятих стовпчиків сиру
відрізають по (1,0±0,5) см верхньої частини стовпчика, який потім
використовують для закривання отвору. Нижню частину стовпчиків переносять у
ємність для складання об’єднаної
проби. Якщо стовпчик потрібен як поверхнева проба, його негайно
переміщують у контейнер для проб. Потім уводять щуп меншого діаметра і
достатньої довжини через внутрішню поверхню отвору від витягнутого стовпчика.
Щуп прокручують на один повний оберт і виймають разом зі стовпчиком продукту.
Верхню частину стовпчиків сиру з поверхневим шаром повертають на колишнє
місце, а поверхню сиру заливають розплавленим полімерно-парафіновим сплавом
для покривання сирів. Проби розсільного
сиру відбирають частинами, маса кожної з них (100±10) г (без розсолу, олії
тощо). Для складання
об’єднаної проби м’яких та розсільних сирів використовують увесь стовпчик
сиру, відібраний щупом. Від батона
ковбасного сиру точкові проби відрізують ножем поперек, на відстані близько Від плавлених
сирів усіх видів у спожитковому пакованні, відібраних до вибірки, точкові
проби відбирають ножем рівномірно з різних частин кожної одиниці спожиткового
паковання і переносять у посуд для складання об'єднаної проби. Від плавленого
сиру в брикетах масою 1.6. Відбирання
проб морозива, тортів і рулетів сиркових та з морозива, заморожених
напівфабрикатів та подібних до них продуктів Відбирають проби
ложкою, пінцетом або іншим приладдям залежно від виду та розміру шматків
продукту. Відбирають точкові
проби вагового продукту зі сформованої вибірки, попередньо підігрітими до
температури (30±5) °С щупом, ложкою, ножем або шпателем. Знімають поверхневий
шар продукту висотою Заморожені сир
кисломолочний, сиркові вироби, напівфабрикати, перед відбиранням проб,
залишають за кімнатної температури до повного розморожування. Проби згідно з
пунктом 1.5, відібрані як від вагового продукту у транспортній тарі, так і
від продукту у спожитковому пакованні, обов’язково розтирають у ступці або змішувачем, до отримання однорідної консистенції. З усієї довжини
щупа стерильним шпателем знімають шар морозива і переносять його у ємність.
Пробу морозива залишають за температури (18±4) ºС або витримують на водяній бані до повного
відтанення. Морозиво в
спожитковому пакованні, що надійшло до вибірку, звільняють від паковання,
після чого кладуть у ємність до повного відтанення за температури (18±4) °С. Проби сухих
напівфабрикатів для морозива (концентрати, суміші для морозива та інші
подібні до них продукти) відбирають згідно з вище вказаним. 1.7. Відбирання
проб згущеного молока (зокрема, стерилізованого) та вершків, сироватки,
сколотин, молочних концентратів та інших продуктів, подібних до них Перед відбиранням
проб продукту у цистернах, бочках, флягах тощо, їх перемішують чистою
стерильною мішалкою впродовж (2±1) хв, а в спожитковому пакованні – чистим
стерильним шпателем. Якщо у продукті є
осад, продукт у спожитковому пакованні нагрівають на водяній бані за
температури (55±5) °С, не допускаючи підвищення температури продукту вище,
ніж 30 °С, і знову перемішують до отримання однорідної маси, потім
охолоджують його до (20±2) °С. Занурюючи пробник,
щуп або ложку до дна тари, відбирають пробу продукту, переносять в одну
ємність, перемішують, отримуючи у такий спосіб об’єднану пробу. 1.8. Відбирання
проб сухого молока, сухих молочних продуктів (сухої сироватки, сухих молочних
білкових продуктів та інших продуктів, подібних до них), таблеткових
продуктів та продуктів у капсулах, молочного цукру, харчового та технічного
казеїну Відбирання проб
продукту (крім таблеткових продуктів та продуктів у капсулах) у тарі або
пакованні, що становлять вибірку, виконують щупом, пробником або ложкою з
різних частин кожної одиниці тари. Точкові проби переносять у ємність та ретельно
перемішують. Щуп на відстані
(3±1) см від стінки паковання занурюють у продукт до дна тари за діагоналлю
відносно протилежної стінки. Точкові проби
таблеткових, гранульованих продуктів та продуктів у капсулах відбирають
пінцетом або ложкою і переносять в один посуд. Продукти в капсулах звільняють
від них. Для того, щоб
отримати об’єднану пробу, точкові проби таблеткових, гранульованих продуктів
та продуктів, вивільнених з капсул, подрібнюють у ступці лабораторним млином
або блендером. 1.9. Відбирання
проб вершкового масла, спредів та продуктів, подібних до них (пластичних
вершків, стерилізованого та топленого масла, сумішей жирових) Точкові проби від
вагового продукту, залученого до вибірки, відбирають щупом. Якщо продукт у
бочці, щуп занурюють під кутом у напрямі від краю бочки до центра, якщо в
ящику – за діагоналлю від торцевої стінки до центра моноліту продукту. Для того, щоб
отримати об'єднану пробу, від нижньої частини стовпчика продукту, взятого
щупом з кожної одиниці транспортної тари, відбирають ножем точкову пробу
масою (50±5) г і переносять у ємність для складання об’єднаної проби. Верхню частину
стовпчика продукту, що залишилася у щупі, повертають на колишнє місце й
акуратно вирівнюють поверхню продукту. Примітка. За температури
продукту нижче, ніж 10 ºС, пробу відбирають щупом, профламбованим
безпосередньо перед узяттям проби. Для того, щоб
проаналізувати продукт у спожитковому пакованні, маса нетто якого не
перевищує Об’єднану пробу
продукту в брикетах масою Отриману об’єднану
пробу продукту поміщають на водяну баню, нагрівають до температури (30±2)
ºС та постійно перемішують до отримання розм’яклої маси. 1.10. Відбирання
проб заквасок сухих та рідких, бактеріальних концентратів, бактеріальних
препаратів прямого внесення Вибірку для
контролювання якості кожної партії продукту формують згідно з чинним
стандартом. Об’єднану пробу
готують, змішуючи разом від: ● 30 до 50
одиниць спожиткового паковання (контейнерів/пакетів) заквасок сухих; ● 3 до 5
одиниць спожиткового паковання (контейнерів/пакетів) бактеріальних
концентратів і бактеріальних препаратів прямого внесення. Для того, щоб
отримати об’єднану пробу заквасок рідких, точкові проби відбирають стерильною
піпеткою об’ємом, не менше, ніж 10 см3 з кожного паковання та переносять в
одну ємність. Маса проби для
контролювання заквасок сухих, бактеріальних концентратів, бактеріальних
препаратів прямого внесення має бути (30±2) г. Кожна проба для
контролювання заквасок рідких має становити (50±5) см3. 2. Марковання,
транспортування та зберігання проб Проби продукту,
відібрані лабораторією підприємства-виробника, контролюють на цьому ж
підприємстві; проби забезпечують етикеткою, де зазначають: − повну назву та ґатунок продукту (за
наявності); − номер проби; − номер та обсяг партії; − час та дату відбирання проби; − посаду та підпис особи, яка відбирала
пробу; − позначення нормативного документа (для
готового продукту). Проби продукту,
направленого для контролювання в інші лабораторії, забезпечують етикеткою та
актом відбирання проб, де зазначають: − повну назву та дату виготовлення продукту; − назву підприємства-виробника; − номер та обсяг партії; − місце відбирання проб; − температуру продукту на момент відбирання
проби; − умови зберігання продукту на момент
відбирання проби; − час і дату відбирання проби; − назву показників, які потрібно визначити в
продукті; − позначення
чинного нормативного документа (для готового продукту); − посаду і підпис особи, яка відбирала пробу. Проби продукту
потрібно доставити в лабораторію не пізніше, ніж через 2 год після їх
відбирання. До початку
контролювання, в лабораторії пробу зберігають у холодильнику за температури
(4±2) °С. Мікробіологічне
контролювання продукту виконують не пізніше, ніж через 4 год з моменту
відбирання проби. Примітка. В
окремих випадках час доставки проби в лабораторію може бути подовжено до 4
год, але це необхідно зазначити в акті відбирання проб та пояснити причину
затримки. Під час
транспортування, проби потрібно зберігати за наступних температурних режимів,
для: − продуктів, що швидко псуються, – (4±2) °С,
підморожування – недопустиме; − морозива та напівфабрикатів – мінус (4±2)
°С. 3. Підготування
посуду та матеріалів Увесь новий посуд
(крім одноразового) для мікробіологічного контролювання кип’ятять у
підкисленій воді (розчин хлористоводневої кислоти з об’ємною часткою (1–2) %
упродовж (15±2) хв, миють до повного вилучення мийних засобів та інших
сторонніх речовин і сушать у сухо-жаровій шафі за температури 100 °С. Підготовлений
посуд стерилізують у сушильній шафі за температури 160 ºС упродовж 2
год, або 180 °С – 1 год, чи парою в автоклаві за температури (128±1) ºС
упродовж 1 год з наступним досушуванням у сушильній шафі, якщо в автоклаві
немає вакуумної сушарки. Чашки Петрі,
піпетки стерилізують загорнутими в папір або в металевих пеналах. У верхній
кінець піпетки заздалегідь вкладають шматочок вати. Нові гумові корки
кип’ятять упродовж 30 хв у розчині двовуглекислого натрію з масовою часткою 2
% і 5 разів промивають водопровідною водою (кип’ятіння та промивання
повторюють двічі). Гумові корки, використовувані раніше, після знезараження
кип’ятять 30 хв у водопровідній воді з нейтральним мийним засобом, промивають
у дистильованій воді, сушать і зберігають до використання. Стерильний посуд
зберігають у щільно закритих шафах або ящиках із накривками за температури
(20±2) ºС й за відносної вологості повітря не більше, ніж 80 %. Термін зберігання стерильного
посуду – не більше, ніж 30 діб. У разі
застосування одноразового пластикового посуду, перевіряють цілісність
пакования та термін придатності до використання. 4. Готування проб
до контролювання Молоко, вершки,
продукти перероблення молока (знежирене молоко, маслянка, сироватка), молоко
(вершки) термічно оброблене (пастеризоване, стерилізоване, УВТ-оброблене
тощо). Відібрані проби,
перед дослідженням, ретельно перемішують, щоб отримати гомогенну суспензію
мікроорганізмів. Необхідно уникати утворення піни. Інтервал між
перемішуванням і перенесенням дослідної проби не повинен перевищувати 3 хв.
Для контролювання, стерильною піпеткою відбирають 10 см3 продукту в стерильну
пробірку або колбу. Кисломолочні напої
і продукти, рідкі закваски Відібрані проби,
перед дослідженням, перемішують та нейтралізують. Для цього у стерильну
пробірку або колбу відбирають стерильною піпеткою 10 см3 продукту або
закваски, що аналізують, додають 1 см3 стерильного розчину двовуглекислого
натрію з масовою концентрацією 100 г/дм3, уміст посудини перемішують. Заморожені молочні
продукти (морозиво, торти і рулети сиркові та з морозива) Готують проби, як
зазначено вище, застосовуючи водяну баню для того, щоб отримати температуру
дослідної проби в межах (37±1) °С. Сир (кисломолочний,
твердий, напівтвердий, м'який, розсільний, плавлений, пастоподібний та
свіжий), сиркові вироби та напівфабрикати, сировина для плавленого сиру Із проби,
відібраної вище, асептично зважують Вершкове масло,
спреди, суміші жирові Зважують Згущені молоко
(вершки) з цукром та без нього та зі смаковими наповнювачами та без них,
згущені стерилізоване молоко (вершки), сироватка та маслянка, концентроване
стерилізовано молоко (вершки) Паковання з
продуктом ретельно миють щіткою в чистій теплій воді й витирають. Перед
відкриванням, накривку банок, верхню поверхню паковань, чопів бочки та
частину поверхні навколо чопа протирають спиртом та фламбують. Відкривають банки
стерильним ножем, а чіп бочки та поверхню паковань – стерильним пробійником.
Отвори, що утворилися, відразу закривають стерильним пергаментом,
профламбованою жерстяною накривкою або накривкою чашки Петрі. Вміст паковання
ретельно перемішують стерильною ложкою або шпателем. Зважують стерильний сухий
посуд і вносять туди Сухе молоко та
сухі продукти перероблення молока (незбиране та знежирене молоко, вершки,
маслянка, сироватка, молочна суміш, кисломолочний продукт, сир), білкові
концентрати (казеїни, казеїнати, казецити тощо), таблеткові продукти та
продукти в капсулах, молочний цукор, молочно-овочеве пюре, замінники
незбираного молока, закваски, бактеріальні концентрати, бактеріальні
препарати прямого внесення Ретельно
перемішують уміст закритої посудини періодичними обертанням та струшуванням.
Якщо дослідна проба розміщена у закоркованій та занадто повній посудині, що
не дає змоги ретельно перемішати вміст, її асептично переносять в іншу,
більшу стерильну посудину, перемішують. Відкривають посудину, беруть наважку
продукту масою Готування
розведень продуктів для висівання Безпосередньо
перед висіванням готують десятиразові розведення продукту в стерильних
розчинах хлориду натрію, пептонно-сольового розчину, розчину пептону,
цитринового натрію (для сирів) або фосфатного буфера. Із проб молока,
вершків, сметани, кисломолочних продуктів, морозива, масла, стерильною
піпеткою відбирають 10 см3 і вносять у 90 см3 стерильних розчинів хлориду
натрію, хлориду натрію з пептоном чи фосфатного буфера. Отримують розведення
1:10. Пробу масла чи
морозива вносять у розчин хлориду натрію чи хлориду натрію з пептоном, чи
фосфатного буфера. Температура проби та розчинів для розведень має бути від
40 до 45 °С. До підготовлених
наважок сиру кисломолочного, сиркових виробів, згущених молочних консервів і
сухих молочних продуктів додають 90 см3 стерильних розчинів для розведення,
збовтують упродовж (4±2) хв до гомогенного стану. У разі використання
змішувачів, до наважки додають 90 см3 розчинника. Перемішують 1–3 хв.
Температура диспергування має становити (45±1) °С. Чекають, доки осяде піна.
Отримують розведення 1:10. 3 першого
розведення (1:10) готують наступні розведення – 1:100, 1:1000 тощо. Для приготування
кожного розведення беруть нову стерильну піпетку або, у разі застосування
автоматичної піпетки, – стерильний наконечник. У разі висівання в чашки Петрі
посівний матеріал уносять, починаючи з вищого розведення. У цьому разі
дозволено використовувати одну піпетку або один наконечник автоматичної
піпетки. Для контролювання
дозволено висівати пробу на чашки Петрі з одного і того ж розведення об’ємом
1 см3 або 0,1 см3. Перед початком
мікробіологічного контролювання розтоплюють потрібну кількість середовища й
охолоджують до температури (45±1) ºС. Поживний агар
заборонено тримати в розтопленому стані більше, ніж 8 год. Агар, що залишився, повторному розплавленню не
підлягає. Після затвердіння
поживного середовища, чашки Петрі перевертають накривками донизу, ставлять у
такому положенні в термостат штабелями висотою не більше, ніж 6 одиниць.
Штабелі не повинні торкатися один одного, стінок та верху термостата. Для того, щоб
упевнитися в стерильності поживного середовища, для контролювання додатково
готують чашку Петрі з 12 см3 відповідного середовища без посівного матеріалу
та інкубують її разом із пробами. Для того, щоб
отримати достовірні результати, готують дві паралельні проби, з яких
засівають не менше, ніж три послідовних розведення. 5. Визначання
кількості мезофільних аеробних і факультативно-анаеробних мікроорганізмів
(КМАФАнМ) Суть методу. Метод
ґрунтується на здатності мезофільних аеробних і факультативно-анаеробних
мікроорганізмів розмножуватися на селективних твердих поживних середовищах за
температури (30±1) °С упродовж 72 год. 5.1. Проведення
випробування Вибирання
розведень для висівання. Кількість продукту, який використовують для
висівання, визначають за ступенем вірогідного мікробного забруднення
відповідно до чинних нормативних документів на продукти або сировину. Для
того, щоб отримати достовірні результати, розведення має бути таким, щоб
забезпечити утворення від 10 до 150 колоній на одній чашці. Висівання. Чашки
Петрі, перед висіванням, маркують, указуючи номер проби та розведення. В одну
чашку засівають одне розведення. Після внесення
посівного матеріалу, в кожну чашку Петрі додають (10–15) см3 розплавленого й
охолодженого до температури (40...45) °С поживного середовища 1 та 2. Для
контролювання сирого, стерилізованого та НВТ молока, застосовують середовище
3 для підрахування колоній у молоці. Інокулят та поживне середовище ретельно
перемішують легкими коловими похитуваннями для рівномірного розподілу
посівного матеріалу в середовищі. Вирощування.
Проміжок часу від закінчення готування проби продукту до змішування дослідної
проби з середовищем не повинен перевищувати 15 хв. Засіяні чашки
залишають за температури (18±2) °С на чистій горизонтальній поверхні для
утворення гелю. Термостатують за температури (30±1) ºС упродовж (72±2)
год. 5.2. Опрацювання
результатів. Підраховування
колоній. Підраховують колонії в чашках Петрі, які містять їх не більше, ніж
300. Щоб полегшити підраховування колоній, можна використовувати лупу або
прилад для підраховування колоній. Треба уникати помилкового сприйняття
частинок осадженої речовини в чашках за колонії. Злиті колонії
розглядають як одну колонію. Якщо такий характер росту спостерігають менше,
ніж на одній чверті чашки, – підраховують колонії на вільній частині чашки й підраховують
їх відповідну кількість для всієї чашки. Якщо злиті колонії займають більше
однієї чверті чашки, – таку чашку бракують. Підраховують
кількість колоній мікроорганізмів у кожному з паралельних посівів одного
розведення. За результатами визначають середньоарифметичне значення кількості
колоній у посівах одного розведення або вихідної проби. Під час
підраховування враховують кратність розведення проб. Результат
виражають у колоніє-утворювальних одиницях (КУО) в 1 см3 досліджуваної проби
і заносять до протоколу. Остаточним
результатом є кількість колоній в одній чашці, якщо по-іншому підрахувати
неможливо (у разі повзучого або злитого росту мікрофлори, що покриває всю
поверхню чашки). Якщо на всіх чашках наявний ріст розпливчастих колоній, який
спостерігають частково на поверхні агару, чи їх виросло більше, ніж 150
колоній, і аналіз не можна повторити, підраховують сектор чашки з наступним
перерахунком на всю поверхню. У таких випадках у протоколі відмічають:
«кількість КУО в 1 см3 – орієнтовна». Якщо підрахувати колонії на поверхні
чашок неможливо, – в протоколі відмічають: «суцільний ріст». 5.3. Обчислення та
вираження результатів Кількість мікроорганізмів у 1 см3 випробної проби
обчислюють за формулою:
∑C − сума колоній, підрахована; n 1 − кількість чашок з першим розведенням; п2 − кількість чашок з другим розведенням; d – коефіцієнт найнижчого розведення. Результат підраховування виражають двома цифрами. Якщо
цифрою, яку округлюють, є п’ять, – цифру, що стоїть зліва, залишають такою ж. Приклад: Розведення 10-2: 278 та 290 колоній;
Розведення 10-3: 33 та 28 колоній;
Якщо на чашці підраховано менше, ніж 10 колоній, – остаточну
кількість мікроорганізмів у 1 см3 подають як у 1м3. У разі отримання незадовільних результатів повторного
контролювання подвійної вибірки продукту всю партію бракують. 5.4. Методика ідентифікації та підрахунку КМАФАнМ та колі-форм
із застосуванням СЛАЙД-ТЕСТІВ Суть методу. Слайд-тести
використовують для підтвердження наявності та визначання, розмежування
КМАФАнМ та колі-формних бактерій у випробних рідких пробах. Слайд-тест складається з пластинки слайда, на обидві
поверхні якої нанесено агаризоване селективне середовище. Пластинка розміщена
у прозорому пластиковому флаконі з накривкою. Колонії бактерій ростуть на поверхні слайд-тесту.
Підраховують колонії за шкалою підрахунку. Групи мікроорганізмів, які визначають умови росту та
критерії оцінювання подано в таблиці 90. Таблиця 90 Групи мікроорганізмів, умови росту та критерії
оцінювання, які визначають за допомогою слайд-тестів
Контролювання. Знімають накривку, обережно дістають слайд, не торкаючись
сторін з нанесеними селективними середовищами. Слайд опускають у випробну
рідину на 10 с. Тверді продукти
гомогенізують до однорідної консистенції, готуючи перше розведення відповідно
до вказаного вище. Потім опускають слайд в отриману суспензію. Чекають, доки
стече надлишок рідини зі слайда. Слайд-тести також дають змогу висівати з
бактеріального фільтра. Після висівання
слайд повертають назад у флакон, щільно закривають накривкою, наносять
відповідне маркування та поміщають у термостат. Вирощування проб. Інкубувати слайд-тести треба у вертикальному
положенні. Температура і тривалість процесу вказані в таблиці 90. Опрацювання результатів. Бактеріальне забруднення рідини вказано з розрахунку 1
КУО на 1 см3. Бактерії підраховують, порівнюючи слайд-тест зі
шкалою порівнювання. Для того, щоб
визначити кількість мікроорганізмів у твердих продуктах, отримані відповідні
значення за шкалою порівняння, ділять на 10. Дуже високий
рівень забруднення може призвести до суцільного росту мікроорганізмів на
поверхні слайда. У разі виконання
арбітражних досліджень застосовують метод, зазначений у п. 5.1. Збіжність. Абсолютна різниця між двома окремими результатами одного дослідження,
отриманими з використанням одного методу, на ідентичному досліджуваному
матеріалі, у тій же лабораторії, тим же оператором, з використанням того ж
устатковання, впродовж короткого проміжку часу, має бути не більше, ніж 50 %
у разі вмісту 100 000 КУО у 1 см3, тобто найвищий результат не має
перевищувати найменший більш ніж на 50 %. Протокол контролювання. До протоколу контролювання вносять усю інформацію,
необхідну для повної характеристики проби та: а) використаний
метод відбирання, якщо він відомий; б) використаний
метод дослідження із посиланням на ДСТУ 7357; в) усі деталі, що
відносяться до цього дослідження, але не зазначені в стандарті або розглянуті
як додаткові, разом із детальним зазначенням усіх побічних обставин, що могли
б вплинути на результат дослідження; г) отриманий
результат дослідження. 6. Визначання
колі-формних бактерій (бактерій групи кишкових паличок) Суть методу. Метод ґрунтується на здатності колі-формних бактерій зброджувати лактозу
з утворенням кислоти і газу за температури (37±1) °С упродовж 24 год. Контролювання. Кількість посівного матеріалу, який засівають у
середовище, вказано у таблиці 2. 6.1. Висівання у середовище Кеслера. По 1 см3 означених у таблиці 91 розведень
продукту засівають у пробірки з 5 см3 середовища Кеслера.
Висівають 10 см3 пастеризованого молока, відібраного з
пастеризатора після проведення пастеризації, 10 см3 рідкої
закваски, 3 см3 кефірної закваски або 10 см3 розведення
1:10 згущеного молока і вершків із цукром, какао і кави зі згущеними молоком
та цукром у спожитковій тарі в колби з 40 см3 середовища Кеслера. Таблиця 91 Обсяги проб для аналізування БГКП у продуктах
Вирощування проб. Пробірки або колби з посівами поміщають у термостат за
температури 37±1 °С і витримують упродовж 18–24 год. У разі дослідження
морозива, засіяні пробірки витримують у термостаті за температури 37±1 °С
упродовж 48 год. Опрацювання результатів. Переглядають пробірки або колби з посівами. Висновок
щодо відсутності колі-формних бактерій роблять на підставі відсутності
газоутворення у найменшому з використаних розведень. За наявності у
найменшому із розведень газу у поплавку, вважають, що у цьому розведенні
наявні колі-формні бактерії. 6.2. Підтвердження
наявності колі-формних бактерій на середовищі Ендо Суть методу. Суть методу полягає у здатності колі-формних бактерій утворювати на
середовищі Ендо темно-червоні колонії з металевим блиском або рожево-червоні
без металевого блиску. Посів на середовище Ендо. Беруть посівний матеріал із позитивних проб,
отриманих на середовищі Кеслера, висівають на підготовлені чашки Петрі з
середовищем Ендо відповідно. Вирощування проб. Чашки Петрі з посівами поміщають у термостат за
температури 37±1 °С і витримують упродовж 19±1 год. Опрацювання результатів. Переглядають утворені колонії. У разі відсутності на
середовищі Ендо характерних колоній, продукт уважають таким, що не є
забрудненим колі-формними бактеріями. Наявність грампозитивних паличок, що
утворюють характерні колонії на середовищі Ендо, свідчить про наявність
колі-формних бактерій. Для остаточного
підтвердження наявності колі-формних бактерій із ізольованих колоній,
характерних для цих мікроорганізмів, роблять препарати, фарбують за Грамом та
мікроскопують. 6.3. Висівання у
жовчний агар з лактозою та фіолетовим червоним Висівання. Кількість посівного матеріалу, який засівають у середовище, вказано у
таблиці 91. 3 см3 дослідної проби розподіляють на три чашки,
вносячи по 1 см3 проби в кожну з них. У кожну
інокульовану чашку наливають по 12–15 см3 жовчного агару з
лактозою та фіолетовим червоним, ретельно перемішують для рівномірного
розподілу суспензії в середовищі. Проміжок часу від закінчення готування
проби і до змішування випробної порції з середовищем становить 12 ± 3 хв. Чашки залишають на
чистій, горизонтальній поверхні доти, доки не утвориться гель. Після цього на
поверхню агару наливають 4±2 см3 середовища, вказаного вище, для утворення
захисного від кисню шару. Вирощування. Переносять чашки в термостат. Чашки ставлять у термостат догори дном за
температури 30±2 °С упродовж 24±2 год. Підраховування колоній. Підраховують колонії в чашках Петрі, що містять не
більше, ніж 150 колоній. Підраховують темно-червоні колонії діаметром не
менше, ніж Якщо всі або деякі
колонії мають нехарактерний вигляд (наприклад, різняться за кольором,
розміром або формуванням преципітату, відмітного від типових колоній),
проводять підтверджувальне контролювання. Підтверджувальне контролювання. Відповідно до ознак, проводять підтверджувальне
контролювання. Для цього бактеріологічною петлею відбирають від 3-х до 5-и
нехарактерних колоній, що утворилися внаслідок висівання, кожну з яких
переносять у пробірки з лактозо-жовчним бульйоном. Витримують пробірки за
температури 31±1 °С упродовж 24±2 год. Колонії, що утворюють газ у трубці Дарема, є
колі-формними бактеріями. Наявність газу в трубці Дарема визначають
візуально. 6.4. Висівання на
селективний агар для одночасного визначання колі-формних бактерій та Е.соlі Суть методу. Метод ґрунтується на здатності характерного для групи колі-формних
бактерій ферменту β-D-галактозидази та специфічного для виду Е.соіі ферменту β-D-глюкуронідази, розщеплювати певні хромогенні субстрати з утворенням
пігментів, що забарвлюють колонії колі-формних бактерій у червоний колір, а
Е.сolі – від темно-синього до фіолетового. Ефективність
селективності хромогенного середовища забезпечує спеціальний реагент
Тергітол-7, що пригнічує розвиток багатьох грампозитивних та деяких
грамнегативних бактерій, за винятком виду Escherichia coli. Додатковим тестом щодо підтвердження розмежування
колі-формних бактерій та Е.соlі слугує реакція з виявляння наявності індолу, для проведення якої
використовують реактив Ковача. Висівання. По 1 см3 розведень продукту, означених у таблиці 92, засівають
у підготовлені чашки Петрі з селективним агаром, для одночасного визначення
колі-формних бактерій та Е. сolі, глибинним або поверхневим методами. Вирощування. Інкубують посіви впродовж 24 год за температури 36±2 ºС. Підраховування колоній. Переглядають колонії, що утворилися на поверхні агару.
Темно-сині або фіолетові колонії свідчать про наявність бактерій виду Е.соli, колонії від жовтувато-рожевого до червоного кольору –
інших колі-формних бактерій. Якщо на чашці реєструють безбарвні або блідо-голубі
колонії – це свідчить про наявність інших грамнегативних мікроорганізмів. Підтверджувальне контролювання. Для того, щоб підтвердити наявність бактерій виду Е.соli, на колонії, що мають темно-синє та фіолетове
забарвлення, наносять по 1 краплі реактиву Ковача. Якщо забарвлення реактиву
змінюється за кілька секунд на вишнево-червоне, це свідчить про позитивну
реакцію на індол і підтверджує наявність Е.соli. Обчислення та вираження результатів. Підраховують кількість колоній, що утворилися на
чашках. Якщо проводили підтверджувальне контролювання, рахують кількість
колоній колі-формних бактерій. Кількість
колі-формних бактерій у 1 см3 дослідної проби обчислюють за формулою:
∑С – загальна
кількість колоній колі-формних бактерій, знайдена дослідженням проби; п – об’єм дослідної
проби (3 см3). За наявності
менше, ніж 150 колоній, результат виражають з точністю до двох значущих цифр. Збіжність. Абсолютна різниця між результатами двох окремих досліджень, отриманих з використанням
одного методу, на ідентичному досліджуваному матеріалі, у тій же лабораторії,
тим же оператором, з використанням того ж устатковання впродовж короткого
проміжку часу, має бути не більше, ніж 50 % за вмісту 100 000 мікроорганізмів
у 1 см3, тобто найвищий результат не має перевищувати найменший
більше ніж на 50 %. Протокол випробування. До протоколу випробування вносять усю інформацію,
необхідну для повної ідентифікації проби, та: а) використаний
метод відбирання, якщо він відомий; б) використаний
метод дослідження із посиланням на стандарт; в) усі деталі, що
відносяться до даного дослідження, але не зазначені в стандарті або
розглянуті як додаткові, разом із детальним зазначенням усіх побічних
обставин, що могли б вплинути на результат дослідження; г) отриманий
результат дослідження. У разі отримання
незадовільних результатів хоча б за одним із показників якості проводять
повторне відбирання та контролювання подвійної вибірки продукту від тієї ж
партії. У разі отримання незадовільних результатів повторного контролювання
подвійної вибірки продукту, всю партію бракують. 7. Метод
мікроскопування Суть методу. Метод ґрунтується на перегляданні мікроскопічних препаратів,
пофарбованих спеціальними барвниками, для орієнтовної характеристики
мікрофлори молока та кисломолочних продуктів й розмежування грампозитивних та
грамнегативних бактерій. Проведення мікроскопування. Для приготування мікроскопічного препарату на чисте
знежирене предметне скло петлею наносять невелику краплю випробного матеріалу
й розподіляють на ділянці площею 1±0,2 см2. Препарат сушать за
температури 20±2 °С, фіксують над полум’ям спиртівки і фарбують спиртовим
розчином метиленового синього. Склад мікрофлори
продуктів подано в ДСТУ 2212. 7.1. Фарбування
препаратів за Грамом Суть методу. Метод ґрунтується на застосуванні диференційованого фарбування
мікроскопічних препаратів бактерій, згідно з яким грампозитивні бактерії
забарвлюються у фіолетовий колір, а грамнегативні – рожевий. Метод полягає у
фарбуванні мікроскопічного мазка барвником карболовим генциановим фіолетовим
та розчином Люголю з наступним знебарвлюванням етанолом. Грампозитивні
бактерії утримують барвник, тоді як грамнегативні потребують додаткового
дофарбовування фуксином (або сафраніном). Особливості фарбування. Мазок має бути тонким. Знебарвлення необхідно
проводити дуже швидко (щоб не вимити фарбу з грампозитивних клітин).
Додаткове контрастне фарбування розчином фуксину має бути короткотривалим –
не більш ніж 40 с (щоб не замаскувати попередньо нанесену фарбу). 7.2. Традиційна
методика Фіксований мазок
покривають клаптиком фільтрувального паперу й зверху наносять розчин
карболового генцианового фіолетового, зафарбовуючи препарат упродовж 1–2 хв. Знімають папір,
зливають фарбу, мазок обережно промивають дистильованою водою і наливають на
нього розчин Люголя (мазок чорніє). Через 1–2 хв
розчин зливають, на мазок наносять етиловий спирт з масовою концентрацією 96
% і витримують упродовж 0,5–1 хв до повного знебарвлення мазка. Мазок промивають
водою, додатково наносять водно-спиртовий розчин фуксину основного і
витримують упродовж 1–2 хв. Мазок промивають
дистильованою водою та сушать. 7.3. Методика за
Синьовим На фіксований
мазок кладуть папірець, виготовлений за методом Синьова. На папірець наносять
2–3 краплі дистильованої води, що повністю вбирається папером, і фарбують
упродовж 2 хв. Знімають папірець
пінцетом. Закінчують фарбування, як зазначено в п. 7.2. 8. Метод
визначання промислової стерильності Промислова стерильність – відсутність мікроорганізмів у 1 см3 ( Суть методу. Метод ґрунтується на здатності мікроорганізмів, які не загинули під час
стерилізації, розмножуватися в молоці, молочних продуктах або бактеріальних
препаратах за температури 37±1 ºС і призводити до відчутних змін
органолептичних, фізико-хімічних та санітарно-гігієнічних показників. 8.1. Проведення
контролювання згущеного стерилізованого молока та вершків Відібрані продукти
у спожитковому пакуванні (банки, пакети тощо) зі згущеним молоком або іншим
продуктом витримують у термостаті за температури 37±1 ºС упродовж шести
діб. Після цього
пакування з випробним продуктом охолоджують до 20±5 ºС і піддають поверхневому огляду. У разі
встановлення здуття накривки або дна, що не зникає за притискання, пакування
вважають бомбажним і занотовують це у протоколі. Пакування без зовнішніх
дефектів відкривають, продукт досліджують органолептично, за фізико-хімічними
(титрована та активна кислотність) та мікробіологічними показниками – готують
мікроскопічний препарат та, за необхідності, роблять посіви відповідно до
вищевказаного розділу відповідно до чинного стандарту або згідно з ДСТУ IDF 100В. Опрацювання результатів. У випробовуваних стерилізованих продуктах після
термостатування не повинно бути органолептичних та фізико-хімічних змін. У
мікроскопічному препараті не може бути наявних клітин мікроорганізмів. На
чашках з посівом випробного матеріалу кількість колоній бактерій не має
перевищувати 10 одиниць у 8.2. Проведення
контролювання стерилізованого чи НВТ молока та вершків Відібрані
пакування зі стерилізованим молоком витримують у термостаті за температури
37±1 ºС упродовж 3 діб, а вершки – 5 діб. Зразки молока, виготовлені
двох-стадійним способом, додатково витримують за температури 55±1 ºС ще
впродовж 5 діб. Після цього
пакування з випробним продуктом охолоджують до температури 20±5 ºС і
піддають поверхневому огляду. У разі встановлення здуття пакування або зміни
зовнішнього вигляду молока в пляшках (наявність згустків, сироватки тощо)
пакування з продуктом вважають таким, що не відповідає вимогам промислової стерильності,
і занотовують це у протоколі. Пакування без
зовнішніх дефектів відкривають, стерилізоване молоко або вершки досліджують
органолептично. Продукт відповідає
вимогам промислової стерильності, якщо не встановлено зміни консистенції та
смаку продукту. У арбітражних
випадках або для встановлення причини псування стерилізованого молока
визначають кислотність і проводять мікробіологічне контролювання,
застосовуючи мікроскопування та висівання 1 см3 проби. Щоб
визначити чисельність бактерій, роблять посіви відповідно до вказаного вище
п. 5 або згідно з ДСТУ IDF 100В. Опрацювання результатів. Продукт відповідає вимогам промислової стерильності,
якщо кислотність молока збільшується не більше, ніж на 2 ºТ, у
мікроскопічному препараті відсутні клітини мікроорганізмів, а загальна
кількість бактерій у 1 см3 не перевищує 10 КУО. У разі отримання
незадовільних результатів хоча б за одним із показників якості, проводять
повторне відбирання та контролювання подвійної вибірки продукту від тієї ж
партії. У разі отримання
незадовільних результатів повторного контролювання подвійної вибірки
продукту, всю партію бракують. 9. Метод
визначання редуктази з метиленовим синім Суть методу. Метод ґрунтується на відновленні метиленового синього
окисно-відновлювальними ферментами мікроорганізмів, що наявні в продукті. За
тривалістю знебарвлення метиленового синього визначають бактеріальне
забруднення сирого молока. Контролювання. У пробірки наливають по 1 см3 робочого
розчину метиленового синього і по 20 см3 дослідної проби молока,
закривають гумовими корками й перемішують, перевертаючи пробірки тричі. Пробірки поміщають
у редуктазник з температурою води 37±1 ºС, де витримують їх упродовж
4-ох год. Якщо немає
редуктазника, можна використовувати водяну баню, яку поміщають у термостат за
температури 37±1 ºС, або водяний термостат, здатний підтримувати
температуру 37±1 ºС. Рівень води в
редуктазнику, водяній бані, водяному термостаті після занурювання пробірок з
молоком має доходити до рівня рідини в пробірці або бути дещо вищим.
Температура води має бути 37±1 ºС упродовж усього терміну дослідження.
Пробірки з пробами впродовж усього контролювання потрібно захистити від
прямих сонячних променів. Для цього редуктазник щільно закривають накривкою. Момент занурювання
пробірок у редуктазник чи інший прилад вважають початком процесу
контролювання. Коли проба
знебарвлюється, контролювання закінчують. Ледь забарвлений кільцеподібний
шар зверху (товщиною не більше, ніж Опрацювання результатів. Ступінь бактеріального забруднення визначають за
тривалістю знебарвлення молока з метиленовим синім (таблиця 92). Таблиця 92 Ступінь бактеріального забруднення за тривалістю
знебарвлення молока з метиленовим синім
10. Метод дослідження редуктазної проби з резазурином Суть методу. Метод ґрунтується на відновленні резазурину окисно-відновлювальними
ферментами мікроорганізмів, які наявні в молоці. За тривалістю знебарвлення
резазурину оцінюють бактеріальне забруднення сирого молока. Контролювання.
Дослідження редуктазної активності треба виконувати не раніше, ніж через 2
год після доїння. У пробірки наливають по 1 см3 робочого розчину
резазурину і по 10 см3 дослідної проби молока, закривають гумовими
корками і змішують, повільно перевертаючи пробірки тричі. Дослідження
проводять згідно з п. 9. Показники реєструють через 1 год та 1,5 год. Можливе
забарвлення молока в цих пробірках унаслідок струшування не враховують. Через 1 год
пробірки дістають із редуктазника (водяної бані, водяного термостата).
Пробірки з молоком, що мають забарвлення від сіро-бузкового до бузкового зі
слабким сірим відтінком, залишають у редуктазнику ще на 30 хв. Опрацювання результатів. Рівень бактеріального забруднення молока визначають за
тривалістю знебарвлення або зміною кольору індикатора резазурину (табл. 93,
рис. 84). Таблиця 93 Рівень бактеріального забруднення молока та зміна
забарвлення молока з резазурином
11. Методи визначання сиро-придатності молока 11.1 Проба на
зброджування Суть методу. Метод ґрунтується на здатності сторонньої мікрофлори молока згортати
його. За тривалістю зсідання та характеру згустку, що утворився, оцінюють
придатність молока для виробництва сиру. Контролювання. Чисто вимиті пробірки ополіскують двічі або тричі
молоком, із якого відбирають пробу. Наливають у пробірки по 20±1 см3
молока. Пробірки закривають ватними корками і ставлять у термостат за
температури 38±1 ºС, де витримують їх упродовж 24 год. Опрацювання результатів. Через 12 год після вилучення з термостата проводять
перший перегляд проб. Якщо молоко не
зсілося або лише починає зсідатися, його оцінюють як сиропридатне. Якщо
молоко зсілося і згусток здутий – не сиропридатне. Вдруге проби переглядають
через 24 год і, за результатами цього перегляду, молоко, за бродильною
пробою, відносять до одного з чотирьох класів, наведених у таблиці 94. Таблиця 94 Клас молока за бродильною пробою
11.2. Сичужно-бродильна проба Суть методу. Метод ґрунтується на здатності спонтанної мікрофлори молока та сичужного
ферменту згортати його. За характером згустку оцінюють якість і
сиропридатність молока. Проведення контролювання. Чисто вимиті пробірки ополіскують двічі або тричі
молоком, із якого відбирають пробу. Наливають у пробірки по 31±1 см3
молока, додають у кожну по 1 см3 розчину сичужного ферменту,
ретельно перемішують і ставлять на водяну баню або термостат за температури
38±1 ºС, де витримують упродовж 12 год. Опрацювання результатів. Через 12 год після вилучення з термостата, проби
переглядають, і за результатами цього перегляду молоко за сичужно-бродильною
пробою відносять до одного з трьох класів, наведених у таблиці 95. Таблиця 95 Клас молока за сичужно-бродильною пробою
11.3. Сичужна
проба Суть методу. Метод ґрунтується на здатності сичужного ферменту згортати молоко. За
характером згустку оцінюють сиро-придатність молока. Контролювання. Молоко, з якого відбирають проби, підігрівають до
температури 35±1 ºС. У пробірки відміряють по 10 см3 молока,
ставлять на водяну баню за температури 35±1 ºС. Таку температуру
підтримують до кінця дослідження. Потім у пробірки додають по 2 см3
розчину сичужного ферменту, ретельно, не струшуючи, перемішують, і знову ставлять
на водяну баню. З цього моменту фіксують початок дослідження. Через кожні 2–3
хв переглядають пробірки на наявність утворення згустку (загущення молока,
поява пластівців). Дослід закінчують, коли завершується остаточне зсідання
молока. Опрацювання результатів. За тривалістю зсідання молоко відносять до одного з
трьох класів, наведених у таблиці 96. Таблиця 96 Клас молока за сичужною пробою
У молоці 1-го
класу утворюється щільний однорідний згусток, з якого швидко відшаровується
сироватка; для молока 2-го класу характерним є утворення щільного згустоку,
що легко віддає сироватку; у молоці 3-го класу утворюється нещільний згусток
або пластівці зі слабким відшаруванням сироватки. Через 20 хв
Через 1 год Від 100 тис. до 500 тис. Від 500 тис. до 3 млн Понад 3 млн Понад 3 млн
12. Дослідження на виявлення бактерій роду Salmonella Суть методу
полягає у визначенні характеру росту сальмонел на елективних середовищах,
визначенні біохімічних та антигенних властивостей. Виявлення
сальмонел проводять у 4-и етапи, що включають первинний (прямий) посів на
елективні середовища, збагачення культур шляхом посіву на рідкі елективні
середовища, пересівання із середовищ накопичення на щільні
елективно-діагностичні середовища (Ендо, Плоскирєва, Левіна,
вісмут-сульфітний агар), визначення властивостей виділеної культури. На елективних
середовищах сальмонели ростуть, утворюючи характерні колонії, на Ендо –
круглі блискучі або ледь рожевуваті, прозорі або напівпрозорі; Левіна –
прозорі та ніжно-рожеві або рожево-фіолетові; бактоагарі Плоскирєва –
безбарвні; вісмут-сульфітному агарі – чорні або коричневі з металевим блиском
(рис. 85).
Якщо після
первинного посіву на елективні середовища ріст на них відсутній, – через 24
год проводять пересів із середовищ накопичення (Мюлера, Кауфмана, Кіліані,
селенітовий бульйон) на елективні середовища. Підозрілі колонії
бактерій сальмонел досліджують у такому порядку: із частини колонії готують
мазки, фарбують їх за Грамом і досліджують на рухливість. Решту колоній
пересівають і, в подальшому, використовують для визначення біохімічних
властивостей, для цього чисту дослідну культуру пересівають на середовище
Гісса (глюкоза, лактоза, сахароза, маніт) або трицукровий агар. За посіву на
трицукровий агар, спочатку сіють штрихом по скошеній поверхні, а потім –
уколом углиб стовпчика. Для визначення сірководню, дослідну культуру
висівають на середовище Олькеницького. До роду сальмонел
належать бактерії, що не ферментують лактозу і сахарозу, не утворюють індолу
й утворюють сірководень, ферментують глюкозу і маніт (S. typhisuis не ферментує маніт). Якщо необхідно
остаточно визначити серовар сальмонел, визначають антигенні властивості
дослідної культури за допомогою О- і Н-аглютинуючих сальмонельозних
сироваток. У випадку, коли
виділена культура сальмонел має відхилення від типових властивостей, для її
ідентифікації проводять додаткове дослідження на чутливість до
О-бактеріофага. Для цього, на добре підсушеному МПА з рН 7,2–7,4, стерильною
пробіркою з рівними краями роблять 5–6 насічок. На кожну з них петлею
наносять по дві краплі 4–18-годинної бульйонної або агарової культури. Після
підсихання тоненькою пастерівською піпеткою наносять на неї краплю
зазначеного на етикетці О-бактеріофага, розведеного в 10 і 100 разів, а на
іншу, для контролю, наносять краплю МПБ. Чашки ставлять у термостат за
температури 37 оС на 18–20 год, а потім ураховують результати.
Позитивною реакцію вважають тоді, коли на місці нанесення фага чітко виражена
зона лізису. Методика
дослідження харчових продуктів на наявність сальмонел за міжнародним
стандартом ДСТУ EN 12824 Міжнародний
стандарт призначений для впровадження спільних мікробіологічних методів
визначення сальмонел у харчових продуктах тваринного походження (рис. 86).
13. Дослідження на
виявлення бактерій Listeria Виявлення цих
бактерій полягає у визначенні специфічного росту цих мікроорганізмів на
поживних середовищах та їхньої диференціації за морфологічними,
культуральними та біохімічними властивостями (табл. 97). Для виявлення
збудників лістеріозу, проводять люмінесцентно-серологічні дослідження. Матеріал для
дослідження має бути свіжим. Для люмінесцентної мікроскопії з паренхіматозних
органів готують суспензію на фізіологічному розчині у співвідношенні 1:5.
Готують по 2–3 мазки на кожний вид сироваток і фарбують їх флюоресціюючими
сироватками. Для виділення
культур збудників із дослідної суспензії, з урахуванням особливостей росту,
роблять посів на МПА, МПБ, агар Хоттінгера, МПА з телуритом калію,
сироватковий МПА з глюкозою та кров’яний МПА з глюкозою. Збудник бешихи на
МПА утворює колонії у вигляді крапель роси; на МПБ – легке рівномірне
помутніння. Таблиця 97 Диференціальні показники збудників бешихи, лістеріозу
та пастерельозу
Лістерії на кров’яному
МПА утворюють росині колонії з β-зоною гемолізу, на МПА з телуритом калію – маленькі,
чорні, ізольовані одна від одної колонії. Для диференціації
збудників лістеріозу проводять люмінісцентно-серологічні дослідження
вирощених культур із використанням флюоресціюючих сироваток. Диференційний
діагноз збудника лістеріозу проводять згідно з показниками таблиці 3. Нижче подано схему
лабораторного дослідження продуктів харчування, зокрема молока на наявність Listeria monocytogenes за міжнародним стандартом ДСТУ ISO 11290–2.
14. Дослідження на наявність бактерій роду Proteus Виявлення бактерій
роду Proteus включає визначення морфології та характеру росту на
поживних середовищах, здатність їх гідролізувати сечовину, утворювати
сірководень і не ферментувати маніт. Для виявлення
бактерій роду Proteus методом Шукевича проводять посів на МПА в
конденсаційну рідину. На МПА Н-форма збудника росте у вигляді розпливчастих
повзучих колоній; можуть зустрічатися й ізольовані напівпрозорі колонії з
рожевим центром. Для виявлення
О-форм, що не рояться, посів роблять на середовище Плоскирєва. О-форма протея
на цьому середовищі росте у вигляді прозорих колоній із жовтуватим відтінком
(унаслідок підлужування) і специфічним запахом. Біохімічні
властивості бактерій роду Proteus наведені в таблиці 98 Таблиця 98 Біохімічні властивості бактерій роду Proteus
Ідентифікація
бактерій роду Proteus за допомогою О- і Н-аглютинуючих полівалентних сироваток. Серологічну
ідентифікацію культур проводять після визначення їх належності за
біохімічними властивостями до роду Proteus. Це є необхідним, тому що окремі представники родових
груп протея – Proteus і Morganella – мають О-антигенні зв’язки, що відрізняються лише
окремими біохімічними властивостями (ферментація ксилози, розрідження
желатину та утворення сірководню). Сухі О- і
Н-сироватки перед використанням розчиняють стерильним розчином хлористого
натрію з масовою часткою 0,85 % до об’єму, зазначеного на етикетці, і
використовують у РА на предметному склі без наступних розведень. Методика постановки РА. На предметне скло наносять краплю аглютинуючої
сироватки, потім бактеріологічною петлеюа край краплі сироватки, додають
20-годинну дослідну агарову культуру і розтирають її по склу, після чого
петлею з’єднують сироватку з бактеріальною масою і знову розтирають. За
слабкої рухливості культури для визначення Н-антигену необхідно провести
повторний пересів у напіврідкий МПА в U-подібні трубки. За результатами РА дослідного штаму за
однією з полівалентних О-сироваток,визначають групову належність; за
допомогою типових О-сироваток, що входять до складу полівалентної, з якою
аглютинувалася культура, визначають О-антиген цих культур. За допомогою
полівалентних Н-сироваток, а потім – типових, визначають серовар культури. Виявлення
поліморфних грамнегативних паличок із характерним для них ростом,
ферментування глюкози, сечовини і не ферментування лактози і маніту свідчать
про наявність бактерій роду Proteus. 15. Дослідження на
наявність коагулазопозитивних стафілококів Дослідження на
наявність коагулазопозитивних стафілококів проводять відповідно до схеми
(рис. 87). Із розведення
зависі продукту 1:10 проводять посів на молочно-сольовий агар із умістом 6,5
% хлориду натрію або на жовтково-сольовий агар (для виявлення лецитиназної
активності).
Посіви культивують
за температури 37 ºС упродовж 24 год. Із підозрілих
колоній (випуклих, емалево-білих або золотистих, а на ЖСА – з райдужною
зоною) готують мазки і фарбують їх за Грамом. Для підтвердження
патогенності стафілококів ставлять реакцію плазмокоагуляції, результати якої
враховують через 3–4 год. Суть методу
полягає у визначенні морфологічних ознак і характеру росту мікроорганізмів на
поживних середовищах та здатності їх продукувати коагулазу і лецитиназу. Із розведення 1:10
дослідної проби, методом Дригальського роблять висів на молочно-сольовий або
жовтково-сольовий агар. Дослідну суспензію в дозі 0,2 см3 додають
на поверхню середовищ і рівномірно розтирають шпателем по всій поверхні.
Посіви ставлять у термостат за температури 37 ºС на 24 год, після чого
витримують ще 24 год за кімнатної температури. За наявності
стафілококів, на поверхні середовища виростають плоскі або ледь блискучі
колонії з рівними краями. На
молочно-сольовому агарі після витримування посівів за кімнатної температури у
колоній з’являється емалево-білий або золотистий пігмент, а на
жовтково-сольовому агарі колонії стафілококів утворюють віночок, подібний до
райдуги. Із підозрілих
колоній готують мазки і фарбують їх за Грамом. У препаратах виявляють коки у
вигляді виноградного грона. Для визначення патогенності стафілококів ставлять
реакцію плазмокоагуляції. 16. Готування
розчинників, поживних середовищ та реактивів Для підвищення
точності отриманих результатів, виготовлення розчинників, поживних середовищ
та реактивів рекомендовано використовувати зневоднені основні компоненти або
зневоднені готові препарати. Необхідно чітко дотримуватися настанов
виробника. Щоб установити
необхідне значення рН розчинників, поживних середовищ та реактивів, якщо
немає інших рекомендацій, використовують розчини гідроксиду натрію або
хлористоводневої кислоти (0,1 моль/дм3). Усі виготовлені
середовища маркують із зазначенням назви середовища, дати виготовлення та
терміну придатності. 1. Готування
розчинників 1.1. Розчинники
загального використання Розчин хлориду
натрію. Склад: натрію хлорид (NаСІ) – Готування:
розчиняють компоненти у воді, за потреби нагрівають, встановлюють рН так, щоб
після стерилізації, за температури 25±1 °С він становив 7,0±0,1. Концентрований розчин фосфатного буфера. Склад: калій фосфорнокислий однозаміщений (К2НР04)
– Готування: у мірну
колбу місткістю (1000±0,50) см3 наливають 500 см3 дистильованої
води, розчиняють у ній 34±0,02 г калію фосфорнокислого одно-заміщеного. До розчину додають
дистильовану воду та доводять нею об'єм до 1000 см3. За допомогою рН-метра встановлюють рН
7,2±1. Робочий розчин фосфатного буфера. Склад: концентрований фосфатний буфер – 1,25 см3;
вода дистильована – 98,75 см3. Готування:
1,25±0,01 см3 концентрованого фосфатного буфера вносять у мірну
колбу ємністю 1000±0,50 см3, дистильованою водою доводять об’єм до
позначки. Пептонно-сольовий розчин. Склад: пептон – Готування:
розчиняють компоненти у воді, підігріваючи їх до температури 70,0±0,5
ºС, установлюють рН так, щоб після стерилізації, за температури 25
ºС, він становив (7,0±0,1). Розчин пептону.
Склад: пептон – Готування:
розчиняють пептон у дистильованій воді. Установлюють рН
так, щоб після стерилізації, за температури 25 °С, він становив (7,0 ±0,1). 1.2. Розчинники спеціального призначення Розчин цитринового натрію (для приготування розведень сиру) Склад: натрій
цитриновий (Nа3С6Н5O7×2Н20) – Готування: у мірну
колбу місткістю 1000±0,50 см3 вносять 20±0,02 г натрію цитринового
за температури 20±3 ºС та доводять об'єм до позначки дистильованою
водою. Ледь похитуючи, розчиняють. Розчин двовуглекислого натрію (для нейтралізації проб кисломолочних продуктів і
заквасок) Склад:
двовуглекислий натрій (Nа2С03) – Готування: у 100 ±
0,05 см3 дистильованої води за температури 20±3 °С розчиняють
10±0,01 г двовуглекислого натрію. Розчин фосфорнокислого калію двозаміщеного (для досліджень сиру, кисломолочних продуктів казеїну,
кислотного казеїну, сухого молочного казеїну, казеїнатів, сухої кислої
сироватки та сметани) Склад:
фосфорнокислий калій двозаміщений (К2НР04) – Готування:
розчиняють сіль у воді, нагрітій до температури 45–50 ºС. Установлюють
величину рН. Для початкового розведення кислотного казеїну і сухої кислої
сироватки після стерилізації, за температури 25±1 ºС рН має становити
8,4±0,1. Для казеїнатів, сирів і сметани рН має становити 7,5±0,1. 1.3. Розливання,
стерилізація та зберігання розчинника Для початкового
розведення розчинники, що описані вище у пп.1.1, 1.2., розливають у колби
ємністю 100 см3, 200, 500, 1000 см3. Розчинник для
десятиразових розведень розливають у пробірки діаметром Стерилізують
розчинник у стерилізаторі за температури 121±1 °С упродовж 20±1 хв. Якщо розчинник не
використовують відразу, його зберігають за температури 0–5 ºС не довше
1-го міс. 2. Готування
поживних середовищ Ураховуючи можливу
зміну рН поживних середовищ після кип'ятіння та стерилізації, під час
приготування середовищ установлюють рН на 0,2 одиниці вище або нижче вказаного. Цю величину
визначають експериментально для кожного середовища. Остаточний контроль рН
проводять у готовому середовищі з використанням рН-метра (рідкі середовища)
або паперових індикаторів з кроком діапазону не більше 0,2 (агаризовані
середовища). Визначення
виконують згідно з інструкцією щодо використання приладу або індикаторної
системи. Поживні середовища
можна готувати із: – комерційного
сухого середовища (у цьому разі необхідно дотримуватися настанов виробника); – основних
компонентів згідно з указаним нижче чинним стандартом. 2.1. Поживні
середовища для визначання кількості мезофільних аеробних і
факультативно-анаеробних мікроорганізмів Для контролювання
можна застосовувати середовища, наведені в ГОСТ 10444.1. Середовище 1. Склад: сухий поживний агар – Готування. Компоненти розчиняють у воді в такій послідовності: дріжджовий
екстракт, глюкоза. Додають сухий поживний агар і, безперервно перемішуючи,
нагрівають до кипіння або тримають над парою впродовж 30±5 хв до повного
розчинення агару. За необхідності, фільтрують через фільтрувальний папір. Величину рН
визначають рН-метром і, за потреби, регулюють його так, щоб після
стерилізації за температури 25 ºС його значення становило 7,0±0,1. Середовище 2. Склад: пептон казеїновий – Готування.
Безперервно перемішуючи, розчиняють у воді складники в такій послідовності:
казеїновий пептон, желатиновий пептон і хлорид натрію. Додають агар,
доводять до кипіння, ретельно перемішуючи до повного розчинення агару, або
кип'ятять упродовж 30±5 хв. Фільтрують, застосовуючи фільтрувальний папір. За допомогою
рН-метра встановлюють рН так, щоб після стерилізації, за температури 25±1 °С
його значення становило 7,5±0,1. Примітка. Для кисломолочних продуктів рН доводять до такого рівня, щоб після
стерилізації, його значення за температури 25±1 ºС становило 8,0 ± 0,1. Середовище 3 для підраховування колоній у молоці. Склад: дріжджовий екстракт триптон
– Примітка. Порошок знежиреного молока має бути без інгібіторів. Готування.
Компоненти розчиняють у воді в такій послідовності: дріжджовий екстракт,
триптон, глюкоза та порошок знежиреного молока. Додають агар і, безперервно
перемішуючи, нагрівають до кипіння або тримають над парою впродовж 30 ± 5 хв
до повного розчинення агару. Фільтрують крізь
фільтрувальний папір, перевіряють величину рН за допомогою рН-метру і, за
потреби, регулюють рН так, щоб після стерилізації за температури 25 ºС
його значення становило 6,9±0,1, використовуючи розчин гідроксиду натрію або
хлористоводневої кислоти. Розливання, стерилізація та зберігання поживних
середовищ для визначання КМАФАнМ Середовища
розливають у кількості від 100 см3 до 150 см3 у колби
або від 12 см3 до 15 см3 – пробірки. Закривають колби та пробірки
корками. Пробірки (колби)
стерилізують в автоклаві за температури 121±1 °С упродовж 15 хв. Якщо поживне
середовище використовують одразу, – перед використанням його охолоджують на
водяній бані до температури 44–47 ºС. Зберігають поживне середовище у темному місці
за температури1–5 ºС не більше 3-х міс. 2.2. Поживні
середовища для визначання колі-формних бактерій (бактерій групи кишкових
паличок) Середовище Кеслера (модифіковане). Склад: пептон – Готування. У мірну
колбу місткістю 1000±0,50 см3 наливають 500 см3 дистильованої
води, додають Установлюють рН
суміші в межах 7,4–7,6, після чого додають 2 см3 розчину
кристалічного фіолетового з масовою часткою 10 г/дм3. Розливають у
пробірки з поплавками по 5 см3 чи колбочки з поплавками від 40 см3
до 50 см3. Стерилізують за
температури 121±2 ºС упродовж 10±1 хв. Готове середовище повинно мати
темно-фіолетовий колір. Поплавки після стерилізації мають бути без повітряних
бульбашок. Якщо середовище не
використовують одразу, – його зберігають у темному місці за температури від 1
°С до 5 ºС не довше 1-го міс. після виготовлення. Розчин фіолетового червоного жовчного агару з лактозою Тверде селективне середовище. Склад: пептон – Компоненти
розчиняють у воді за температури 25±1 ºС, залишають для відстоювання на
10–15 хв, після чого енергійно перемішують. Установлюють рН на
рівні 7,4±0,2 за температури 25±1 °С, використовуючи розчин гідроксиду натрію
або хлористоводневої кислоти. Доводять до
кипіння, час від часу перемішуючи, і негайно вносять по 100 см3
або 150 см3 розчину в колби. Регулюють температуру середовища на
водяній бані за температури 45±3 ºС. Середовище можна
використовувати впродовж 3 діб. Лактозо-жовчний бульйон з діамантовим зеленим Підтверджувальне
середовище. Склад: пептон – Готування.
Розчиняють компоненти у воді під час кип’ятіння. Установлюють рН
так, щоб після стерилізації за температури 25±1 ºС його значення становило 7,2±0,1. Розливають середовище
по 10 см3 у пробірки, що містять трубки Дарема. Закривають
пробірки корками. Стерилізують у
автоклаві за температури 120±1 ºС упродовж 15±2 хв. Трубки Дарема (поплавки) після стерилізації мають
бути без повітряних бульбашок. Перевіряють рН середовища. Якщо середовище не
використовують негайно, – його зберігають у темному місці за температури від
0 ºС до 5 ºС не довше 1-го міс після виготовлення. Середовище Ендо Розчин сірчанокислого натрію. Склад: сірчанокислий натрій (Na2S04) – У колбу ємністю
100±0,50 см3 додають М’ясо-пептонний агар (МПА). Склад: м’ясо-пептонний бульйон – 1000 см3;
агар – Готування. У мірну
колбу місткістю 1000±0,50 см3 додають Установлюють рН
середовища в межах 7,1±1. Гарячий розчин
фільтрують. Розливають середовище у колби в кількості від 100 см3
до 150 см3. Стерилізують в
автоклаві за температури 120±1 ºС упродовж 20±2 хв. Готування повного середовища Ендо. Склад: м’ясо-пептонний агар – 100 см3;
розчин фуксину основного – 1 см3; сірчанокислий натрій – 5 см3;
лактоза – У колбу з
розплавленим МПА ємністю 100±0,50 см3 додають Чашки Петрі з
середовищем необхідно зберігати в захищеному від світла місці. Термін
зберігання за температури 3 ± 1 ºС становить три доби. Селективний агар
для одночасного визначання колі-формних бактерій та Е. соli. Склад: пептон – Готування.
Зважують Середовище не
можна автоклавувати та перегрівати. Величина pH готового середовища має бути 6,8±0,2 за температури
25±1 ºС. Перед
використанням середовище ретельно перемішують і розливають у чашки Петрі. Середовище в
чашках Петрі має жовтуватий колір, мутнувате. Зберігають середовище в
холодильнику, захищаючи від світла. Для того, щоб запобігти висиханню,
підготовлені чашки з середовищем поміщають у пластикові пакети. За цих умов
воно може зберігатися впродовж 6-ти міс. 3. Готування
реактивів 3.1. Готування
барвників Розчини барвників
зберігають у ємностях, захищених від світла. Спиртовий розчин
метиленового синього (для фарбування препаратів) Склад: метиленовий
синій – Готування: у мірну
колбу ємністю 100±0,50 см3 додають Термін зберігання
розчину метиленового синього не має перевищувати 3-х міс. Робочий розчин метиленового синього Готування. У мірну
колбу місткістю 200±0,50 см3 додають 30 см3 спиртового
розчину приготовленого метиленового синього, 100 см3 дистильованої води і 1
см3 розчину гідроксиду калію з масовою часткою 10 г/дм3. Термін зберігання робочого розчину
метиленового синього не має перевищувати 1 міс. Розчин метиленового синього для редуктазної проби Готування водного
розчину з концентрацією метиленового синього 0,005 г/ см3: Готування розчину
метиленового синього з концентрацією 0,00015 г/см3: у мірну колбу ємністю 200±0,50 см3
додають 6 см3 розчину метиленового синього з масовою концентрацією
0,005 г/см3, змішують зі 194 см3 дистильованої води. Термін зберігання
готового розчину – не більше, ніж 30 діб у холодильнику за температури 3±1
ºС. Розчин резазурину. Готування основного розчину: 100 мг
резазурин-натрієвої солі вносять у мірну колбу ємністю 200 см3 і доводять
водою до позначки. Суміш ретельно перемішують. Термін зберігання основного
розчину резазурин-натрієвої солі не має перевищувати 30 діб за температури
9±1 ºС. Готування робочого
розчину. Робочий розчин резазурин-натрієвої солі готують розведенням
основного розчину, попередньо кип’яченою і охолодженою до температури (25±2)
ºС дистильованою водою, у співвідношенні 1:2,5 (наприклад до 10 см3
маточного розчину додають 25 см3 дистильованої води). Масова частка
резазурину в робочому розчині становить 0,014 %. Готування розчину
резазурину з таблеток. Коли застосовують резазурин у таблетках? Для
приготування робочого розчину в мірну колбу ємністю 50±0,10 см3 додають 1
таблетку і 50 см3 попередньо кип’яченої та охолодженої до 25±2
ºС дистильованої води. Масова частка резазурину в цьому розчині
становить 0,01%. Термін зберігання
робочого розчину резазурину – не довше 3-х діб за температури від 0 °С до 5
°С. Основний та робочий розчини зберігають у ємностях, захищених від світла. Розчин сичужного ферменту. Склад: сичужний порошок – Готування: у мірну
колбу ємністю 100±0,50 см3 додають Готування розчинів для фарбування за Грамом. Насичений розчин фуксину
основного. Склад: фуксин основний кристалічний – У мірну колбу
ємністю 100±0,50 см3 додають Готування водно-спиртового розчину фуксину основного. У мірну колбу ємністю 10±0,50 см3 додають 1
см3 насиченого спиртового розчину та доводять об’єм до позначки дистильованою
водою. Розчин карболового
фуксину. Склад: фуксин основний кристалічний – Готування. Розчин карболового генцианового фіолетового. Склад: генциановий фіолетовий – Готування: Розчин є нестійким
до світла, тому зберігати його необхідно в ємностях з темного скла. Термін
зберігання розчину – не довше 3-х міс. за температури 0–5 ºС. Папір за Синьовим.
Готування паперу для фарбування за Синьовим. У мірну колбу
ємністю 100±0,50 см3 додають 100 см3 розчину етилового
спирту з масовою концентрацією 96 %, Розчин Люголя. Склад: йод кристалічний – Готування: у порцеляновій ступці розтирають |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||