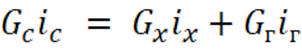|
|
|
ТЕОРЕТИЧНІ ОСНОВИ ХОЛОДИЛЬНОЇ ТЕХНІКИ частина I Електронний посібник |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
РОЗДІЛ 2. ТЕРМОДИНАМІЧНІ
ОСНОВИ ШТУЧНОГО ОХОЛОДЖЕННЯ |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
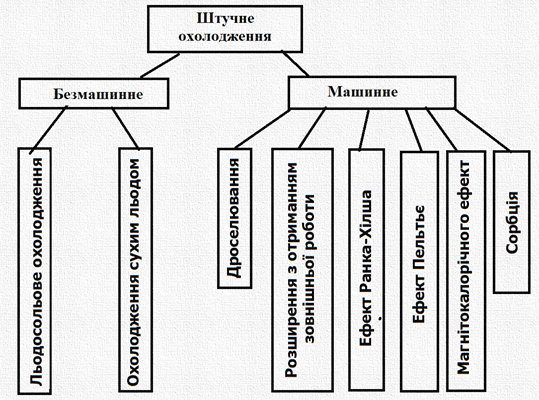
Розрізняють два способи отримання
холоду природний та штучний. Природне охолодження характеризується
передачею тепла від охолоджуваного
тіла навколишньому середовищу, за умови, що температура навколишнього середовища менше від температури охолоджуваного тіла. Але таке охолодження використовується не часто, адже
температура навколишнього середовища
має значні коливання і не піддається регулюванню.
Для
здійснення процесів
машинного охолодження необхідні
витрати енергії.
Найпоширенішими способами одержання
низьких температур є дроселювання,
що застосовується в парових компресорних і тепловикористовуючих холодильних
машинах, а також розширення
з отриманням зовнішньої роботи, що застосовується
в газових холодильних
машинах. Магнітокалорічний ефект
і десорбція газів застосовуються в основному в лабораторній
практиці для отримання
температур від 4 К до близьких
до абсолютного нуля. Для штучного отримання
низьких температур в області
помірного холоду (в діапазоні
від 0 до мінус 100 оС) використовують спеціальні середовища – рідини, здатні кипіти і випаровуватися за низьких температур. До них належать деякі
зріджені гази, такі як: аміак, пропан, бутан, двоокис вуглецю або двоокис сірки,
а також штучно створені хімічні сполуки метану з хлором
та фтором – хладони. Для отримання
низьких температур в області
глибокого холоду (в діапазоні
температур від -100 до -273 оС)
використовують гази, критична температура яких нижча за температуру навколишнього середовища. До
таких газів відносять: азот етан,
етилен, метан, повітря та
інші. Основними
параметрами та теплофізичними характеристиками зріджених і регазованих середовищ є хімічний склад,
температура, тиск, агрегатний
стан, густина, теплоємність,
теплопровідність, в’язкість,
питома теплота фазового переходу та ін. Залежно від необхідного діапазону отримання низьких температур використовують різні способи штучного охолодження. У способах помірного охолодження переважно використовують проміжні робочі тіла (низькокиплячі рідини), в інших способах робочими тілами є самі охолоджувані гази.
Низькі температури отримують
зa допомогою фізичних процесів, які супроводжуються поглинанням теплоти. До таких процесів належать фазові перетворення речовин, які супроводжуються поглинанням теплоти зовні: плавлення; кипіння (випаровування);
сублімація; адіабатичне дроселювання газу з попередньою
температурою, яка менша за температуру верхньої точки інверсії (ефект Джоуля-Томпсона); адіабатичне
розширення газу з віддачею
корисної зовнішньої роботи; вихровий ефект (ефект Ранка); термоелектричний ефект (ефект Пельтьє).
Фазове перетворення
певної кількості речовини при плавленні, кипінні, сублімації здійснюється за низьких
температур і з поглинанням значної
кількості теплоти. Ця особливість фазових перетворень дає можливість отримувати низькі температури.
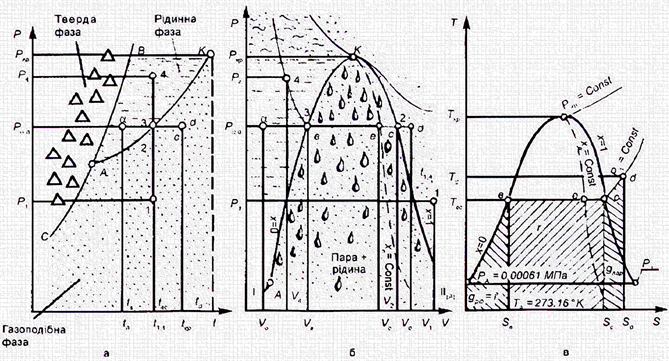
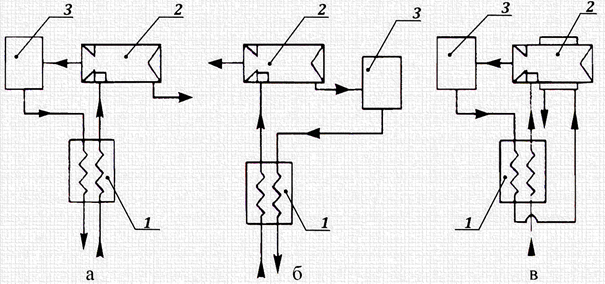
Фазові перетворення
в Р-t-координатах подано на рис. 2.1 а. Три однофазні
стани (тверда, рідинна i газоподібна фази) розділені кривими СА, ВА і KA, кожна з яких відповідає двофазному стану речовини: АВ ‒ «тверде тіло ‒ рідина», АК ‒
«рідина ‒ пара», АС ‒ «тверде тіло ‒ газ», AB ‒
називають кривою плавлення,
АК ‒ крива кипіння, АС ‒ крива сублімації. Вид і розташування цих кривих залежать
від природи речовини.
Будь-які
термодинамічні діаграми
стану реального газу (P-V, S-T, i – S та ін.) також
є фазовими діаграмами. Однак, на відміну від Р‒t-діаграми, де вони
двофазного стану зображені
лініями, на P‒V i Т‒S-діаграмах вони зображені відповідними площами (рис. 2.1
б, в). Це дає можливість здійснювати аналіз процесів y двофазному стані речовини. Так, процес
ізотермічного тиску на Р‒t-діаграмі (1‒2‒3‒4, рис. 2.1 а) виразніше відображається на P‒V-діаграмі (1‒2‒3‒4, рис. 2.1 б). Процес (2‒3) на Р‒t-діаграмі
відображається однією
точкою 2, 3 і не розкриває характеру процесу. На Р‒V-діаграмі
процес (2‒3), що супроводжується конденсацією і повним перетворенням газоподібної фази на рідину в точці 3, піддається аналізу з урахуванням даних діаграми. Так, з діаграми
виходить, що ступінь сухості змінюється від x = 1 (точка 2)
до x = 0 (точка 3). Процес ізотермічної
конденсації (2‒3) збігається
з ізобарою св. Подальше стиснення
(3‒4) призводить до різкого
підвищення тиску, оскільки рідина менше стискається, ніж газ. Отже, ліворуч
I‒К існує тільки рідинна фаза, a праворуч ІІ‒К
‒ тільки газ. Між цими кривими знаходиться ділянка двофазного стану (пара + рідина).
У критичній точці К різниця між газом і рідинною фазою зникає. Вище від цієї
точки існування речовини
у двофазному стані неможливе (жодним тиском перетворити газ у рідину за умови t > tкp не можна). На Р‒V-діаграмі
крива I‒К ‒ це стан киплячої
рідини. Пара, що при цьому утворюється, знаходиться в динамічній рівновазі з киплячою рідиною. Таку пару називають насиченою. Наявність рідини в парі характеризується коефіцієнтом сухості пари. Отже, крива ІІ‒К відповідає стану сухої насиченої пари (x = 1), a крива І‒К ‒ стану киплячої рідини (x = 0). Проміжок між цими кривими відповідає стану вологої насиченої пари. Пару, температура якої за такого тиску (наприклад, Ра, d) більша
за температуру кипіння (наприклад,
Td), називають перегрітою парою
(точка d). Процес отримання
перегрітої пари (a‒d) складається
з трьох послідовних стадій: підігрівання рідини до температури кипіння (а‒в), пароутворення
(в‒с) за сталої температури
й перегрівання пари до необхідної
температури (c‒d). Усі
ці стадії протікають за сталого тиску та на термодинамічних діаграмах відображається ізобарою. Процес пароутворення
в Т‒S-діаграмі відображено
на рис. 2.1 в. Кількість теплоти,
що витрачається на пароутворення в процесі (в‒с),
називають теплотою пароутворення
Компресорні холодильні
машини залежно від агрегатного стану холодильного агента, за допомогою якого здійснюються робочі процеси циклу, діляться на парові таі газові.
У парових холодильних
машинах робоча речовина
робить замкнутий зворотний
круговий термодинамічний
цикл, змінюючи свій агрегатний стан за схемою: пар-рідина-пар. У газових
холодильних машинах агрегатний
(газоподібний) стан робочої
речовини не змінюється, причому? як робоча речовина застосовується здебільшого повітря. Адіабатичне дроселювання ‒ це необоротне розширення газу під час його проходження крізь пристрій з малим прохідним перерізом (дросель, пориста
перегородка та ін.). Процес
протікає швидко, тому теплообмін із зовнішнім середовищем практично
не відбувається і ентальпія
речовини не змінюється. Корисна зовнішня робота не здійснюється, тому? що робота проштовхування перетворюється
на теплоту тертя. Під час адіабатичного дроселювання реального газу, на відміну
від ідеального? внаслідок зміни внутрішньої енергії, виконується робота проти сил взаємодії молекул. Це призводить до зміни температури газу (ефект
Джоуля-Томпсона) ‒ підвищення або зниження залежно від його
попереднього стану. Ефект Джоуля-Томпсона (дросель-ефект) ‒ зміна температури газу під час його адіабатичного дроселювання, тобто зниження тиску газу під час його протікання крізь пористу перегородку, діафрагму або вентиль без теплообміну з навколишнім середовищем. Такий ефект називають
позитивним, якщо температура
газу під час адіабатичного
дроселювання знижується,
і негативним, якщо вона підвищується. Позитивний ефект Джоуля-Томпсона використовують
y техніці для отримання низьких температур, а також під час зрідження газу. Для всіх
газоподібних речовин y зоні, близькій до критичної, адіабатичне дроселювання призводить до зниження температури. У надкритичній зоні існує стан газу, що називають точками інверсії, y яких ефект зміни
температури змінює знак. Сукупність цих точок ‒ це крива, яку називають інверсійною кривою. Вибираючи стан газу, що лежить під інверсійною
кривою, можна здійснити процес, який супроводжується зниженням температури газу. Процес адіабатичного
дроселювання використовують
для утворення помірно низьких і кріогенних температур.
Під час дроселювання
проводиться внутрішня робота, яка витрачається на розсування
молекул всупереч силам їх
взаємного притягання. Це відбувається тому, що під час виходу
газ має протистояти міжмолекулярним силам. Як результат частина
енергії теплового руху молекул переходить в потенційну енергію їх взаємодії. Відповідно температура газу знижується, хоча загальна його енергія не змінюється. Відбувається лише її перерозподіл ‒ спад кінетичної і зростання потенційної. Ефект
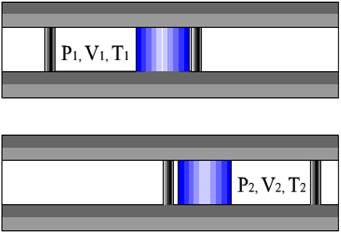
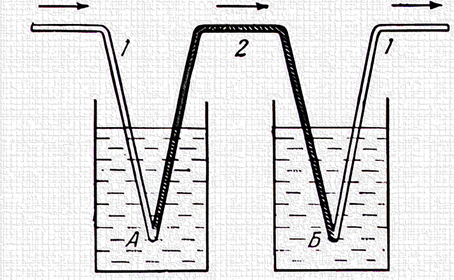
Ранка-Хілша (рис. 2.3) – розділення газу або рідини під
час закручування в циліндричній
або конічній камері на дві фракції. На периферії утворюється закручений потік з більшою температурою, а
в центрі ‒ закручений
охолоджений потік, причому обертання в центрі відбувається в ту ж
сторону, що і на периферії.
Ефект, що виникає під час подавання стисненого повітря з температурою, яка дорівнює
температурі навколишнього
середовища, по тангенціальному
вводу в трубу зумовлює те, що
температура повітря біля стінок труби буде вищою, а в центрі ‒ нижчою, ніж температура повітря на вході в трубу. Таке явище викликане тим, що швидкість обертання повітря в трубі є різною: біля центральної частини вона більша, ніж на периферії. Якщо розділити периферійну і центральну частини потоку, то можна отримати потоки повітря з низькою i високою
температурами. Утворення охолодженого
та нагрітого потоків є
результатом перерозподілу енергії
стиснутого газу, що входить до вихрової
трубки.
Незважаючи
на порівняно низьку енергетичну ефективність процесу вихрового
температурного розділення газів,
іноді доцільно використовувати вихрові
холодильно-нагрівні апарати.
Однак, суттєвим
недоліком вихрової труби є порівняно низька термодинамічна ефективність
процесу енергетичного розділення, тому під час використання вихрових труб y складі холодильно-нагрівних установок прагнуть до максимальної
утилізації енергії потоків, що виробляються y вихровій трубці.
Ефект Пельтьє ‒ термоелектричне явище, під час якого відбувається виділення або поглинання тепла під час проходження електричного струму
в місці контакту (спаю) двох
різнорідних провідників. Причина виникнення явища Пельтьє.
На контакті двох речовин є контактна різниця потенціалів, яка створює внутрішнє контактне поле. Якщо через контакт протікає електричний струм, то це поле
буде або сприяти проходженню струму, або перешкоджати. Якщо струм йде проти контактного поля, то зовнішнє джерело має витратити додаткову енергію, яка виділяється в контакті, що призведе до його нагрівання. Якщо ж струм йде за напрямом контактного поля, то він
може підтримуватися цим полем, яке і здійснює
роботу з переміщення зарядів.
Необхідна для цього енергія відбирається у речовини, що призводить до охолодження його в місці контакту. Ефект Пельтьє
пояснюється тим, що середня енергія
носіїв заряду по обидві сторони контакту різна. Під час переходу електронів з
одного провідника в інший
вони або передають надлишкову енергію атомам (поблизу контакту виділяється
тепло), або поповнюють енергію за рахунок атомів (поглинається теплота). Під час переходу з напівпровідника
в метал електрони віддають надлишкову енергію. Якщо напрям струму зміниться на протилежний, то з металу в напівпровідник можуть вийти тільки ті електрони, які володіють достатньою енергією. Теплова рівновага порушується і відновлюється за рахунок теплових коливань кристалічної решітки. При цьому поглинається теплота Пельтьє. Наявність тепла Пельтьє означає, що кінетична енергія електронів під час переходу з одного матеріалу
в іншій змінилася. На
рис. 2.4 зображено схему досліду
з вимірювання тепла Пельтьє,
де в спайці А струм йде від металу 1 до металу 2, а в спайці Б ‒ навпаки. Отже, в одному калориметрі відбувається нагрівання, а в іншому ‒ охолодження.
Сорбційні холодильні
машини відносяться до класу тепловикористальних
машин. Сорбцією –
від латинського слова «sorbco» (поглинати, втягувати) називається будь-який природний процес поглинання однієї речовини іншою (сорбентом) незалежно від механізму поглинання. Залежно від механізму поглинання розрізняють адсорбцію і абсорбцію.
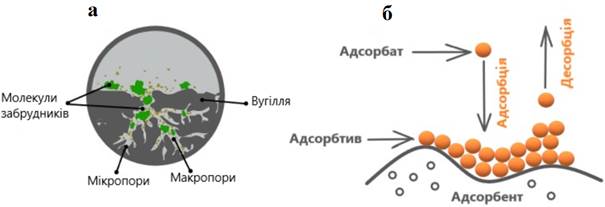
Для
того, щоб одне тіло поглинало інше необхідно існування сили, яка здатна рухати цей процес (рис. 2.6). Рушійною силою сорбційних
машин є відсутність механічної
рівноваги між станом речовини, що поглинається, всередині
сорбенту, на його поверхні
і далеко від нього. Адсорбція обмежується
насиченням поверхні
твердого тіла. Абсорбція супроводжується
хімічною реакцією з утворенням нової речовини, яка в хімії називається (хемосорбцією). Таким
чином, сорбційні процеси відрізняються механізмом, з чого випливає і назва цих машин. Робочою речовиною
в таких машинах є суміш холодильного агента (робочої речовини) і сорбенту.
Фазовий стан холодильного агента – пара. Процеси внутрішнього
охолодження робочого тіла й відводу тепла від об’єкта охолодження
здійснюються в абсорбційних
холодильних машинах так само, як і в парових компресійних
установках. Їхня основна особливість полягає в тому, що вони споживають не механічну, а теплову енергію. Звідси випливають їхні достоїнства й недоліки. Абсорбційні машини прості за конструкцією (крім насосів для перекачування рідини, у них немає інших механізмів,
що рухаються), дешеві у виготовленні, надійні, малошумні. Їх можна розміщати
поза приміщеннями на відкритих
майданчиках під легкими навісами для захисту від опадів. Головний
недолік – невисока енергетична ефективність. Для вироблення однакової кількості холоду абсорбційним холодильним машинам потрібно більше енергії, ніж парокомпресійним. Це пояснюється тим, що в агрегаті
холодильника абсорбційного типу, що живиться від електромережі, споживана електрична енергія спочатку перетворюється в теплову, яка потім забезпечує вироблення холоду. У
великих промислових установках використовувати
електроенергію необов’язково.
Якщо ж на об’єкті є надлишкові теплові ресурси, у
вигляді пари або гарячої рідини (тепло яких іноді навіть
«скидають» у навколишнє середовище), то абсорбційні машини стають вигідніші парокомпресійних. Саме в таких випадках головним чином і використовують
абсорбційні машини. Дію термохімічного
компресора засновано на використанні
екзотермічних процесів змішання й ендотермічних – поділу.
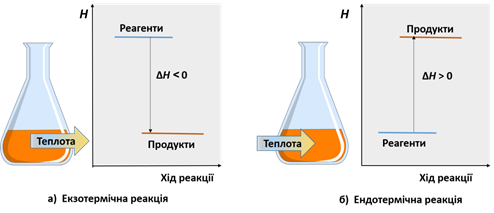
Ендотермічна реакція ‒ хімічна
реакція, під час якої реагуюча система поглинає теплоту з навколишнього
середовища. Екзотермічна реакція ‒ хімічна реакція, під час якої з реагуючої системи в навколишнє середовище виділяється теплота. В абсорбційних
установках, як правило, застосовуються дві речовини – робочий агент і абсорбент (поглинач),
що мають різні нормальні температури кипіння й мають властивість утворювати за адіабатного змішання суміші з температурою,
яка відмінна від
температур речовин, що змішуються. Для створення
холодильного циклу в абсорбційній холодильній установці рідкі абсорбенти мають з достатньою швидкістю поглинати холодоагент і за однакового
тиску температура їх кипіння має бути значно вищою за температури кипіння холодоагента. Вимоги до бінарної
суміші, застосовуваної
для абсорбційних холодильних
установок, відносно впливу
її на метали, пожежної безпеки, санітарії й гігієни не відрізняються від вимог, взагалі
пропонованих до холодоагентів. Найбільше застосування
одержали водоаміачні абсорбційні
установки, у яких аміак є
холодоагентом, а вода – поглиначем
– абсорбентом. Аміак активно абсорбується
водою: за 0 °С у одному обсязі води розчиняється до 1148 обсягів пароподібного аміаку. Поглинання або абсорбція рідкого аміаку у воді супроводжується значним виділенням тепла (близько 190
ккал на 1 кг аміаку). Ще більша кількість тепла виділяється під час розчинення у воді парів аміаку, тому що при цьому відбувається виділення теплоти паротворення, у середньому рівної 300 ккал/кг. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||