|
|
ФІЗИЧНА І КОЛОЇДНА ХІМІЯ Електронний посібник |
|||||||||||||||||||||||||||||||||||||||
|
|
МІКРОГЕТЕРОГЕННІ СИСТЕМИ |
|||||||||||||||||||||||||||||||||||||||
|
8.1. Загальна характеристика мікрогетерогенних
систем. 8.2. Суспензії та їх стабілізація. 8.3. Емульсії, їх класифікація і методи одержання. 8.4. Піна: її утворення, стабілізація та руйнування. 8.5. Аерозолі: одержання їх властивості, способи руйнування. 8.6. Порошки: властивості та добування. 8.1. Загальна характеристика мікрогетерогенних
систем До мікрогенних
систем відносяться системи
меншої дисперсності, ніж золі. Розмір частинок у таких системах від 10-7до
10-4м. У мікрогетерогенних і грубодисперсних системах не мають місця такі
молекулярно-кінетичні властивості, як броунівський рух, дифузія, осмотичний
тиск. У більшості випадків частинки дисперсної фази можна спостерігати за
допомогою звичайного мікроскопу. До
мікрогетерогенних систем відносять
системи з газоподібним дисперсійним середовищем
(аерозолі, порошки) та із рідким дисперсійним середовищем (суспензії,
емульсії, піни). У мікрогетерогенних
і грубодисперсних систем є спільні ознаки з
колоїдними системами. Вони гетерогенні, тобто складаються із декількох фаз з
достатньо великою поверхнею розділу фаз, а відповідно, зі значним запасом
поверхневої енергії. Тому як і колоїдні
системи, мікрогетерогенні
та грубодисперсні системи
термодинамічно нерівноважені
і в них існує тенденція до самодовільного зменшення дисперсності шляхом
агрегації частинок дисперсної фази. Агрегативна стійкість таких систем, за винятком систем з газоподібним
дисперсійним середовищем, також зумовлена стабілізатором, який адсорбується
на частинках дисперсної фази. 8.2. Суспензії та їх стабілізація Суспензія – мікрогетерогенна система, в якій тверда дисперсна фаза розподілена в рідкому дисперсійному
середовищі.
Рис. 8.2.1.
Приклад суспензії: кров, пиво Деякі з властивостей
суспензій, схожі з аналогічними за фазовим станом ультрагетерогенних
систем – золями, але мають низку суттєвих відмінностей. Це ілюструє табл.1. Таблиця
1 Основні
відмінності та схожі характеристики суспензій і ліозолей
Залежно від
відносного вмісту дисперсної фази, суспензії поділяють на три типи: розведені,
концентровані та висококонцентровані. Висококонцентровані
суспензії називають пастами.. Одержання
суспензій Для одержання
суспензій використовують методи диспергування і конденсації. Практично,
найчастіше, суспензії отримують диспергуванням нерозчинених твердих речовин у
рідкому середовищі або скаламученням у цьому середовищі попередньо одержаного
порошку. Стійкість суспензій Суспензії є седиментаційно нестійкими системами внаслідок дуже великого розміру частинок
(10-6 – 10-4м). Дисперсна фаза за порівняно короткий
час цілком випадає в осад. Агрегативна стійкість суспензій зумовлюється тими ж факторами, що і стійкість ліозолей: електростатичними, адсорбційно-сольватними і структурно-механічними.
Рис. 8.2.2. Седиментаційно нестійкі суспензії Для стабілізації
суспензій використовують високомолекулярні речовини. Захисний шар цих речовин
забезпечує гідратацію частинок, крім того, довгі ланцюги
макромолекул охоплюють частинки,
утворюючи структурні гратки. Агрегативно стійкими, як правило, є суспензії гідрофільних
мінеральних порошків (СаСО3, А12О3, BaSО4) у воді та суспензій
гідрофобної сажі в бензені, оскільки вода добре змочує мінеральні порошки, а бензен – сажу. Якщо ж змочування недостатнє, то сольватна оболонка не утворюється і відбувається коагуляція. У таких випадках під
час коагуляції суспензій утворюються великі частинки дисперсної фази, які
погано змочуються середовищем і піднімаються на поверхню. Таке явище
називається флокуляцією.
Рис. 8.2.3. Ступінь флокуляції пива залежить від PYF –
потенціалу (що більший PYF-потенціал, то менш мутний зразок пива) Флокуля́ція (англ. Flocculation, нім. Ausflockung f, Flockung f, Flocken n) – утворення нетривких пухких агрегатів невизначеної форми з дрібних частинок дисперсної фази, які знаходяться в завислому стані в рідкому чи газовому середовищі.
Рис. 8.2.4. Флокуляція У рідких дисперсних системах (золях, суспензіях,
емульсіях,
латексах)
флокуляція спричинюється спеціальними речовинами – флокулянтами і реагентами,
які ліофобізують поверхню частинок, а також
тепловими, механічними, магнітними та іншими зовнішніми впливами. У присутності флокулянтів та ліофобізуючих реагентів відбувається зчеплення частинок дисперсної фази і виникнення просторових
дисперсних структур. Застосування
суспензій та паст Суспензії мають сферу
широкого застосування. Так, розведені суспензії використовують
під час фарбування, наприклад, тканин, а концентровані – у керамічній
промисловості та виробництві будівельних матеріалів. Суспензії, завдяки
адсорбційним властивостям, широко використовують як каталізатори у гетерогенному
каталізі. До суспензій
відносяться кукурудзяний крохмаль, неочищені рослинні олії,
дифузійний сік цукрових буряків (полікомпонентна система, в якій
міститься 16 – 17 % сухих речовин, з них 14 – 15 %
цукрози і 2 % нецукрів). Диспенсійним
середовищем суспензії розплаву
какао є какао-масло, а дисперсною фазою – тверді частинки какао і кристали
цукру. Суспензії отримують у
процесі приготування їжі (наприклад, протерті супи).
Рис. 8.2.5. Суспензії: 1) протерті супи; 2) пасти; 3) дифузійний сік цукрових буряків Адсорбційне
рафінування масла засноване на використанні суспензії, яка утворюється із частинок бентонітових глин, що виконують роль адсорбента. Для приготування паст
використовують рідини, що мають підвищену в'язкість і температуру кипіння.
Так, деякі сорти зубної пасти готують шляхом змішування крейди з в'язкою
рідиною, яку добувають у процесі заварювання крохмалю в гліцериновому розчині
з додаванням невеликої кількості ПАР. Пасти деяких харчових
мас складаються з кристалів сахарози, яка є дисперсною фазою, а дисперсійним
середовищем є розчин сахарози і мальтози. Додавання невеликої
кількості ПАР може надавати пастам текучості. Наприклад, паста А12О3
у вазеліновому маслі (цю пасту інколи застосовують у харчовій промисловості
для допоміжних цілей) надає крихкість. Під час додавання невеликої кількості
олеїнової кислоти ця паста набуває здатності текучості. 8.3. Емульсії, їх класифікація і методи одержання Емульсії – це мікрогетерогенні
дисперсні системи, в яких
дисперсна фаза і дисперсійне середовище складаються із рідни, що практично
нерозчинні одна в одній. Радіус частинок
дисперсної фази в емульсіях 10-7 – 10-5м. До емульсій належать
молоко, вершкове масло, маргарин, сметана, майонез, сік рослин –
каучуконосів, нафта тощо.
Рис. 8.3.1. Приклад емульсій: 1) дерева каучуконоси (збір натурального природного латексу); 2) маргарин; 3) молоко Емульсії
класифікують за характером дисперсної фази і дисперсійного середовища.
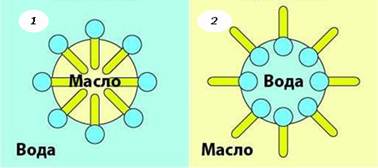
Рис. 8.3.2. Класифікація емульсій: 1) прямі ( масло у воді м/в); 2) зворотні ( вода в маслі в/м) Прямі емульсії
(емульсії 1-го ряду), що складаються із полярного дисперсійного середовища
(умовно – вода) і неполярної дисперсної фази (умовно – масло); їх позначають
м/в; Зворотні (емульсії 2-го ряду) – мають неполярне дисперсійне середовище (масло) і
полярну дисперсійну фазу (вода); їх умовно позначають в/м. Тип емульсії залежить
від співвідношення об'ємів рідких фаз, умов емульгування та інших факторів,
але головну роль відіграє природа емульгатора. Для встановлення типу
емульсії розроблені різні методи. Найпростішим із них є метод забарвлення фаз. Невеликий об'єм
емульсії перемішують на предметному склі з водорозчинним барвником,
наприклад, метиленовим блакитним. Якщо емульсія типу в/м, то під мікроскопом
блакитні кульки видно на безбарвному фоні. Якщо емульсія типу м/в – на
блакитному фоні
маємо безбарвні кульки. Інколи застосовують
неполярний барвник – судан. Він забарвлює неполярну рідину в червоний колір.
Рис. 8.3.3. Барвник судан І – структурна формула Добування емульсій Одним із методів
добування емульсії є подрібнення речовини дисперсної фази. Для цього, до
дисперсійного середовища в присутності емульгатора за сильного перемішування
додають речовину, що є дисперсною фазою. Добування емульсій
Другий метод полягає в
утворенні плівок та їх розриву на дрібні краплини. Плівка, яка утворюється за
повільного додавання рідини до дисперсійного середовища, розривається
пухирцями повітря, які виходять із отвору трубки на дні посудини. При цьому ступінь
дисперсності емульсії та її стійкість залежать від швидкості перемішування,
введення речовини дисперсної фази та її кількості, природи та концентрації
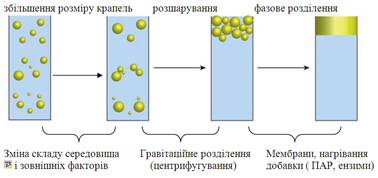
емульгатора, температури та pH середовища. Стійкість емульсій Емульсії седиментаційно та агрегативно нестійкі, тому що величина
частинок і їх маса значно більша, ніж у колоїдних розчинах.
Рис. 8.3.4.
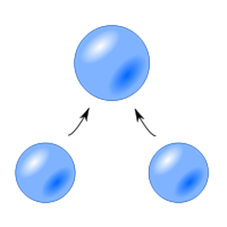
Стійкість емульсії Коалесценція – злиття
крапель емульсії, що відбувається самодовільно і призводить до розшарування рідини.
Рис. 8.3.5.
Коалесценція крапель Для надання емульсії
стійкості застосовують емульгатори або стабілізатори. Емульгатори
– це речовини, що
стабілізують емульсію.
Рис. 8.3.6. Дія емульгатора Емульгатор повинен
бути подібним до тієї рідини, яка утворює дисперсійне середовище. Так,
емульсії типу масло/вода (далі – м/в) стабілізуються розчинними у воді високомолекулярними сполуками, наприклад, білками або водорозчинними милами
(милами лужних металів).
Емульгаторами під час добування емульсії типу вода/масло (далі – в/м), є
високомолекулярні речовини, нерозчинні у воді, але добре розчинні в
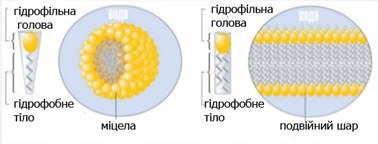
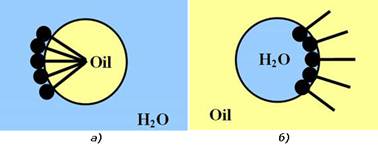
неполярних розчинниках (каучук, смоли). В адсорбційному шарі
молекули емульгатора, що містять полярні та неполярні групи (мила, білки),
орієнтуються полярною частиною до полярної рідини, а неполярною – до
неполярної. На поверхні крапель рідини в емульсіях типу м/в і в/м буде
спостерігатись протилежна орієнтація молекул таких емульгаторів (рис. 8.3.2).
Рис. 8.3.7. Стабілізація емульсій: а) м/в; б) в/м Подібні оболонки із
поверхнево-активних речовин на поверхні крапель емульсії досить міцні та
пружні. Під час зіткнення
частин вони, як слід, не руйнуються – емульсії набувають стійкості. Крім високомолекулярних сполук і ПАР емульгаторами емульсій як першого, так і другого типів
можуть бути порошки, так звані тверді емульгатори. Однак їх ефективність
значно менша. Порошки мають бути високодисперсними і обов'язково повинні
краще змочуватись тією рідиною, яка служить дисперсійним середовищем; в цьому
випадку більша частина твердих частинок буде знаходитись із зовнішнього боку
крапельок, утворюючи оболонки високої міцності, які оберігають їх від
коалесценції під час зіткнення. Емульсії типу м/в
добре стабілізують гідрофільні
порошки, наприклад, борошно,
крейду, ферум (III)
оксид, алюмосилікати, а емульсії
типу в/м добре стабілізують гідрофобні порошки, наприклад, сажу. За деяких умов
емульсії одного типу можуть перетворюватись на емульсії другого типу. Це
явище має назву перетворення фаз
емульсій. Його викликають
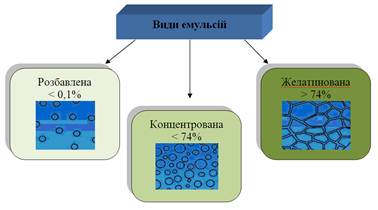
додаванням емульгатора протилежного типу, тобто змінюють природу емульгатора. За агрегативною стійкістю емульсії можна поділити на дві
великі групи – розбавлені та концентровані.
Розбавлені емульсії –
дисперсна фаза
становить не більше 0,1 % всього об'єму. Вони стійкі без емульгаторів. Їх
стабілізують невеликими домішками електролітів. У концентрованих
емульсіях дисперсна фаза може
займати велику частину всього об'єму. Якщо вважати, що всі крапельки однакові
за розміром і строго кулеподібні, то за найщільнішого упакування кульок, вони
становитимуть 74 % від загального об'єму системи, а 26 % об'єму припадає на
проміжки між крапельками, тобто на дисперсійне середовище. За більшої
концентрації дисперсної фази відбувається деформація кульок: із кулеподібних
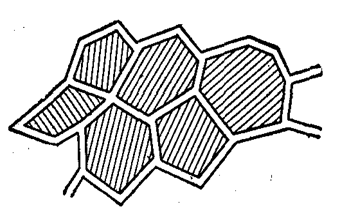
вони перетворюються на багатогранники. Такі емульсії називаються желатинованими.
Рис. 8.3.8. Схема желатинованої емульсії Желатиновані
емульсії твердоподібні та
характеризуються напруженням зрушення. Прикладом таких емульсій є вершкове
масло, маргарин, густі креми, майонез. Для них наявність емульгатора є
обов'язковим. Руйнування
емульсій називається деемульгування.
В деяких випадках
деемульгування має позитивне значення. Наприклад, під час збивання вершків. Руйнування
емульсій можна викликати такими методами:
Дією
електричного струму або електролітів викликають руйнування емульсій типу
«вода в нафті», стабілізованих електричним зарядом частинок. Значення
емульсій. Молоко
– це полідисперсна
система, компоненти якої знаходяться в різній ступені дисперсності. Тепле
молоко містить жир в емульгованому
стані, а білкові речовини і частина солей – в колоїдному, друга частина
солей – в розчиненому стані. Під
час зберігання молока утворюється шар концентрованої емульсії – вершків. У
промисловості молоко гомогенізують. У процесі гомогенізації великі жирові
крапельки молока зменшуються в декілька разів. Таке гомогенізоване молоко
дуже стійке і не утворює шар вершків протягом декількох місяців. Майонез
– є концентрованою
емульсією рослинної олії типу м/в. Дисперсійним середовищем є вода, що
містить яєчні жовтки, оцет, гірчицю, цукор, спеції.
Маргарин – це концентрована емульсія типу в/м, в якій дисперсною фазою
є вода, а дисперсним середовищем – очищений від домішок харчовий жир, який
добувають із соєвих бобів, соняшникової або кукурудзяної олії. Крім того, до
маргарину додають вітаміни, барвники та інші речовини. Вершкове масло – це висококонцентрована, структурована система, до складу якої
входять пряма і зворотна емульсії – в більшій кількості, в/м, і частково в/м.
Емульсії відіграють важливу роль у життєдіяльності організму людини. До
складу крові входить емульсія, дисперсною фазою якої є еритроцити, а
емульгаторами – білки. Жири, необхідна складова частина продуктів харчування,
нерозчинні у воді, засвоюються тільки в емульгованому стані. Як
емульгатор виступає жовч, до складу якої входять жовчні кислоти – моно-карбонові оксикислоти, що відносяться до класу
стероїдів. За відносно високих
значень рН, рівних
8,0 – 8,5, утворюються солі жовчних кислот. Ці солі є добрими емульгаторами.
Емульсії широко застосовують у медицині, виробництві, косметичних засобах,
переробці нафти, виготовленні мастил, фарб, мийних засобів тощо. 8.4. Піна: її утворення, стабілізація та руйнування Піна – висококонцентрована
грубодисперсна система, в якій
дисперсійне середовище рідина, а дисперсна фаза – газ.
Рис. 8.4.1.
Приклади піни Газові бульбашки в
піні мають великі розміри (від міліметрів до сантиметрів), у порівнянні з
іншими подібними системами. При цьому, бульбашки, завдяки деформації, формою
наближаються до багатогранників. Якщо об'єм дисперсної фази перевищує об'єм
рідкої фази у 2 – 10 разів, то газові бульбашки набувають кулястої форми.
Якщо концентрація дисперсної фази (газу) в системі невелика і бульбашки газу
не зв'язані між собою, а вільно переміщуються в рідині, то ця система є
емульсією газу в рідині. Основними показниками,
що характеризують піну є: Пінявість (кратність)
– відношення об'єму
піни до об'єму вихідного розчину піноутворювача:
де Vг
– об'єм газу; Vр – об'єм рідини. Якщо β >
10, то утворюється «волога» піна, яка складається із сферичних бульбашок,
розділених товстими прошарками. Для «сухих» пін з
тонкими прошарками – стінки
поліедричних комірок, заповнених газом, β
досягає значення
1000. У цьому випадку піна має таку саму коміркову структуру, як і
висококонцентрована емульсія. Дисперсність – визначається середнім розміром бульбашок і середньою
товщиною плівок рідини (розмір плівок сягає 10-3 –10-2м). Стійкість – час, що витрачається на самодовільне руйнування піни з моменту
її утворення.
Рис. 8.4.2. Піна: 1) мильна піна; 2) флотаційна піна, флотація міді; 3) флотаційна піна – флотація вугілля Стійкість піни (час життя) залежить від концентрації і природи
піноутворювача. Час існування піни – від декількох секунд до декількох годин.
Низькомолекулярні ПАР-спирти, жирні кислоти утворюють малостійку піну, час існування якої не перевищує 20 сек. Мило дає стійкішу піну. Максимальна стійкість піни відповідає милам з середньою довжиною вуглеводневого
радикалу.
Рис. 8.4.3. Стійкість піни Глюкозиди (сапоніни), таніди,
барвники і, особливо, білки утворюють стійку піну,
причому стійкість неперервно зростає з підвищенням концентрації. Стабільність високостійкості піни
зумовлюється структурно-механічними
властивостями адсорбційних
шарів піноутворювача. Ці шари, з одного боку,
уповільнюють стікання рідин, а з іншого – надають плівці піни високу
структурну в'язкість і
механічну міцність. Також на стійкість
піни впливають температура та в'язкість
дисперсійного середовища,
рН. Піноутворення Піну одержують
методами диспергування та конденсації. За методом диспергування рідину, яка
не повністю заповнила посудину, збовтують або перемішують, пропускаючи через
неї газ. У процесі перемішування рідина захоплює повітря, внаслідок чого на
поверхні утворюється піна. У методі конденсації
відбувається хімічна реакція, результатом якої є утворення в рідині газової
фази. Наприклад, для надання пористості хлібобулочним виробам, що добувають із прісного тіста, використовують натрій гідрогенкарбонат (харчова сода)
і амоній
карбонат, що розкладаються за
рівнянням: 2NaHCO3 = Na2CO3
+ CO2 + H2O (NH4)2CO3
= 2NH3 + H2O + CO2 Під час виготовлення дріжджового тіста, розпушування відбувається за рахунок
карбон (IV) оксиду, що утворюється за спиртового бродіння гексоз:
Рис. 8.4.4. Піноутворення: 1) в хлібобулочних виробах; 2) в капучино; 3) в газованих
напоях Обов'язковою умовою
існування піни є наявність поверхнево-активних речовин (ПАР). У деяких випадках
утворення піни небажано, наприклад, у виробництві мила, дріжджів, цукру.
Руйнування піни – піногасіння
– досягають механічною
дією на піну, продуваючи повітря над поверхнею розчину, що піниться, або
фізико-хімічним шляхом, замінюючи в плівці механічно міцну речовину іншою
речовиною, яка добре адсорбується, але не дає міцних плівок. Ефективно гасять піну естери, спирти, карбонові кислоти. Так, наприклад, одна крапля естеру повністю руйнує піну в стакані пива. Гасіння піни ультразвуком
Значення піни Таблиця
1 Можливі
джерела утворення, тип і форма деяких пін у харчовій промисловості і
продуктах харчування
Значне піноутворення цукрового
сиропу зумовлене сапоніном,
а також такими речовинам, як гумінова кислота і
продукти розпаду білків. Піноутворення відбувається як в об'ємі рідини, так і на її поверхні. Стійкість піни продуктів бродіння (пива, солодових напоїв) викликана наявністю альбуміну, желатину, солодового екстракту та таніну. Наявність нітрогеновмісних речовин зумовлює спінювання плодово-ягідного варення та екстрактів чайного листа. Особливу роль піна
відіграє під час збивання масла із вершків або молока.
Рис. 8.4.5. Мікрофотографія піни яєчного білка (х 400
разів) У рідкому
дисперсійному середовищі на бульбашках піни концентруються крапельки жиру. Внаслідок
коагуляції крапель утворюється масляна дисперсна фаза, оточена водним
середовищем. Пряма емульсія м/в переходить в обернену в/м; цьому сприяє піна. Позитивні властивості
піни проявляються інколи в домашніх умовах, зокрема, під час виготовлення варення.
В ягодах містяться ПАР, які сприяють утворенню піни із бульбашок повітря.
Бульбашки випливають на поверхню і захоплюють різні забруднення, забезпечуючи
тим самим очищення продуктів. Піноутворювачем є сапонін, а цукор збільшує в'язкість і підвищує стійкість піни.
Піноутворення відіграє важливу роль у процесі засвоєння їжі. Слина утворює
високодисперсну і міцну піну, внаслідок чого процес змочування їжі
відбувається всього за 16 – 18 секунд. Піни широко
застосовуються в різних галузях господарства, промисловості, медицині та в
косметичних засобах. 8.5. Аерозолі: одержання, їх властивості, способи руйнування Аерозолі –
це дисперсні
системи, в яких дисперсною фазою є | рідина або тверде тіло, а дисперсійним
середовищем – газ. В аерозолях розмір
частинок становить від 10-9 – 10-3 м. Ці системи
відносяться до полідисперсних. Аерозолі часто
зустрічаються в довкіллі. Серед природних аерозолів доречно згадати такі
різновиди: 1) туман
– аерозольна дисперсна система, що складається з рідкої дисперсної
фази (краплі рідини 10 мкм) і газового дисперсійного
середовища (рис. 8.5.1 а); 2) дим
– аерозольна дисперсна система, що складається з твердої дисперсної фази
(частинки 0,1 – 5 мкм) і газового дисперсійного середовища (рис. 8.5.1б); 3) смог
– аерозольна дисперсна система, що складається з суміші твердої і рідкої
дисперсних фаз (частинки 0,1 – 50 мкм) і газового дисперсійного
середовища (рис. 8.5.1в); 4) пил
– аерозольна дисперсна система, що складається з твердої дисперсної фази
(частинки 10 – 100 мкм) і газового дисперсійного середовища (рис. 8.5.1г).
Рис. 8.5.1. Приклади аерозольних дисперсних систем: а) туман; б) дим; в) смог;
г) пил Наприклад, розміри часток (у см.) деяких типових аерозолів: • туман (Н2О) 5·10-5 • шаруваті хмари 1·10-4 –1·10-3
• дощові хмари 1·10-3 –1·10-2
• H2SO4
(туман) 1·10-4–1·10-3
• Zn
(дим) 5·10-6 • тютюновий дим 1·10-5 –1·10-4
• топковий дим 1·10-5 –1·10-2
• Р2О5
(дим) 5·10-4
–1·10-4 Аерозолі виникають за
різних технологічних процесів, наприклад, борошняний пил на млинах, пил
цукрової пудри, порошку какао на кондитерських виробництвах. Найчастіше аерозолі
класифікують за агрегатним станом дисперсної фази. Аерозолі з рідкою
дисперсною фазою – тумани, з твердими частинками – дими. Добування аерозолів В основу
конденсаційного утворення аерозолів покладено процес конденсації насиченої
пари. Методами диспергування одержують
полідисперсні та седиментаційно
нестійкі дими і тумани (розмір частинок більше 10-6 м). Седиментаційно стійкі дими і тумани одержують конденсаційними методами. Процес конденсації
пари залежить від таких факторів:
Хімічні процеси, що
призводять до утворення аерозолів, різноманітні, але суть їх полягає в тому, що газоподібні речовини в результаті
реакцій дають тверді або рідкі продукти, які мають дуже малу пружність пари. Розглянемо класичний
приклад утворення диму під час проходження хімічної реакції. Якщо з'єднати
два стакани, один з яких заповнений хлороводнем, а другий – амоніаком, то
утворюється дим амоній хлориду:
Дим без
вогню. Взаємодія розчину амоніаку з концентрованими кислотами.
Під час згоряння
магнію утворюється дим, що складається з магній оксиду:
Аерозолі - це агрегативно нестійкі системи. Але таким
системам – з газоподібним дисперсійним
середовищем можна надати агрегативну стійкість, для чого необхідно штучно надати їм високий електричний заряд, в
результаті їх частинки не будуть з'єднуватись. Це єдиний шлях стабілізації
дисперсних систем з газоподібним дисперсійним середовищем. Однак, у низці
випадків, виникає потреба не стабілізувати, а навпаки, руйнувати дими та
тумани, як шкідливі та небажані явища. Існують дві групи
методів, які використовують для боротьби з димом і туманом: електричні методи прискорення
коагуляції частинок та механічні,
за допомогою яких тверді або рідкі частинки відокремлюються від газоподібного
середовища. Ультразвукова коагуляція аерозолю
Перша група методів
базується на електрофорезі – русі заряджених частинок в електричному полі. Ці
методи досягаються лише в електричному полі високої напруги (до 90000 В). За
такої високої напруги катод посилає велику кількість електронів, які
пронизують повітря, частинки аерозолю отримують високий від'ємний заряд і
досить швидко притягуються до позитивного електрода. Такий принцип покладено
в основу роботи електрофільтра. За допомогою електрофільтрів у великих містах
в обов'язковому порядку очищують димові гази, які випускають в атмосферу
промислові підприємства, а також уловлюють оксиди металів, різні види сажі,
цемент та ін. Серед механічних
методів руйнування диму та туману найбільше значення має фільтрація.
Використовують фільтри із паперу та пористих матеріалів. Осідання частинок на
фільтрі може відбуватись з різних причин. Дуже дрібні частинки досягають
поверхні волокна завдяки броунівському руху і прилипають до неї. Більші
відкидаються на стінки силою інерції, втрачають швидкість і залишаються в
порах фільтра. Нарешті, найбільші можуть затримуватись механічно, так само,
як сито затримує частинки більші, ніж його отвори. Головну роль під час
фільтрації відіграють, звичайно, не розміри пор, а їх звивистість. Повітряний фільтр
Кінетичні
властивості аерозолів зв'язані також з такими специфічними процесами, як термофорез, фотофорез
і термопреципітація.
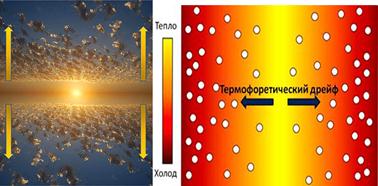
•
Термофорез – це рух частинок аерозолю в
напрямку зниження температури, зумовлений тим, що з боку більшої температури
молекули газу налітають на частинку з більшою швидкістю, ніж на менш
нагрітий, і тому надають частинці імпульс у напрямку зниження температури.
Рис. 8.5.2. Алегорія. Хмари-молекули
спрямовуються геть від сонячного тепла • Фотофорез
–
це рух частинок при односторонньому освітленні під тиском світлових променів. Розподіл температури всередині освітленої
частинки залежно від розміру, форми, прозорості й коефіцієнта заломлення може
бути різним, і частинка може рухатися як у напрямку променя світла (позитивний фотофорез), так і назустріч йому (негативний фотофорез). • Термопреципітація
зумовлена осіданням частинок аерозолю на холодних поверхнях, бо під час зіткнення
з такою поверхнею частинки аерозолю втрачають кінетичну енергію. Цим
пояснюється осадженням пилу на стінках та стелях поблизу радіаторів, ламп,
печей та ін. Явища
термофорезу і фотофорезу спостерігаються в атмосфері під час утворення й переміщення хмар і туманів. За оптичними
властивостями аерозолі дуже близькі до колоїдних розчинів. Для них також
характерне розсіювання світла. Однак, внаслідок великої різниці в показниках
заломлення газового дисперсійного середовища і рідкої або твердої дисперсної
фази, розсіювання світла у аерозолів більш інтенсивніше і вони не пропускають
світло. На цьому засноване використання маскувальних димових завіс. Завдяки сильному світлорозсіюванню
аерозолей, що знаходяться у верхньому шарі
атмосфери, зменшується інтенсивність сонячної радіації, що впливає, таким
чином, на кліматичні умови. Застосування аерозолів Після розпилювання
емульсій або суспензій в утворений аерозоль вводять потік гарячого газу,
здійснюючи так звану «розпилювальну сушку», її застосовують для добування
сухого молока, розчиненої кави та інших продуктів. Під час коптіння м'ясних
та рибних продуктів використовують дим, який надає цим продуктам відповідний
смак.
Рис. 2.5.3. Аерозолі: 1) дим під час копчення м’ясних та рибних виробів; 2) вугільний пил; 3) борошняний пил Під час виробництва
продуктів харчування, їх зберіганні та транспортуванні утворюється пил.
Залежно від джерела аерозолю цей пил може бути неорганічний, органічний або змішаний. До органічних відносяться:
рослинний (крохмальний, борошняний, цукровий, чайний, тютюновий та ін.) і
тваринний (кістковий, шерстяний та ін.) пил. Пил неорганічного походження
утворюється, наприклад, під час переробки насіння соняшнику (в ньому
міститься понад 20 хімічних елементів). Борошно, крохмаль, цукор
у вигляді пилу можуть вибухати (пірофорні властивості).
Температура самозаймання борошна різних сортів знаходиться в межах 1023 –
1148 К, а для аерозолів бурякового цукру вона складає 798К. Самозаймання
зумовлене великим надлишком поверхневої енергії, швидким окисненням поверхні
аерозольних частинок. Таким чином,
аерозолі, утворені із легкозаймистих речовин, поводять себе як суміші
горючого газу у повітрі. За певної концентрації вони сприяють розповсюдженню
полум'я, а в замкнутому просторі можуть викликати вибух. Мінімальну
концентрацію пилу, яка може призвести до спалахування, визначають дослідним
шляхом. Так, наприклад, для деяких харчових мас в аерозольному стані вона
становить (в г/м3): борошна – 52, глюкози – 225, комбікормів – 272
– 300, пшеничних висівок – 150, крохмалю – 58 – 98, цукру – 66, какао-порошку
– 103, сухого молока – 94 – 103, картопляного борошна – 225, соєвого борошна
– 66. Крім
вибухонебезпечності, аерозолі харчових мас мають токсичну дію. Так,
борошняний пил, особливо під час утворення, може викликати такі хвороби, як
астма та кон’юнктивіт. Аерозолі широко застосовують у сільському господарстві, медицині, косметиці, техніці, побуті. 8.6. Порошки: властивості та добування порошків Порошки
– мікрогетерогенні системи,
в яких тверді частинки
дисперсної фази розподілені у газовому дисперсійному середовищі. Розмір частинок у
порошках знаходиться в межах 10-8 –10-4м.
Рис. 8.6.1. Приклади порошків: 1) цукрова пудра; 2) какао; 3) цемент; 4) мінеральні добрива У порошках частинки
дисперсної фази стикаються одна з одною, тому і можуть злипатись. Щоб
запобігти злипанню, попередньо змочені порошки або порошки, в які додають клейкі
речовини, гранулюють шляхом механічного ущільнення. Гранулювання порошків –
це спонтанний процес, який відбувається в міру великої енергії системи в
результаті злипання частинок.
Рис. 8.6.2. Гранулювання порошків Механізм гранулювання
полягає в тому, що частинки порошку під дією молекулярних сил вступають у
енергетичну взаємодію, утворюючи агрегати. Як показав С.С. Воюцький, гранулювання йде краще, якщо у порошок
ввести «зародки». Гранули є однією з лікарських форм, крім того, з них
способом пресування готують таблетки. Порошки, гранули, таблетки складають до
80 % готових лікарських форм сучасної рецептури. Властивості
порошків Однією
із властивостей порошків є текучість. Оцінювання текучості можна зробити за
допомогою кута природного відхилення. Кутом природного відхилення називається
кут, утворений порошком, насипаним у вигляді конусу з горизонтальною
площиною. Що менший кут відхилення, то більша текучість порошку. На величину
текучості впливають:
Якщо
крізь шар порошку, що міститься в циліндрі з пористою дниною, продувати знизу
газ, то порошок почне розширюватись у разі перевищення
градієнтом тиску газу градієнту гідростатичного тиску порошку. Порошок із
великими частинками розширюється рівномірно, контакт між частинками
зберігається, але структура стає пухкішою. У
дрібнодисперсних порошках спостерігається розпад на окремі агрегати, між
якими утворюються канали для проходження значної частини газу. За певної
швидкості пропускання газу, він починає барботувати крізь шар грубих
порошків, що рівномірно розширюються як крізь рідину. Порошок у цьому стані
нагадує рідину, що кипить, і тому називається «киплячим шаром». Частинки
порошку виносяться з
«киплячого шару»,
тобто він видувається. У дрібнодисперсних порошках канали руйнуються, у шарі
відбувається інтенсивне перемішування, безперервне утворення і розпад агрегатів (агрегативна флюїдизація), що
призводить до певного
видування порошку газом. Багато
порошків можна перевести в розширений стан не тільки пропусканням через них
газу, але й просто обережним пересипанням. Пересипання сприяє утворенню
пухкої структури внаслідок проникнення газу між частинками. В такому стані
порошок має велику
текучість і нагадує за цією властивістю рідину. Цю властивість застосовують
для просіювання борошна. Порошки
одержують методом диспергування і
конденсації. Метод
диспергування заснований на подрібненні твердих тіл за допомогою різних
млинів: жорнових, кульових, вібраційних, молоткових та ін.
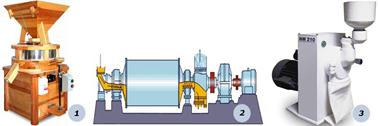
Рис. 8.6.3. Приклади млинів: 1) жорновий; 2)
кульовий СМ 6008; 3) молотковий лабораторний НМ 210 У лабораторних
умовах для порошкування користуються ступкою з товкачиком. У більшості порошків частинки анізометричні, найчастіше – подовжені або пластинчасті.
Ізометричні частинки мають форму сфери багатогранника. Метод конденсації
заснований на добуванні порошків осадженням із розчинів внаслідок коагуляції золей або хімічної реакції. Наприклад,
осаджену крейду добувають за реакцією:
Деякі високодисперсні
порошки отримують спалюючи метали. Наприклад, цинк оксид (цинкові білила) отримують за температури 300 оС, окислюючи пари цинку:
Дисперсність порошків
має важливе практичне значення, наприклад, яскравість забарвлення, криюча здатність фарб, смакові властивості кави, какао, борошна, крохмалю – в значній
мірі залежать від ступеня їх дисперсності.
Що
таке смог «димовий туман»? Смог «димовий туман» – серйозна
екологічна проблема сучасного суспільства. Їдкий туман накриває багато міст –
від Лондона до Пекіна. Смог – це суміш диму, туману і деяких
забруднювальних речовин. Даний термін англійського походження («smog») є злиття двох англійських слів «smoke» і «fog» – «дим» і «туман». Вперше це слово було використано
в Лондоні на початку 1900-х років, щоб описати екологічну ситуацію в місті.
Основні випадки появи смогу часто
пов’язані з інтенсивним рухом автотранспорту, високою температурою повітря,
сонячним світлом і безвітряною погодою. Так, низька швидкість вітру дозволяє
смогу застоюватися в певному районі. Застою може посприяти і температурна
інверсія, за якої тепле повітря біля поверхні землі і всі забруднювачі в
ньому блокуються «кришкою» з холодного повітря. Крім інших шкідливих речовин і газів, у
смогу міститься оксид вуглецю, знайомий нам як чадний газ. Він не помітний
для нас, оскільки не має ні запаху, ні кольору, але його задушливий вплив
може значно вплинути на здоров’я і навіть призвести до загибелі.
Як
боротися зі смогом?
Кожен
може внести свій вклад, щоб запобігти виникненню смогу:
Чому утворюється туман? Туман –
метеорологічне явище, при якому в атмосфері виникає високий вміст водяної пари.
За теплої температури туман являє – це скупчення дрібних крапель води, а за
холодної до них додаються кристалики льоду, які виблискують на сонці. Туман виникає не тільки під час
зіткнення холодного і теплого повітря, а й під час випаровування, наприклад,
над морем або вологою ділянкою суші. Існують так звані сухі тумани, які
складаються не з води, а з диму, пилу і кіптяви. Іноді над містами виникає
суміш сухого і вологого туманів, наприклад, під час викиду у вологе повітря
маси твердих частинок з димових або вихлопних труб. Штучний туман утворюється в результаті
промислової діяльності людини, його ще називають фотохімічним смогом.
Він виникає за появи в атмосфері різних
забруднювальних речовин, таких як продукти горіння палива, пари бензину, хімічних розчинників, фарб, пестицидів, нітратів і т.д.
Питання для самоконтролю 1. Що називається
суспензіями? 4. Де застосовують суспензії і пасти? 8. Наведіть приклади харчових емульсій. 10. Якими методами одержують піни? 12. Що називається аерозолями? 14. Які властивості мають аерозолі? 17. Які властивості мають порошки? 19. Які продукти харчування належать до порошків?
Порошки, способи їх одержання. Вплив розміру
частинок на смакову якість, умови зберігання. Яку емульсію буде стабілізувати сажа: емульсію бензолу
у воді, чи води в бензолі. Поясніть і покажіть на схемі механізм
стабілізації. Встановіть
відповідність між мікрогетерогенними системами (піна,
емульсія, суспензія, аерозоль, порошок) та об’єктами
Лепбук дослівно
з англійської – «наколінна
книга»: «lap» – коліна, «book» – книга. По суті Лепбук – це папка або мінікнижка, в якій багато кишеньок
та конвертиків, що містять необхідний
систематизований матеріал (зокрема ілюстрований) для вивчення і закріплення
знань з теми. Лепбуки
допомагають швидко та
ефективно засвоїти нову інформацію
і закріпити вивчене в пізнавально-ігровій формі. Ці
тематичні посібники мають яскраве оформлення. Під час роботи з тематичним
матеріалом студенти проводять спостереження, виконують завдання, вивчають і
закріплюють інформацію. Згодом, маючи під рукою готову тематичну папку,
студент зможе освіжити свої знання з тієї чи іншої теми. Отже, створіть лепбук для емульсій, суспензій, порошків і аерозолів.
|
||||||||||||||||||||||||||||||||||||||||